
题目列表(包括答案和解析)
7.下列实验现象或结论描述正确的是 ( )
A.加热滴有酚酞的 (稀溶液):红色变浅
(稀溶液):红色变浅
B.含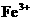 的溶液中滴入KSCN(溶液):产生红色沉淀
的溶液中滴入KSCN(溶液):产生红色沉淀
 C.稀溴水滴入含少量的苯酚浓溶液中:产生白色沉淀
C.稀溴水滴入含少量的苯酚浓溶液中:产生白色沉淀
D.将三氯化铝溶液蒸干,可得固体氯化铝
6.下列叙述不正确的是 ( )
A.构成分子晶体的微粒中一定含有共价键
B.只含有共价键的化合物一定是共价化合物
C.离子晶体中不一定只含有离子键
D.同主族元素形成的氧化物的晶体类型可能相同
5.下列对化学反应的认识错误的是 ( )
A.有化学键破坏的一定是化学反应 B.会产生新的物质
C.可能会引起物质状态的变化 D.一定伴随着能量的变化
4.下列物质溶于水时会破坏水的电离平衡,且属于电解质的是 ( )
A.氯气 B.二氧化碳 C.碘化钾 D.醋酸钠
2.月球上的每百吨 He聚变所释放出的能量相当于目前人类一年消耗的能量,地球上氦元素主要以
He聚变所释放出的能量相当于目前人类一年消耗的能量,地球上氦元素主要以 He的形式存在。已知一个
He的形式存在。已知一个 C原子的质量为ag,一个
C原子的质量为ag,一个 He原子的质量为bg,NA为阿伏伽德罗常数。下列说法正确的是 ( )
He原子的质量为bg,NA为阿伏伽德罗常数。下列说法正确的是 ( )
A. He比
He比 He多一个中子 B.氦元素的近似相对原子质量为3
He多一个中子 B.氦元素的近似相对原子质量为3
C. He的相对原子质量为
He的相对原子质量为 D.
D. He的摩尔质量为bNA
He的摩尔质量为bNA
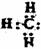 3.下列化学用语表示正确的是 ( )
3.下列化学用语表示正确的是 ( )
 A.甲基的电子式:
A.甲基的电子式:
B.氮原子的轨道表示式:
C.氯离子的最外层电子排布:3s23p6

D.硫离子的结构示意图:
1.上海要建成资源节约和生态保护型省份。下列措施或说法不符合这一理念的是( )
A.推广“绿色自由”计划,吸收空气中的CO2并利用廉价能源合成汽油
B.做好空气质量预报工作,以便污染程度高时好防护
C.工业废水的“再生”处理,用于道路保洁、城市喷泉和洗车等
D.利用风能、生物能发电,强制实施火力发电用煤的脱硫处理
24.(本题共14分)
A、B、C、D、E、F分别是KCl 、Mg(NO3)2、Ba(OH)2、AgNO3、Na2CO3、(NH4)2SO4六种溶液的一种,将它们两混合后,现象如下表。表中用“↑”代表产生气体,用“↓”代表产生沉淀,用“-”代表无现象。
|
|
A |
B |
C |
D |
E |
F |
|
A |
|
↑↓ |
- |
- |
↓ |
- |
|
B |
↑↓ |
|
↓ |
- |
↓ |
↓ |
|
C |
- |
↓ |
|
- |
- |
↓ |
|
D |
- |
- |
- |
|
↓ |
- |
|
E |
↓ |
↓ |
- |
↓ |
|
↓ |
|
F |
- |
↓ |
↓ |
- |
↓ |
|
试回答下列问题:
(1)这六种溶液分别是A B C D E F
(2)试写出A与B反应的离子方程式:
(3)向E中逐滴加入氨水的现象是
离子方程式为
23.(本题共10分)
下列三组物质中,均有一种物质的类别与其它三种不同
A.MgO、Na2O、CO2、CuO B.HCl、H2O、H2SO4、HNO3
C.NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A B C 。
(2)A、B、C三种物质相互作用可生成一种新物质,该反应 氧化还原反应(填“是”或“不是”)。这种新物质与盐酸反应的离子方程式为________________ 。
22.(本题共12分)
欲用98%的浓硫酸(ρ=1.84g/cm)配制成浓度为0.5mol/L的稀硫酸500mL。
(1)主要仪器有:量筒、烧杯、玻璃棒、 、 。
(2)简要回答下列问题:
①所需浓硫酸的体积为 ;
②如果实验室有15mL、20mL、50mL的量筒应选用 mL的最筒最好。
③在转入容量瓶前烧杯中液体应冷却至室温,否则会使结果浓度偏 。(填“高”、“低”、下同)
④定容时必须使溶液的凹液面的最低点与刻度相平,若俯视会使结果浓度偏
21.(本题共14分)
(1)实验室制取Fe(OH)3 胶体的方法是: 取一个小烧杯,加入25mL蒸馏水。将烧杯的蒸馏水加热至 ,向 中逐滴加入1~2mLFeCl3溶液。继续 至溶液呈红褐色,停止加热,即得到Fe(OH)3 胶体。
(2)己知反应(未配平): KMnO4+KCl+H2SO4=K2SO4+MnSO4+Cl2↑+H2O
①此反应的氧化剂是 ,氧化产物是 ,被氧化的元素 。(填化学式或元素符号)
②上述反应中若标准状况下产生11.2L气体物质,则转移电子的数目为 。
③上述反应中氧化剂与氧化产物的物质的量比为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com