
题目列表(包括答案和解析)
0. 5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是______________________。
5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是______________________。
 (6)在298
K下,Q、T的单质各1
mol完全燃烧,分别放出热量a
kJ和b
kJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3
mol Q的单质,则该反应在298
K下的△H=__________(注:题中所有单质均为最稳定单质)。
(6)在298
K下,Q、T的单质各1
mol完全燃烧,分别放出热量a
kJ和b
kJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3
mol Q的单质,则该反应在298
K下的△H=__________(注:题中所有单质均为最稳定单质)。
24.
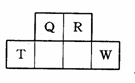 (14分)短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W最外层电子数比内层电子总数少4个,请回答下列问题:
(14分)短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W最外层电子数比内层电子总数少4个,请回答下列问题:
 (1)第四周期与W同主族的元素符号为___________。
(1)第四周期与W同主族的元素符号为___________。
 (2)元素Q和R的氢化物沸点关系为__________(用氢化物
(2)元素Q和R的氢化物沸点关系为__________(用氢化物
 化学式表示),其理由是_________________________________.
化学式表示),其理由是_________________________________.
 (3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式___________________________。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式___________________________。
 (4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是__________________________________。
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是__________________________________。
 (5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L的甲气体与
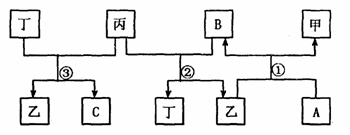
23. (12分)有A、B、C、D四种单质,在一定条件下,A、B、C分别跟D发生化合反应相应生成甲、乙、丙(甲、乙、丙每个分子中都含有10个电子),B与丙在该条件下反应只能生成丁和乙,而B跟C发生化合反应生成丁,这些单质和化合物之间发生如图所示的反应关系:
(12分)有A、B、C、D四种单质,在一定条件下,A、B、C分别跟D发生化合反应相应生成甲、乙、丙(甲、乙、丙每个分子中都含有10个电子),B与丙在该条件下反应只能生成丁和乙,而B跟C发生化合反应生成丁,这些单质和化合物之间发生如图所示的反应关系:

 (1)写出下列物质的化学式:
(1)写出下列物质的化学式:
 甲_____________________________________,
甲_____________________________________,
 乙______________________________________,
乙______________________________________,
 丙______________________________________;
丙______________________________________;
 (2)写出反应①②③的化学方程式:
(2)写出反应①②③的化学方程式:
 ①________________________________________________________________________;
①________________________________________________________________________;
 ②________________________________________________________________________;
②________________________________________________________________________;
 ③________________________________________________________________________;
③________________________________________________________________________;
22. (12分)在2 L密闭容器内充入1
molA和2.4
mol B,发
(12分)在2 L密闭容器内充入1
molA和2.4
mol B,发

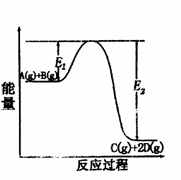 生反应:A(g)+B(g)
生反应:A(g)+B(g)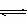 C(g)+2D(g),t
min
C(g)+2D(g),t
min
 (t>2)后达到化学平衡。反应过程中的能量变化如图所
(t>2)后达到化学平衡。反应过程中的能量变化如图所
 示,回答下列问题。
示,回答下列问题。
 (1)该反应是___________反应(填“吸热”、“放热”)。
(1)该反应是___________反应(填“吸热”、“放热”)。
 (2)反应体系中加入催化剂,反应体系的温度是否改变?___________________,原因是___________________________________________________
(2)反应体系中加入催化剂,反应体系的温度是否改变?___________________,原因是___________________________________________________
 (3)如果反应速率ν(A)=0.05
mol/(L·min),2
min时,生成D的物质的量为_____________mol。
(3)如果反应速率ν(A)=0.05
mol/(L·min),2
min时,生成D的物质的量为_____________mol。
 (4)在某温度下,达到平衡后,A的转化率为60%,此时B的转化率为____________;
(4)在某温度下,达到平衡后,A的转化率为60%,此时B的转化率为____________;
 (5)若在相同温度下,在一个体积可变的容器中充入1
molA和2.4
molB,达到平衡后,则A的转化率_______________60%(填”<”、”>”或”=”)。其理由是__________________________________________________________________.
(5)若在相同温度下,在一个体积可变的容器中充入1
molA和2.4
molB,达到平衡后,则A的转化率_______________60%(填”<”、”>”或”=”)。其理由是__________________________________________________________________.

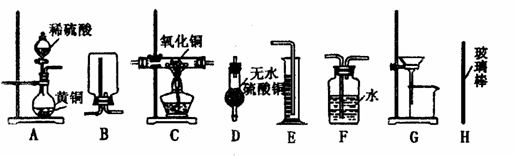
21. (12分)实验室有黄铜(铜和锌两种金属的混合物)粉末,请你利用给出的实验仪器及实验数据,设计二种测定该样品中锌的质量分数的方案。
(12分)实验室有黄铜(铜和锌两种金属的混合物)粉末,请你利用给出的实验仪器及实验数据,设计二种测定该样品中锌的质量分数的方案。
 I.除托盘天平必用外,供选择的实验装置如下图所示:
I.除托盘天平必用外,供选择的实验装置如下图所示:

 Ⅱ.实验中可测得的数据:
Ⅱ.实验中可测得的数据:
 ①黄铜的质量a
g。
①黄铜的质量a
g。
 ②充分反应后在标准状况下生成氢气的体积为b
L。
②充分反应后在标准状况下生成氢气的体积为b
L。
 ③反应前仪器和药品的质最为c
g。
③反应前仪器和药品的质最为c
g。
 ④充分反应后剩余固体的质量为d
g。
④充分反应后剩余固体的质量为d
g。
 ⑤充分反应后仪器和药品的质量为e
g。
⑤充分反应后仪器和药品的质量为e
g。
 请填写下列表格中有关内容:
请填写下列表格中有关内容:
|
|
实验装置 (填写装置序号) (填写装置序号) |
测得的数据 (填写数据序号) (填写数据序号) |
锌的质量分数 (用a、b、c、d、e表示) (用a、b、c、d、e表示) |
|
方案一 |
|
|
|
|
方案二 |
|
|
|
2. 答卷前将密封线内的项目填写清楚。
答卷前将密封线内的项目填写清楚。
1. 第Ⅱ卷共4页,用钢笔或圆珠笔直接写在试题卷上。
第Ⅱ卷共4页,用钢笔或圆珠笔直接写在试题卷上。
20. 在由Fe、FeO和Fe2O3组成的混合物中加入100
mL 2 mol/L的盐酸,恰好使混合物完全溶解,并放出448
mL气体(标准状况下),此时溶液中无Fe3+。则下列判断正确的是
在由Fe、FeO和Fe2O3组成的混合物中加入100
mL 2 mol/L的盐酸,恰好使混合物完全溶解,并放出448
mL气体(标准状况下),此时溶液中无Fe3+。则下列判断正确的是
 A.混合物中三种物质反应时消耗盐酸的物质的量之比为1
:1
:3
A.混合物中三种物质反应时消耗盐酸的物质的量之比为1
:1
:3
 B.反应后所得溶液中的Fe2+和Cl-的物质的量之比为1
:3
B.反应后所得溶液中的Fe2+和Cl-的物质的量之比为1
:3
 C.混合物中,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多
C.混合物中,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多
 D.混合物中,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多
D.混合物中,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多

 第Ⅱ卷(非选择题,共60分)
第Ⅱ卷(非选择题,共60分)
 注意事项:
注意事项:
19.
 右图为用某浓度的NaOH溶液(Y),滴定10
mL某浓度的HCl溶液(X)的图象,据此推断NaOH溶液和HCI溶液的物质的量浓度是
右图为用某浓度的NaOH溶液(Y),滴定10
mL某浓度的HCl溶液(X)的图象,据此推断NaOH溶液和HCI溶液的物质的量浓度是
|
|
A |
B |
C |
D |
|
X溶液/mol·L-1 |
0.15 |
0.09 |
0.08 |
0.04 |
|
Y溶液/mol·L-1 |
0.05 |
0.03 |
0.16 |
0.12 |
18. 将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后所得的固体物质是
将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后所得的固体物质是
 A.Na2SiO3 B.Na2CO3、Na2SiO3
A.Na2SiO3 B.Na2CO3、Na2SiO3
 C.Na2CO3、SiO2 D.SiO2
C.Na2CO3、SiO2 D.SiO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com