
题目列表(包括答案和解析)
11.常温下,0.1mol·L-1某一元酸(HA)溶液中c(OH-)/ c(H+)=1×10-8,下列叙述正确的
是 ( )
A.该溶液中由水电离出的c(H+)=1×10-3 mol·L-1
B.由pH=3的HA与pH=11的NaOH溶液等体积混合,溶液中c(Na+)>c(A-)>c(OH-)>c(H+)
 C.浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,
C.浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,
则c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-)
D.0.1 mol·L-1HA溶液与0.05 mol·L-1NaOH溶液等体积混合后溶液中
2 c(H+)+ c(HA)= c(A-)+2 c(OH-)
10.混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留
固体不是纯净物的是 ( )
A.向Fe、FeO和Fe2O3的混合物中加入过量的盐酸
B.等物质的量浓度、等体积的(NH4)2SO4与BaCl2溶液
C.等物质的量的NaHCO3溶液与Na2O2固体
D.在NaBr溶液中通入过量氯气
9.下列说法不正确的是 ( )
① △H<0,△S>0的化学反应一定能自发进行
② 若R2-和M+的电子层结构相同,则原子序数:R>M
③ F2、Cl2、Br2、I2熔点随相对分子质量增大而升高
④ NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤ 若X的质子数为a,中子数为b,则原子可表示为abX
⑥ 原电池在工作时电子由负极通过溶液流向正极
⑦ 由于氨和水分子之间能形成氢键,NH3分子极易溶于水
⑧ 原子序数为34号的元素属于长周期的副族元素
A.②⑤⑥⑧ B.①③④⑤ C.②④⑤⑦ D.③⑤⑦⑧
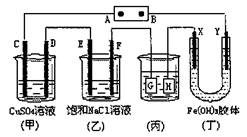
8.如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴
入酚酞溶液,在F极附近显红色。则以下说法正确的是 ( )
 A.电极B极是正极
A.电极B极是正极
B.(甲)、(乙)装置的C、D、E、F
电极均有单质生成,其物质的量之
比1:2:2:2
C.欲用(丙)装置给铜镀银,H应该
是Ag,电镀液是AgNO3溶液
D.装置(丁)中看到的现象是X极附
近红褐色变深
7.室温时,某溶液中水电离出的c(H+)=10-13mol/L,下列离子在溶液中一定能大量共存的是( )
A.Fe3+、NH4+、Cl-、I- B.Ba2+、Na+、Cl-、NO3-
C.K+、HCO3-、Br-、Ba2+ D.K+、CO32-、NO3-、Al3+
6.下列各项中的两个量,其比值一定为2:1的是 ( )
A.100mL1.0mol·L-1Fe(NO3) 2溶液与200ml 0.5mol·L-1HNO3溶液混合,混合前和混
合后c(NO3-)之比
B.相同温度下,0.2 mol·L-1醋酸溶液与0.1 mol·L-1醋酸溶液中c(H+)之比
C.NH4+浓度相同时,CH3COONH4溶液与(NH4) 2SO4溶液的物质的量浓度之比
 D.室温时pH=2的HCl溶液与pH=12的Ba(OH)
2溶液的物质的量浓度之比
D.室温时pH=2的HCl溶液与pH=12的Ba(OH)
2溶液的物质的量浓度之比
5.下列离子方程式中正确的是 ( )
A.NaHCO3溶液与足量的Ca(OH)2溶液:Ca2++2HCO3-+2OH-=2H2O+CaCO3↓+CO32-
B.铜与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
C.氯化铝溶液与过量的氨水反应:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D.氯气通入水中:Cl2+H2O=Cl-+ClO-+2H+
4.下列对有关实验事实的解释正确的是 ( )
A.酸性KMnO4溶液中通入SO2后,颜色褪去,是因为SO2具有漂白性
B.铁在海水中比在淡水中更易腐蚀,是因为海水中含丰富的氧气
C.常温下,将铝片放入浓硫酸中无明显现象,是因为铝不和冷的浓硫酸反应
D.浓硝酸在光照条件下变黄,是因为浓硝酸分解生成的有色产物溶于浓硝酸
3.设NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.常温常压下33.6LCl2与足量Fe反应,转移的电子数为3NA
B.1molNO2与足量H2O反应,转移的电子数为NA
C.由CO2和O2组成的混合物共有NA个分子,其中的氧原子数为2NA
D.1molCO2分子中共价键总数为2NA
2.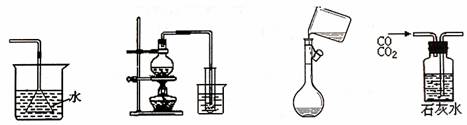 下列装置能达到实验目的的是 ( )
下列装置能达到实验目的的是 ( )
A.吸收氨气制氨气 B.制取少量蒸馏水 C.转移溶液 D.除去杂质气体CO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com