
题目列表(包括答案和解析)
I类: 在恒温恒容下,对于化学反应前后气体体积发生变化的可逆反应,只改变起始加入物质的物质的量,如果通过可逆反应的化学计量数之比换算成化学方程式的同一边物质的物质的量与原平衡相同,则两平衡等效。
例1:在一定温度下,把2mol SO2和1mol
O2通入一定容积的密闭容器中,发生如下反应,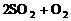

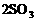 ,当此反应进行到一定程度时反应混合物就处于化学平衡状态。现在该容器中维持温度不变,令a、b、c分别代表初始时加入的
,当此反应进行到一定程度时反应混合物就处于化学平衡状态。现在该容器中维持温度不变,令a、b、c分别代表初始时加入的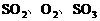 的物质的量(mol),如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡状态时,反应混合物中三种气体的百分含量仍跟上述平衡完全相同。请填空:
的物质的量(mol),如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡状态时,反应混合物中三种气体的百分含量仍跟上述平衡完全相同。请填空:
(1)若a=0,b=0,则c=___________。
(2)若a=0.5,则b=___________,c=___________。
(3)a、b、c的取值必须满足的一般条件是___________,___________。(请用两个方程式表示,其中一个只含a和c,另一个只含b和c)
解析:通过化学方程式: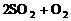

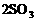 可以看出,这是一个化学反应前后气体分子数不等的可逆反应,在定温、定容下建立的同一化学平衡状态。起始时,无论怎样改变
可以看出,这是一个化学反应前后气体分子数不等的可逆反应,在定温、定容下建立的同一化学平衡状态。起始时,无论怎样改变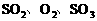 的物质的量,使化学反应从正反应开始,还是从逆反应开始,或者从正、逆反应同时开始,但它们所建立起来的化学平衡状态的效果是完全相同的,即它们之间存在等效平衡关系。我们常采用“等价转换”的方法,分析和解决等效平衡问题。
的物质的量,使化学反应从正反应开始,还是从逆反应开始,或者从正、逆反应同时开始,但它们所建立起来的化学平衡状态的效果是完全相同的,即它们之间存在等效平衡关系。我们常采用“等价转换”的方法,分析和解决等效平衡问题。
(1)若a=0,b=0,这说明反应是从逆反应开始,通过化学方程式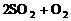

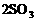 可以看出,反应从2mol SO3开始,通过反应的化学计量数之比换算成
可以看出,反应从2mol SO3开始,通过反应的化学计量数之比换算成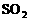 和
和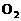 的物质的量(即等价转换),恰好跟反应从2mol SO2和1mol O2的混合物开始是等效的,故c=2。
的物质的量(即等价转换),恰好跟反应从2mol SO2和1mol O2的混合物开始是等效的,故c=2。
(2)由于a=0.5<2,这表示反应从正、逆反应同时开始,通过化学方程式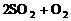

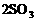 可以看出,要使0.5 mol SO2反应需要同时加入0.25mol O2才能进行,通过反应的化学计量数之比换算成SO3的物质的量(即等价转换)与0.5 mol SO3是等效的,这时若再加入1.5 mol SO3就与起始时加入2 mol SO3是等效的,通过等价转换可知也与起始时加入2 mol SO2和1mol O2是等效的。故b=0.25,c=1.5。
可以看出,要使0.5 mol SO2反应需要同时加入0.25mol O2才能进行,通过反应的化学计量数之比换算成SO3的物质的量(即等价转换)与0.5 mol SO3是等效的,这时若再加入1.5 mol SO3就与起始时加入2 mol SO3是等效的,通过等价转换可知也与起始时加入2 mol SO2和1mol O2是等效的。故b=0.25,c=1.5。
(3)题中要求2mol
SO2和1mol O2要与a mol SO2、b mol O2和c mol SO3建立等效平衡。由化学方程式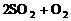

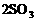 可知,c mol SO3等价转换后与c mol SO2和
可知,c mol SO3等价转换后与c mol SO2和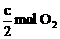 等效,即是说,
等效,即是说, 和
和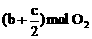 与a mol SO2、b mol O2和c mol SO3等效,那么也就是与2mol SO2和1mol O2等效。故有
与a mol SO2、b mol O2和c mol SO3等效,那么也就是与2mol SO2和1mol O2等效。故有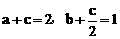 。
。
II类: 在恒温恒容下,对于反应前后气体体积不变的可逆反应,只要反应物(或生成物)的物质的量之比与原平衡相同,则两平衡等效。
例2:在一个固定容积的密闭容器中,保持一定的温度进行以下反应:
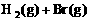

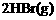
已知加入1mol H2和2mol Br2时,达到平衡后生成a mol HBr(见下表已知项),在相同条件下,且保持平衡时各组分的体积分数不变,对下列编号①-③的状态,填写下表中的空白。
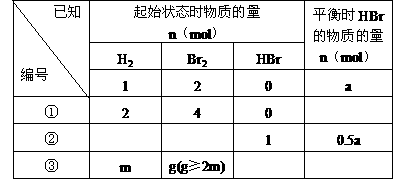
解析:在定温、定容下,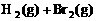

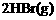 建立起化学平衡状态,从化学方程式可以看出,这是一个化学反应前后气体分子数相等的可逆反应。根据“等价转换”法,通过反应的化学计量数之比换算成同一边物质的物质的量之比与原平衡相同,则达到平衡后与原平衡等效。
建立起化学平衡状态,从化学方程式可以看出,这是一个化学反应前后气体分子数相等的可逆反应。根据“等价转换”法,通过反应的化学计量数之比换算成同一边物质的物质的量之比与原平衡相同,则达到平衡后与原平衡等效。
①因为标准项中n(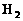 起始):n(
起始):n(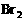 起始):n(HBr平衡)=1:2:a,将n(H2起始)=2mol,n(Br2起始)=4mol,代入上式得n(HBr平衡)=2a。
起始):n(HBr平衡)=1:2:a,将n(H2起始)=2mol,n(Br2起始)=4mol,代入上式得n(HBr平衡)=2a。
②参照标准项可知,n(HBr平衡)=0.5a mol,需要n(H2起始)=0.5mol,n(Br2起始)=1mol,n(HBr起始)=0mol。而现在的起始状态,已有1mol HBr,通过等价转换以后,就相当于起始时有0.5 mol H2和0.5 mol Br2的混合物,为使n(H2起始):n(Br2起始)=1:2,则需要再加入0.5 mol Br2就可以达到了。故起始时H2和Br2的物质的量应为0mol和0.5mol。
③设起始时HBr的物质的量为x mol,转换成H2和Br2后,则H2和Br2的总量分别为(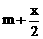 )mol和(
)mol和(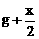 )mol,根据
)mol,根据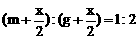 ,解得
,解得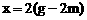 。设平衡时HBr的物质的量为y mol,则有
。设平衡时HBr的物质的量为y mol,则有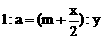 ,解得
,解得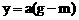 。
。
III类: 在恒温恒压下,改变起始时加入物质的物质的量,只要按化学计量数之比换算成化学方程式的同一边物质的物质的量之比与原平衡相同,达到平衡状态后与原平衡等效。
例3:如图所示,在一定温度下,把2体积N2和6体积H2通入一个带有活塞的容积可变的容器中,活塞的一端与大气相通,容器中发生以下反应: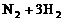

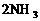 (正反应放热),若反应达到平衡后,测得混合气体的体积为7体积。据此回答下列问题:
(正反应放热),若反应达到平衡后,测得混合气体的体积为7体积。据此回答下列问题:

(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各气体的体积分数仍与上述平衡相同,那么:
①若a=1,c=2,则b=_________。在此情况下,反应起始时将向_________(填“正”或“逆”)反应方向进行。
②若需规定起始时反应向逆反应方向进行,则c的取值范围是_________。
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是_________,原因是_________。
解析:(1)①化学反应: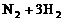

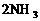 在定温、定压下进行,要使平衡状态与原平衡状态等效,只要起始时
在定温、定压下进行,要使平衡状态与原平衡状态等效,只要起始时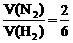 就可以达到。已知起始时各物质的体积分别为1体积N2、b体积H2和2体积
就可以达到。已知起始时各物质的体积分别为1体积N2、b体积H2和2体积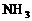 。根据“等价转换”法,将2体积
。根据“等价转换”法,将2体积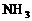 通过反应的化学计量数之比换算成
通过反应的化学计量数之比换算成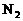 和
和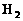 的体积,则相当于起始时有(1+1)体积
的体积,则相当于起始时有(1+1)体积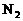 和(b+3)体积
和(b+3)体积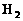 ,它们的比值为
,它们的比值为 ,解得b=3。
,解得b=3。
因反应前混合气体为8体积,反应后混合气体为7体积,体积差为1体积,由差量法可解出平衡时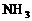 为1体积;而在起始时,
为1体积;而在起始时,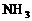 的体积为c=2体积,比平衡状态时大,为达到同一平衡状态,
的体积为c=2体积,比平衡状态时大,为达到同一平衡状态,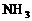 的体积必须减小,所以平衡逆向移动。
的体积必须减小,所以平衡逆向移动。
②若需让反应逆向进行,由上述①所求出的平衡时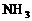 的体积为1可知,
的体积为1可知,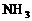 的体积必须大于1,最大值则为2体积
的体积必须大于1,最大值则为2体积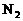 和6体积
和6体积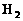 完全反应时产生的
完全反应时产生的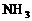 的体积,即为4体积,则
的体积,即为4体积,则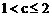 。
。
(2)由6.5<7可知,上述平衡应向体积缩小的方向移动,亦即向放热方向移动,所以采取降温措施。
例4:(一)恒温、恒压下,在一个容积可变的容器中发生如下反应:
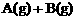

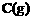
(1)若开始时放入1mol A和1mol B,达到平衡后,生成a mol C,这时A的物质的量为________ mol。
(2)若开始时放入3mol A和3mol B,达到平衡后,生成C的物质的量为_________mol。
(3)若开始时放入x mol A、2mol B和1mol C,达到平衡后,A和C的物质的量分别为y mol和3a mol,则x=________,y=________。平衡时,B的物质的量________(填编号)。
(甲)大于2mol (乙)等于2mol (丙)小于2mol (丁)可能大于、等于或小于2mol
(4)若在(3)的平衡混合物中再加入3mol C,待再次达到平衡后,C的物质的量分数是___________。
在等效平衡中比较常见并且重要的类型主要有以下三种:
I类:恒温恒容下对于反应前后气体体积发生变化的反应来说(即△V≠0的体系):等价转化后,对应各物质起始投料的物质的量与原平衡起始态相同。
II类:恒温恒容下对于反应前后气体体积没有变化的反应来说(即△V=0的体系):等价转化后,只要反应物(或生成物)的物质的量的比例与原平衡起始态相同,两平衡等效。
III类:恒温恒压下对于气体体系等效转化后,要反应物(或生成物)的物质的量的比例与原平衡起始态相同,两平衡等效。
解题的关键,读题时注意勾画出这些条件,分清类别,用相应的方法求解。我们常采用“等价转换”的方法,分析和解决等效平衡问题
在一定条件(恒温恒容或恒温恒压)下,同一可逆反应体系,不管是从正反应开始,还是从逆反应开始,在达到化学平衡状态时,任何相同组分的百分含量(体积分数、物质的量分数等)均相同,这样的化学平衡互称等效平衡(包括“相同的平衡状态”)。
概念的理解:
(1)外界条件相同:通常可以是①恒温、恒容,②恒温、恒压。
(2)“等效平衡”与“完全相同的平衡状态”不同:“完全相同的平衡状态” 是指在达到平衡状态时,任何组分的物质的量分数(或体积分数)对应相等,并且反应的速率等也相同,但各组分的物质的量、浓度可能不同。而“等效平衡”只要求平衡混合物中各组分的物质的量分数(或体积分数)对应相同,反应的速率、压强等可以不同
(3)平衡状态只与始态有关,而与途径无关,(如:①无论反应从正反应方向开始,还是从逆反应方向开始②投料是一次还是分成几次③反应容器经过扩大-缩小或缩小-扩大的过程,)只要起始浓度相当,就达到相同的平衡状态。
29.(10分)元素的电离能对元素的性质影响很大。
(1)观察下表总结三条有关第一电离能变化的规律
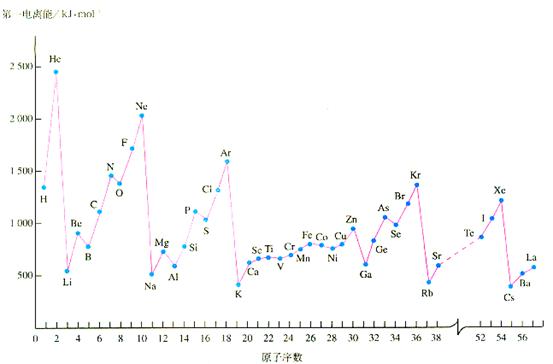
例如:同周期主族元素的第一电离能的变化趋势是由小变大;
;
;
。
(2)
|
|
Li |
Na |
K |
|
熔点 |
180 |
98 |
63 |
|
沸点 |
1347 |
881 |
756 |

根据以上三个图表回答:(M表示碱金属)
△H2(Li) △H2(Na), △H3(Li) △H3(Na),
已知金属锂比钠活泼,则△H4(Li) △H4(Na)。
(3)钒(V)原子的基态电子排布式为: ,钒元素的最高化合价为 。
(4)CuO受热易分解为Cu2O和O2,请从铜的原子结构来说明CuO受热易分解的原因:
。
28.(10分)已知羰基化合物与饱和NaHSO3溶液可以发生以下反应:
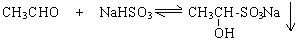
(1)羰基化合物和饱和NaHSO3的反应速率如下:
|
羰基化合物 |
CH3CHO |
CH3COCH3 |
C2H5COCH3 |
CH3CH2CH2COCH3 |
|
产率(1小时内) |
88.7 |
56.2 |
36.4 |
23.4 |
|
羰基化合物 |
(CH3)2CHCOCH3 |
(CH3)3CCOCH3 |
C2H5COC2H5 |
C6H5COCH3 |
|
产率(1小时内) |
12.3 |
5.6 |
2 |
1 |
可见,取代基对羰基化合物和NaHSO3反应的影响有(写出3条即可)
①
②
③
(2)利用以上可逆反应可以分离醛和酮的混合物,请写出能使醛与NaHSO3生成的沉淀重新溶解的试剂的化学式 (写出2种,属于不同类别的物质。)
(3)检验甲基酮(RCOCH3)通常用到下列2步反应来生成难溶于水的氯仿。
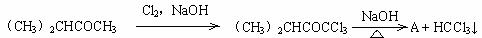
①写出第一步反应的化学方程式
②写出A的结构简式
(4)苯甲醛在浓碱作用下反应生成苯甲酸盐和苯甲醇,此反应的类型是 。
27.(10分)为测定某有机化合物A的结构,进行如下实验。
[分子式的确定]
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下)。则该物质中各元素的原子个数比是 ;
(2)质谱仪测定有机化合物的相对分子质量为46,则该物质的分子式是 ;
(3)根据价键理论,预测A的可能结构并写出结构简式 。
[结构式的确定]
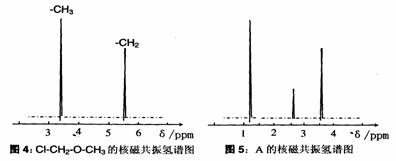
(4)核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚
(Cl-CH2-O-CH3)有两种氢原子(图4)。经测定,有机物A的核磁共振氢谱示意图如图5,则A的结构简式为 。
[性质实验]
(5)A在一定条件下脱水可生成B,B可合成包装塑料C,请写出B转化为C的化学反应方程式: 。
(6)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉。请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应方程式: 。
(7)A可通过粮食在一定条件下制得,由粮食制得的A在一定温度下密闭储存,因为发生一系列的化学变化而变得更醇香。请写出最后一步反应的化学方程式:
。
26.(10分)10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
|
温度(℃) |
10 |
20 |
30 |
加热煮沸后冷却到50℃ |
|
pH |
8.3 |
8.4 |
8.5 |
8.8 |
甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为 。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3。丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则 (填“甲”或“乙”)判断正确。试剂X是 。
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH (填“高于”、“低于”或“等于”)8.3,则 (填“甲”或“乙”)判断正确。
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言 (填“甲”或“乙”)判断是错误的,理由是 。
25.(10分)在元素周期表中,锌(30Zn)、镉(48Cd)、汞(80Hg)同属于锌族,锌和汞在自然界中常共生,镉的金属活动性介于锌和汞之间。湿法炼锌过程中产生的铜镉渣中含有Cu、Cd、Zn等多种金属,可用于生产金属镉。镉的主要用途可以用作镍-镉电池,以及用于颜料生产,镉化合物还在PVC稳定剂、发光材料、半导体材料、杀菌剂等方面有广泛的应用。镉的生产流程如图示意如下:
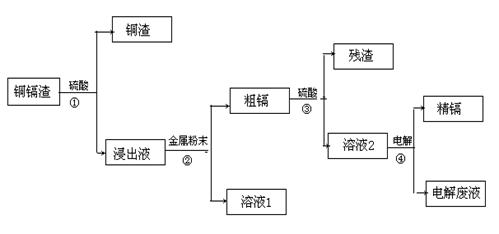
请回答下列问题:
(1)镉元素位于周期表中第 周期,第 族,其原子结构示意图为 ;
(2)写出步骤①反应的离子方程式 。
(3)步骤②所加入的金属是 。
(4)步骤④用“溶液2”作电解液,镉在 极析出,该电极材料是
(5)“电解废液”中含有镉,不能直接作为污水排放。目前含镉的废水处理的方式有两种,一种是在含镉污水中加入硫化钠,沉淀镉离子,另一种是加入聚合硫酸铁和聚合氯化铝,沉淀镉离子。写出硫化钠沉淀镉离子的离子方程式 。
24.(10分)纯三氟化氮(NF3)在集成电路、大型屏幕液晶显示屏(TFT-LCD)的生产中,作为清洗剂之用。
三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)NF3的电子式为 。
(2)写出该反应的化学方程式。 。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体泄漏时的现象是 。
(4)一旦NF3泄漏,可以用喷淋 溶液的方法减少污染。
(5)一种生产NF3的方法:氟气与液态氟化氢铵(NH4HF2)反应,产生NF3。
写出该反应的化学方程式:
23.(13分)过碳酸钠俗称固体双氧水,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,它的制备原理和路线如下:
2Na2CO3 + 3H2O2 = 2 Na2CO3·3H2O2 △H<0
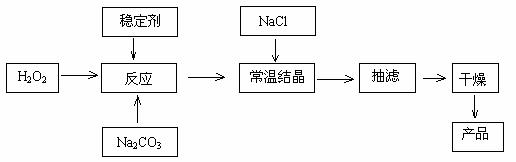
回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是 。
(2)下列物质可使过碳酸钠较快失效的是 。
A.MnO2 B.H2S C.稀硫酸 D.NaHCO3
(3)加入NaCl的作用是 。
(4)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与Fe3+生成稳定的配合物,Fe3+对反应的不良影响是 。
(5)反应的最佳温度控制在15℃-20℃,温度偏高时造成产率低的可能原因有 ,温度偏低时造成产率低的可能原因有 。
(6)以上生产流程中遗漏了一步,造成所得产品纯度偏低,该步操作的名称是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com