
题目列表(包括答案和解析)
10.
下列类型的反应,一定发生电子转移的是( ) ()1世纪教育网
()1世纪教育网
 A. 化合反应
B. 分解反应 C. 置换反应 D.
复分解反应
A. 化合反应
B. 分解反应 C. 置换反应 D.
复分解反应
9. 下列各组气体在常温下能共存且能用向上排空气法收集的是( )
下列各组气体在常温下能共存且能用向上排空气法收集的是( )
 A.NO和O2 B.HCI和NH3
A.NO和O2 B.HCI和NH3
 C.H2和CO D.SO2和CO2 Blog/?UserId=997609
C.H2和CO D.SO2和CO2 Blog/?UserId=997609

8.下列说法正确的是( )
 A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红
A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红
 B.Al3+、NO3-
、Cl-、CO32 -、Na+可大量共存于pH=2的溶液中
B.Al3+、NO3-
、Cl-、CO32 -、Na+可大量共存于pH=2的溶液中
 C.乙醇和乙酸都能溶于水,都是电解质
C.乙醇和乙酸都能溶于水,都是电解质
 D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同
D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同
7.下列关于硅单质及其化合物的说法正确的是( )
 ①硅是构成一些岩石和矿物的基本元素
①硅是构成一些岩石和矿物的基本元素
 ②水泥、玻璃、水晶饰物都是硅酸盐制品
②水泥、玻璃、水晶饰物都是硅酸盐制品
 ③高纯度的硅单质广泛用于制作光导纤维
③高纯度的硅单质广泛用于制作光导纤维
 ④陶瓷是人类应用很早的硅酸盐材料
④陶瓷是人类应用很早的硅酸盐材料
 A.①② B.②③ C.①④ D.③④
A.①② B.②③ C.①④ D.③④
1:.  下列有关化学用语使用正确的是( )
下列有关化学用语使用正确的是( )
A. 硫原子的原子结构示意图: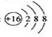
B.NH4Cl的电子式: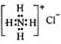
C.原子核内有10个中子的氧原子:
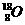
 D.对氯甲苯的结构简式:
D.对氯甲苯的结构简式: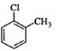
2 :X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是( )
 A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
 B.元素X不能与元素Y形成化合物
B.元素X不能与元素Y形成化合物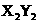
 C.元素Y、R分别与元素X形成的化合物的热稳定性:
C.元素Y、R分别与元素X形成的化合物的热稳定性: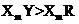
 D.元素W、R的最高价氧化物的水化物都是强酸
D.元素W、R的最高价氧化物的水化物都是强酸
3:. 下列离子方程式与所述事实相符且正确的是( )
 A.漂白粉溶液在空气中失效:
A.漂白粉溶液在空气中失效: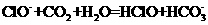
 B.用浓盐酸与
B.用浓盐酸与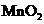 反应制取少量氯气:
反应制取少量氯气: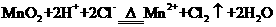
 C.向
C.向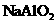 溶液中通入过量
溶液中通入过量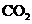 制
制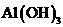 :
:

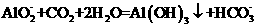
 D.在强碱溶液中次氯酸钠与
D.在强碱溶液中次氯酸钠与 反应生成
反应生成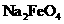 :
:

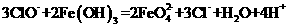
4:.用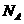 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是 ( )高.考.资.源.网
( )高.考.资.源.网
 A.标准状况下,5.6L一氧化氮和5.6L氧气混合后的分子总数为0.5
A.标准状况下,5.6L一氧化氮和5.6L氧气混合后的分子总数为0.5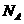
 B.
1mol乙烷分子含有8
B.
1mol乙烷分子含有8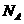 个共价键Blog/?UserId=997609
个共价键Blog/?UserId=997609
C.22.4 L Cl2中含有nA个C12分子
D.在1L0.1mol·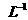 碳酸钠溶液中,阴离子总数大于0.1
碳酸钠溶液中,阴离子总数大于0.1 
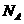
5:已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高。则下列溶液沸点最高的是( )
 A.0.01mol·
A.0.01mol·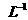 的蔗糖溶液
B. 0.01mol·
的蔗糖溶液
B. 0.01mol·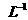 的
的 溶液
溶液
 C.0.02mol·
C.0.02mol·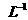 的
的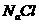 溶液
D. 0.02mol·
溶液
D. 0.02mol·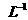 的
的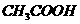 溶液
溶液
6.下列实验能达到实验目的且符合安全要求的是( )


23.(12分)在一个容积为2L的密闭容器中,加入0.8mol的A2气体和0.6mol B2气体,一定条件下发生如下反应:A2(g)+B2(g) 2AB+(g)△H<0,反应中各物质的浓度随时间的变化情况如图所示。(1)该反应进行到
时达到平衡,
用AB表示的平均反应速率为:
(分数表示)。
(2)图中对应的a的数值是 ,
该反应的化学平衡常数Kc=
(保留分数)
温度升高Kc值 (填“增大”、
“减少”或“不变”)
(3)在上述反应达到平衡后,第4min时,若将容器的体积快速扩大一倍(其他条件不变),请在上图中画出4min~5min的AB浓度的变化线。
(4)在相同条件下,若开始时向此容器中国入的A2(g)、B2(g)和AB(g)的物质的量分别为amol、bmol、cmol,要使达平衡时各物质的体积分数不变,则a、b、c应满足的关系是 (用含a、b、c的代数式表示)。
24(12分) 按照右图所示装置进行有关实验,
按照右图所示装置进行有关实验,
拔掉分液漏斗玻璃塞,将A逐滴加入B中。
(1)①若A是浓盐酸,B为二氧化锰,
当将A滴入B中时发生反应的离子方程式
为:
;
当实验一段时间后,发现C、D中有红棕色烟,则C的化学式为: 。
②实验室常用MnO2与浓盐酸共热制取Cl2,也可用KClO3,KMnO4,K2Cr2O7代替MnO2与浓盐酸反应制Cl2。若制取等量的Cl2需浓盐酸最少的是
A.KClO3和浓盐酸反应 B.MnO2和浓盐酸反应
C.KMnO4和浓盐酸反应 D.K2Cr2O7和浓盐酸反应
③在实验室中,要获得干燥纯净的氯气,可以将它通过下图中的装置,其中瓶I中盛放的是 。
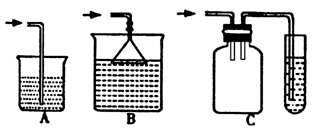 ④实验中多余的氯气必须吸收,以免污染空气。下图是实验室用NaOH吸收氯气的装置,为防止产生倒吸现象,合理的装置是
。
④实验中多余的氯气必须吸收,以免污染空气。下图是实验室用NaOH吸收氯气的装置,为防止产生倒吸现象,合理的装置是
。
(2)若A是乙醇,B是生石灰,实验中观察到C中黑色固体逐渐变红。当C中
黑色固体大部分变红时,关闭F,然后往烧杯中加入热水,静止一会,观察到III中试管壁出现了光亮的银镜。则C是 ,
试管E中所发生反应的离子方程式 。
22、(6分)做好环境消毒是预防“甲型H1N1流感”的重要措施,防控专家表示,含氯消毒剂和过氧化物消毒可防甲型H1N1流感。
(1)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,实验室可通过以下反应制得ClO2(未配平):KClO3+H2C2O4+H2SO4===ClO2↑+K2SO4+CO2↑+H2O.
在上述反应中 做氧化剂 ;0.5 mol KClO3参加反应有 个电子转移。
(2)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了氧化反应的是 。
A.稀硫酸 B.KMnO4溶液 C.稀盐酸 D.Na2SO3溶液
21.(10分)A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别位于同一主族,A是自然界中原子半径最小的元素,B的最外层电子数是内层电子数的3倍。
(1)写出B的元素符号:B_________,C的原子结构示意图____________;
(2)B与D的氢化物较稳定的是 (填化学式),其中所含有的化学键类型为 ;
(3)将A2D和DB2混合,发生反应的化学方程式为___________________;
(4)写出两种均含A、B、C、D四种元素的化合物相互间发生反应,且生成气体的离子方程式 。
20.化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学
键时释放(或吸收)出的能量。
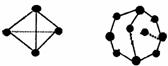 已知白磷和P4O6的分子结构如图所示:
已知白磷和P4O6的分子结构如图所示:
现提供以下化学键的键能(kJ·mol-1)
P-P 198 P-O 360 O-O 498
则反应P4(白磷)+3O2→P4O6的反应热△H为 ( )
A.-1638kJ/mol B.+1638kJ/mol
C.-126kJ/mol D.+126kJ/mol
第Ⅱ卷(非选择题 共40分)
19.用过量的H2SO4、NaOH、NH3·H2O、NaCl等溶液,
按图示步骤分开五种离子,则溶液①④是
A.①NH3·H2O ④NaCl
B.①NaCl ④H2SO4
C.①NaOH ④ H2SO4
D.①H2SO4 ④NaCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com