
题目列表(包括答案和解析)
13.有下列五个化学方程式(X、Y、Z均为正值):
①C2H2(g)+H2(g)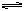 C2H4(g)
C2H4(g)
②CH4(g)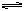 H2(g)+
H2(g)+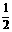 C2H4(g)
C2H4(g)
③C(s)+2H2(g)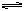 CH4(g);△H=
-X kJ·mol-1
CH4(g);△H=
-X kJ·mol-1
④C(s)+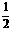 H2(g)
H2(g)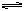
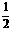 C2H2(g);△H= -Y kJ·mol-1
C2H2(g);△H= -Y kJ·mol-1
⑤C(s)+H2(g)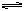
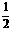 C2H4(g)△H= -ZkJ·mol-1
C2H4(g)△H= -ZkJ·mol-1
当温度下降时①式平衡向右移动,②式平衡向左移动。据此判定③-⑤式中关于X、Y、Z的大小顺序排列正确的是:
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Y>Z>X
12.甲、乙、丙、丁四种短周期主族元素的最外层电子数之和为20。在周期表中甲与乙、丙、丁紧密相邻,甲、乙两元素的原子序数之和等于丙元素的原子序数。下列说法正确的是:
A.甲、乙、丙、丁四种元素中原子半径最小的是丁元素
B.甲、乙、丙、丁四种元素中可能有三种元素处在同一主族
C.甲、乙、丙、丁四种元素中一定有三种元素处在同一周期
D.甲、乙、丙、丁四种元素中非金属性最强元素是丁元素
11.著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土溶剂萃取体系方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法不正确的是:
A.电解熔融Ce02制Ce,铈在阴极获得
B.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑
C.用Ce(S04)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+=Ce3++2Fe3+
D.四种稳定的核素13658Ce、13858Ce、14058Ce、14258Ce,它们互称为同位素
10.时钟反应或振荡反应提供了迷人课堂演示实验,也是一个活跃的研究领域。测定含I-浓度很小的碘化物溶液时,利用振荡反应进行化学放大,以求出原溶液中碘离子的浓度。主要步骤是:①在中性溶液中,用溴将试样中I-氧化成IO3-,将过量的溴除去
②再加入过量的碘化钾,在酸性条件下,使IO3-完全转化成I2
③将②中生成的碘完全萃取后,用肼将其还原成I-,方程式为:H2N-NH2+2I2→4I-+N2↑+4H+
④将生成的I-萃取到水层后用①法处理。
⑤将④得到的溶液加入适量的KI溶液,并用硫酸酸化。
⑥将⑤反应后的溶液以淀粉作指示剂,用Na2S2O3标准溶液滴定,方程式为:
2Na2S2O3+I2→Na2S4O6+2NaI
经过上述放大后,则溶液中I-浓度放大为原溶液中I-浓度的(设放大前后体积相等):
A.2倍 B.4倍 C.6倍 D.36倍
9.下列图像是NaCl的晶体结构图像的是:
A: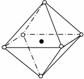 B:
B: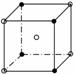 C:
C: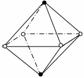 D:
D: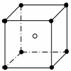
8.已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为Y kJ/mol,则1mol C与O2反应生成CO的反应热△H为:
A.-Y kJ/mol B.(0.5Y+5X) kJ/mol
C.-(5X-0.5Y) kJ/mol D.+(10X-Y) kJ/mol
7.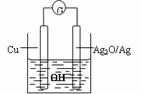 普通水泥在固化过程中自由水分子减少并产生OH-,溶液呈碱性。根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是:
普通水泥在固化过程中自由水分子减少并产生OH-,溶液呈碱性。根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是:
A.工业上以黏土、纯碱为主要原料来制造水泥
B.测量原理示意图中,Ag2O为负极
C.负极的电极反应式为:2Cu+2OH--2e-=Cu2O+H2O
D.电池工作时,OH-向正极移动
6.一定体积0.01mol/L的稀硝酸溶液恰好能氧化一定质量的铁、铝混合物,已知两种金属均被氧化为最高价态,还原产物只有NO。若用0.01mol/L的NaOH溶液溶解相同质量的该混合物,当反应完全时所需氢氧化钠溶液的体积是稀硝酸溶液的1/5,则样品中铁、铝的物质的量之比为:
A.2:3 B.1:3 C.1:4 D.5:3
5.下列实验操作会导致实验结果偏低的是:
①配制100g10%的CuSO4溶液,称取10gCuSO4晶体溶于90g水中
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮
③配制一定物质的量浓度溶液时,药品与砝码放反了,游码读数为0.2 g,所得溶液的浓度
④用酸式滴定管量取用98%,密度为1.84 g/cm3的浓H2SO4配制200mL 2 mol·L-1的稀H2SO4时,先平视后仰视
A.只有① B.只有② C.②③④ D.①③④
4.微观粒子是化学研究的主要对象,若NA代表阿伏加德罗常数的数值,下列对粒子数判断正确的是:
A.6.2g氧化钠和7.8g过氧化钠混合物中所含有的离子数为0.7NA
B.2.8g聚乙烯中含有的碳原子数为0.2NA
C.5.6g铁粉与硝酸溶液反应失去的电子数一定为0.3NA
D.标准状况下,22.4LCH4和CCl4的混合物所含有的分子数目为NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com