
题目列表(包括答案和解析)
1、据报道,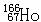 可有效地治疗肝癌,该原子核内的中子数与核外电子数之差为( )
可有效地治疗肝癌,该原子核内的中子数与核外电子数之差为( )
A.32 B.67 C.99 D.166
29.(10分)常温下用惰性电极电解200 mL 一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(以下气体体积已换算成标准状况下的体积),根据图中信息回答下列问题。

⑴通过计算推测:
①原混合溶液NaCl和CuSO4的物质的量浓度;
②t2时所得溶液的pH;
⑵若用惰性电极电解NaCl和CuSO4的混合溶液200mL,经过一段时间后两极均得到224mL气体,则原混合溶液中的氯离子浓度的取值范围为 ,铜离子浓度的取值范围为 。
28.已知稀溴水和氯化铁溶液都呈黄色,现在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液呈黄色。
(1)甲同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是:______ (填粒子的化学式,下同);乙同学认为这是发生化学反应所致,则使溶液呈黄色的微粒是_________;
(2)如果要验证乙同学判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
实验可供选用试剂:A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳
D.硫氰化钾溶液 E.硝酸银溶液 F.碘化钾淀粉溶液
|
实验方案 |
所选用试剂(填代号) |
实验现象 |
|
方案一 |
|
|
|
方案二 |
|
|
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,则首先被氧化的离子是______ ,相应的离子方程式为 ;
27.(10分)几种中学化学常见的单质及其化合物相互转化的关系图如下:
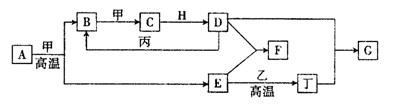
可供参考的信息有:
①甲、乙、丙、丁为单质,其余为化合物
②A由X和Y两种元素组成,其原子个数比为l︰2,元素质量之比为7︰8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为 ,每反应lmol的A转移的电子数为 mol;
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式: ;
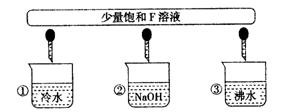 (3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。
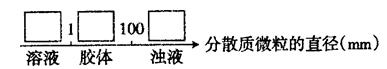 试将①、②、③填人下列方框中:
试将①、②、③填人下列方框中:
(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式: 。
26.(14分)向体积为2 L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应: 2X(g)  Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5min 后反应达到平衡 , 此时测得容器内的压强为起始时的1.2倍, 则用Y表示的速率为 mol/(L·min);
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲:v(X)=3.5 mol/(L·min); 乙:v(Y)=2 mol/(L·min);丙:v(Z)=4.5mol/(L·min);丁:v(X)=0.075 mol/(L·s)。若其它条件相同,温度不同,则温度由高到低的顺序是(填序号) ;
(3)若向达到(1)的平衡体系中充入氮气,则平衡向 (填"左"或"右"或"不)移动;若向达到(1)的平衡体系中移走部分混合气体,则平衡向 (填“左”或“右”或“不”)移动;
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体 , 则平衡后X 的转化率与(1)的平衡中X的转化率相比较:
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol, 达到平衡时仍与(1)的平衡等效,则a、b、c应该满足的关系为 ;
(6)若保持温度和体积不变,起始时加入X、Y、Z 物质的量分别为a mol、b mol、c mol, 达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为 。
25.某学生设计了如图的方法对A盐进行鉴定:
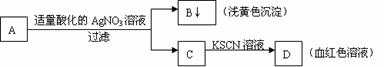
由此分析,下列结论中,正确的是
A.A中一定有Fe3+ B.B为AgI沉淀
C.C中一定有Fe3+ D.A一定为FeBr2溶液
第Ⅱ卷(非选择题,共50分)
24.根据下列实验现象,所得结论正确的是
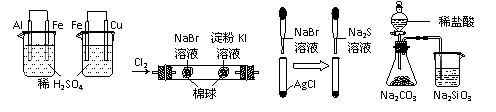 A
B
C
D
A
B
C
D
|
实验 |
实验现象 |
结论 |
|
A |
左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Fe>Cu |
|
B |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
|
C |
白色固体先变为淡黄色,后变为黑色 |
溶解性Ag2S>AgBr>AgCl |
|
D |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:Cl>C>Si |
23.a、b、c、d、e是同周期的五种元素, a的最高价氧化物对应水化物的碱性弱于b的; c的气态氢化物的还原性弱于d的;五种元素的原子得到或失去电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是
A、abdce B、baedc C、ebadc D、cdeab
22.多硫化钠Na2Sx(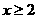 )在结构上与Na2O2, FeS2等有相似之处,Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的量之比为1:16,则x值是
)在结构上与Na2O2, FeS2等有相似之处,Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的量之比为1:16,则x值是
A.5 B.4 C.3 D.2
21.限用一种试剂,经过一次性实验就能鉴别Na2CO3、(NH4)2SO4、NH4Cl、KNO3溶液,应选用
A.AgNO3溶液 B.NaOH溶液 C.Ba(OH)2溶液 D.盐酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com