
题目列表(包括答案和解析)
7.联合国气候变化大会2009年12月7日在丹麦首都哥本哈根拉开帷幕,很多人称这次大会为“人类拯救地球的最后机会”。据报道,在火星和金星大气层中发现了一种非常特殊的会导致温室效应的气态化合物,它的结构式为:16O=C=18O。下列说法正确的是
A.16O与18O为同种核素
B.16O=C=18O与16O=C=16O互为同位素
C.16O=C=18O的化学性质与16O=C=16O完全不同
D.目前提出的“零碳经济”,不再向环境排放CO2,有利于控制温室效应
19. 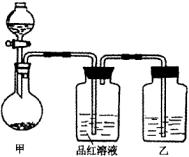 (14分)某同学在学习“硫酸及其盐的某些性质与用途中,进行如下实验探究。
[实验一]探究浓硫酸的氧化性
将实验室常用的药品放入如右图所示的实验装置后,加热装置甲。(夹持和加热装置省略)
(14分)某同学在学习“硫酸及其盐的某些性质与用途中,进行如下实验探究。
[实验一]探究浓硫酸的氧化性
将实验室常用的药品放入如右图所示的实验装置后,加热装置甲。(夹持和加热装置省略)
(1)该装置设计上存在明显缺陷,请指出: 。
反应开始前如何检查甲装置的气密性 。
(2)写出装置甲中反应的化学方程式: 。
[实验二]探究明矾晶体的某些性质成分与用途
(3)明矾可以净水的原因是 (用离子方程式表示):取少量明矾晶体配成溶液,置于洁净的试管中,检验明矾溶液中含有硫酸根离子的操作是 。
[实验三]用KHSO4制取H2O2并测其质量分数
查阅资料得知:工业上用电解KHSO4饱和溶液制取H2O2,示意图如下:
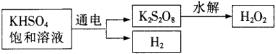
用此法制取一定浓度的H2O2,并进行下列实验测定H2O2的质量分数:(离子方程式:2MnO4―+5H2O2+6H+=2Mn2++8H2O+5O2↑)
①取5.00 mL H2O2溶液(密度为1.00 g/mL)置于锥形瓶中加水稀释,再加稀硫酸酸化;
②用0.1000 mol/L KMnO4溶液滴定;
③用同样方法滴定,三次消耗KMnO4溶液的体积分别为20.00 mL、19.98 mL、20.02 mL。
回答下列问题:
(4)电解饱和KHSO4溶液时,阳极的电极反应式为 。
(5)原H2O2溶液中溶质的质量分数为 。
18.(12分)A、B、C、D、E、F六种物质的转化关系如下图所示(条件及部分产物未标出)。
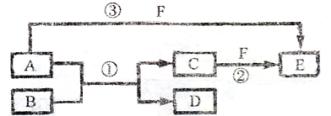 (1)若A、D、F都是非金属单质,常温下,A、D为固体,D单质可作为半导体材料,F为气体,且A、D所含元素为同主族短周期元素,A、F所含元素同周期,则反应①的化学方程式是
。
(1)若A、D、F都是非金属单质,常温下,A、D为固体,D单质可作为半导体材料,F为气体,且A、D所含元素为同主族短周期元素,A、F所含元素同周期,则反应①的化学方程式是
。
(2)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,C的溶液为浅绿色,则反应②(在水溶液中进行)的离子方程式是: 。
(3)若B、C、F都是气态单质,B有毒且呈黄绿色,反应③中有水生成, 反应②需要放电才能发生,A、D相遇有白烟生成,则反应③的化学方程式是
。
反应②需要放电才能发生,A、D相遇有白烟生成,则反应③的化学方程式是
。
(4)若A、B、D为有机物,B的相对分子质量比A大14,E、F为单质,F是短周期中原子半径最大的元素。C能与乙烯在一定条件下发生加成反应生成A。则反应③的化学方程式为 。写出D的结构简式 。A在铜做催化剂的作用下可以与O2 反应生成有机物甲,甲在一定条件下还可以反应生成B,欲检验甲中官能团,所选用的试剂为(填序号) 。
①NaOH溶液 ②新制氢氧化铜悬浊液 ③银氨溶液 ④高锰酸钾溶液 ⑤稀HNO3
17.(13分)从石油裂解中得到的1,3-丁二烯可进行以下多步反应,得到重要的合成橡胶和杀菌剂富马酸二甲酯。
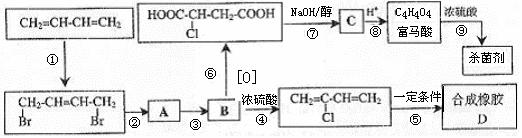
(1)写出D的结构简式
(2)写出B的结构简式
(3)以上反应中属于消去反应的是 (填入编号)
(4)写出第②步反应的化学方程式
(5)写出富马酸的一种同系物的结构简式
(6)写出第⑨步反应的化学方程式 。
16.(16分)某链烃A具有下列性质:取0.1molA充分燃烧,燃烧所得的CO2为13.44L,(标准状况);质谱分析显示,A物质的最大质荷比为84;已知A分子中所有的碳原子共平面,该分子的一氯取代物只有一种,回答下列问题:
(1)A的结构简式为 ;下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量相等的是(填序号) 。
a. C7H12O2 b. C7H12O c. C6H14O d. C7H14O3 (2)A与Br2的CCl4溶液反应生成B,B与NaOH的醇溶液共热可得到D,D分子中无溴原子。请写出由B制备D的化学反应方程式: 。
(3)B与足量NaOH水溶液完全反应,生成有机物E。
①E可能发生的反应类型有(填序号)
a.取代反应 b.消去反应 c. 加聚反应 d. 加成反应 e. 还原反应
② E与乙二醇的关系是(填序号)
a.同分异构体 b.同一物质 c.同系物 d.同素异形体
(4)E与乙二酸在一定条件下等物质的量反应生成分子式为C8H12O4的有机物,请写出该反应的化学方程式 。
(5)已知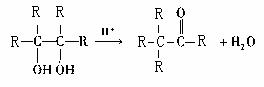 :(-R为烃基),请写出E在酸性条件下生成G的化学反应方程式:
。
:(-R为烃基),请写出E在酸性条件下生成G的化学反应方程式:
。
与G分子相同,能发生银镜反应,且结构中有两个甲基的异构体共有 种。
15.在一体积可变的密闭容器中,加入一定量的A、B,发生反应aA(g)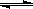 bB(g)
ΔH=Q kJ/mol。反应达到平衡时,B的物质的量浓度为1.00 mol·L-1。现将容器的容积扩大一倍,B的物质的量浓度变为0.60 mol·L-1;如保持容积不变只升高温度,则B浓度变1.20 mol·L-1,下列说法正确的是
bB(g)
ΔH=Q kJ/mol。反应达到平衡时,B的物质的量浓度为1.00 mol·L-1。现将容器的容积扩大一倍,B的物质的量浓度变为0.60 mol·L-1;如保持容积不变只升高温度,则B浓度变1.20 mol·L-1,下列说法正确的是
A. a>b B. Q<0 C.温度不变,压强增大,B的质量分数减少 D.体积不变,温度升高,平衡向逆反应方向移动
第二卷(非选择题,共55分)
14.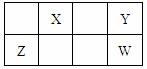 X、Y、Z、W四种短周期元素在周期表中相对位置如表所示,Y、Z质子数之和为21,下列说法中正确的是
X、Y、Z、W四种短周期元素在周期表中相对位置如表所示,Y、Z质子数之和为21,下列说法中正确的是
A.X、Y、Z、W均为非金属元素
B.X、Y、W的氢化物中,Y的氢化物沸点最高
C.Z、W的最高价氧化物都是酸性氧化物
D.W元素的原子半径大于Z元素的原子半径
13.下列浓度关系正确的是 A.pH=3的盐酸与pH=11的氨水等体积混合,混合溶液呈酸性
B.等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-)
C.在碳酸氢钠溶液中:C(H2CO3 )+ C(H+) =C(OH-) +C(CO32-)
D.Na2S溶液中:c(Na+)>c(S2-)>c(HS-)>c(OH-)>c(H+)
12. H是一种性能优异的高分子材料,其结构简式为 CH-CH-CH2-CH n已被
H是一种性能优异的高分子材料,其结构简式为 CH-CH-CH2-CH n已被
广泛应用于声、热、光的传感等方面。它是由HC≡CH、(CN)2、CH3COOH三种单体通过适宜的反应形成的。由H的结构式分析合成过程中发生反应的类型有 ①加成反应 ②取代反应 ③缩聚反应 ④加聚反应 ⑤酯化反应
A.①④ B.①④⑤ C.①②④ D.①②③
11.下列有关物质结构和同分异构体的说法错误的是
A. 分子式为C8H6O2的芳香族有机物(除苯环外不含其他环)中不可能有一个羧基
B.一溴代烷C5H11Br水解后的产物在红热铜丝催化作用下最多可被氧化成4种不同的醛
C.分子式为C5H10的烯烃共有(要考虑顺反异构体)6种
D.已知某氨基酸的相对分子质量小于210,且氧的质量分数约为0.5,则其分子中碳的个数最多为5个
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com