
题目列表(包括答案和解析)
30、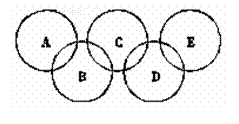 (16分)下图为“奥运五环”,如果五元环分别代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素;五种化合物由五种短周期元素形成,每种化合物仅含有两种元素。A是沼气的主要成分;B、E分子中所含电子数都为18,B不稳定,具有较强的氧化性;E是由六个原子构成的分子,可用于火箭燃料;C是由地壳中含量最高的两种元素组成;D中所含的两种元素的原子个数之比为3∶4。根据以上信息回答下列问题:
(16分)下图为“奥运五环”,如果五元环分别代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素;五种化合物由五种短周期元素形成,每种化合物仅含有两种元素。A是沼气的主要成分;B、E分子中所含电子数都为18,B不稳定,具有较强的氧化性;E是由六个原子构成的分子,可用于火箭燃料;C是由地壳中含量最高的两种元素组成;D中所含的两种元素的原子个数之比为3∶4。根据以上信息回答下列问题:
(1)A、B、C、D、E的化学式分别是
(2)。A燃烧的化学方程式为 。
(3)B的水溶液呈弱酸性,其电离方程式可表示为 ,
(4)B与E反应可生成单质G和一种常见的液体H,其反应的化学方程式为
。
23、镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为: 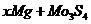
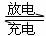
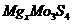 在镁原电池放电时,下列说法错误的是
在镁原电池放电时,下列说法错误的是
A.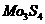 发生氧化反应
发生氧化反应
B.正极反应为: 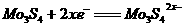
C.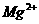 向负极迁移
向负极迁移
D.负极反应为: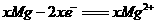
22、NA代表阿伏加德罗常数值,下列说法正确的是
A.0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA
B.常温常压下,48gO3含有的氧原子数为3NA
C.标准状况下,aL SO3所含分子个数为aNA/22.4
D.0.5mol Na2O2晶体中含有1.5NA个离子
12. 室温下,取0.3 mol·L-1HY溶液与0.3 mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH = 9,则下列说法(或关系式)正确的是
室温下,取0.3 mol·L-1HY溶液与0.3 mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH = 9,则下列说法(或关系式)正确的是
A.混合溶液中由水电离出的c(OH-)=10-9 mol·L-1
B.溶液中离子浓度由大到小的顺序为 c(Y-)> c(Na+) > c(OH-)>c(H+)
C.c(OH-)-c(HY)=c(H+)=1×10-9mol·L-1
D.c(Na+)=c(Y¯)+c(HY) =0.3 mol·L-1
11.右图是向MgCl2、AlCl3混合溶液中,开始滴加6 ml试剂A,之 后改滴试剂B,所得沉淀y mol与试剂体积V(ml)间的关系.以下结论不正确的是
A.A是盐酸,B是NaOH,且C(B)=2C(A)
B.原混合液中,C(Al3+)∶C(Mg2+)∶C(Cl-)=1∶1∶5
C.A是NaOH,B是盐酸,且C(NaOH)∶C(HCl)=2∶1
D.从6到9,相应离子反应式H++OH-= H2O
10.下列离子方程式正确的是B
A.碳酸氢钠溶液与少量石灰水反应:HCO3一+Ca2++OH一= CaCO3↓+H2O
B.氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH一 H2O+NH3↑
H2O+NH3↑
C.金属Na投入到CuSO4溶液中:2Na + Cu2+ = 2Na+ + Cu
 D.次氯酸钙溶液中通入少量SO2气体:Ca2++ ClO一+SO2+H2O=CaSO4↓+ HCl
D.次氯酸钙溶液中通入少量SO2气体:Ca2++ ClO一+SO2+H2O=CaSO4↓+ HCl
9.下列有关描述正确的是
A.只用淀粉溶液即可检验食盐是否为加碘盐
B.除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶
C.液氯罐泄漏时,可将其移入水塘中,并向水塘中加入生石灰
D.将60℃下澄清石灰水降温到常温,会出现浑浊
8.有A、B两种烃,含碳元素的质量分数相等,下列关于A和B的叙述正确的是
A.A和B一定是同分异构体
B.A和B可能是同系物
C.A和B分子式一定相同 www.
D.A和B各1 mol完全燃烧后生成的CO2的质量一定相等
7.去年,我国部分地区出现了50年一遇的严重雪灾,这给人民群众的出行制造了极大的麻烦。为防止路面积雪路滑,常在路面撒融雪剂使雪融化,融雪剂的成分有氯化钠、氯化钙、氯化镁等。下列说法正确的是
A.融雪剂的融雪原理主要是盐类溶解放热
B.融雪剂的融雪原理主要是盐类的水解
C.使用融雪剂融化的雪水会使多数植物生长茂盛
D.含有融雪剂的雪水在钢筋混凝土中可形成原电池,对这种结构的桥梁造成腐蚀
24.(10分)
⑴.在一定条件下,容积为 100 L密闭容器中发生反应:CH4(g)+H2O(g)
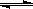 CO(g)+3H2(g);ΔH>0
CO(g)+3H2(g);ΔH>0
将1.0 mol CH4和2.0 mol H2O(g)通入该密闭容器 l0 min时有0.1 mol CO生成,则10 min内该反应的平均速率v(H2) 。
⑵.在压强为0.1 MPa条件下,容积为V L某密闭容器中a mol CO与
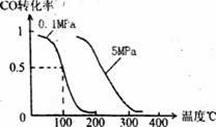
2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)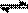 CH3OH(g);CO的转化率与温度、压强的关系如右图所示。
CH3OH(g);CO的转化率与温度、压强的关系如右图所示。
 ①该反应的△H 0
(填“<”、“>”或“=”)。
①该反应的△H 0
(填“<”、“>”或“=”)。
②100℃时该反应的平衡常数K= (用含a、V的代数式表示)。
③在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率 (填“增大”、“减小”或“不变”),平衡常数 (填“增大”、“减小”或“不变”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com