
题目列表(包括答案和解析)
19.下列叙述中正确的是 ( )
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1:2
C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出
18.有下列五个化学方程式(x、Y、Z均为正值):
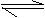 ①C2H2(g)+H2(g) C2H4(g)
①C2H2(g)+H2(g) C2H4(g)
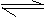 ②CH4(g) H2(g)+
②CH4(g) H2(g)+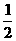 C2H4(g)
C2H4(g)
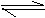 ③C(s)+2H2(g) CH4(g);△H= -X kJ·mol-1
③C(s)+2H2(g) CH4(g);△H= -X kJ·mol-1
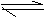 ④C(s)+
④C(s)+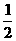 H2(g)
H2(g) 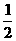 C2H2(g);△H= -Y kJ·mol-1
C2H2(g);△H= -Y kJ·mol-1
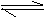 ⑤C(s)+H2(g)
⑤C(s)+H2(g) 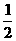 C2H4(g)△H= -ZkJ·mol-1
C2H4(g)△H= -ZkJ·mol-1
当温度下降时①式平衡向右移动,②式平衡向左移动。据此判定③-⑤式中关于X、Y、Z的大小顺序排列正确的是 ( )
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Z>X>Y
17.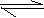 把氢氧化钙放入蒸馏水中,一定时间后达到如下平衡Ca(OH)2(s) Ca2++2OH-加入以下物质,可使Ca(OH)2(s)减少的是 ( )
把氢氧化钙放入蒸馏水中,一定时间后达到如下平衡Ca(OH)2(s) Ca2++2OH-加入以下物质,可使Ca(OH)2(s)减少的是 ( )
A.蒸馏水 B.A1C13溶液
C.NaOH溶液 D.CaCl2溶液
16.已知白磷(P4)与CuSO4溶液反应的化学方程式为:11P4+60CuSO4+96H2O
20Cu3P+24H3PO4+60H2SO4,则lmolCuSO4能氧化白磷的物质的量是 ( )
A.2/5mol B.1/5mol C.1 1/5mol D.1/20mol
15.同温同压下,两个等体积的干燥圆底烧瓶中分别充满①等物质的量空气和NH,的混合气,②NO2气体,分别进行喷泉实验,经充分反应后,两瓶内溶液的物质的量浓度关系为 ( )
A.①>② B.①<② C.①=② D.不能确定
14.下列反应的离子方程式书写不正确的是 ( )
A.4mol/L的NaAlO2溶液和7mol/L的HCl等体积均匀混合:
4A1O2-+7H++H2O 3AI(OH)3+AI3+ 电解
B.用石墨电极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2↑+4H+
C.将0.1mol/L 25mL盐酸逐滴缓缓滴入0.1mol/L 25mLNa2CO3溶液中,并不断搅拌:2H++CO32-===CO2↑+H2O
D.硫酸氢钠溶液与足量氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4+H2O
13.在密闭容器中充入CO2和CO的混合气体,其密度是相同条件下氦气密度的8倍,这时测得容器内的压强为P1。若控制容器的体积不变,加入足量的Na2O2,充分振荡并不断用电火花点燃至反应完全,恢复到开始时的温度,再次测得容器内的压强为P2。则P1和P2之间的关系是 ( )
A.P1=8P2 B.P1=4P2 C.P1=2P2 D.P1=P2
12.在xR2++yH++O2=mR3++2H2O的离子方程式中,对m和R3+的判断正确的是 ( )
A.m=4;R3+是氧化产物 B.m=2y;R3+是氧化产物
C.m=2 R3+是还原产物 D.m=y/2;R3+是还原产物
11.将3.72g由金属钠、氧化钠和过氧化钠组成的混合物与足量水反应,在标准状况下得到672mL混合气体。将该混合气体用电火花点燃,恰好完全反应,则原混合物中钠、氧化钠、过氧化钠的物质的量之比为 ( )
A.3:2:1 B.4:2:1 C.1:1:l D.2:l:l
10.某混合气体,可能含有N2、HCl、CO,把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体体积都没有变化,再通过足量的Na2O2固体,气体体积减小,最后通过灼热的铜网,经充分反应后,气体体积又减小,但还有剩余气体,以下对混合气体组成的判断正确的是 ( )
A.一定没有N2,CO和HCl中至少有一种-
B.一定有N2、HCl、CO
C.一定有N2,CO和HC1中至少有一种
D.一定有N2和HCl,没有CO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com