
题目列表(包括答案和解析)
57.
 答案:
答案:
 (1)反应物能量 生成物能量
(1)反应物能量 生成物能量
 (2)无 降低 因为催化剂改变了反应的历程使活化能E降低
(2)无 降低 因为催化剂改变了反应的历程使活化能E降低
 (3)-198
(3)-198
 (4) SO2
+V2O5=SO3+2VO2 4VO2+ O2=2V2O5 (4)0.025 0.05
(4) SO2
+V2O5=SO3+2VO2 4VO2+ O2=2V2O5 (4)0.025 0.05

 (5) S(s)+O2(g) =2SO2(g)△H1=-296
KJ·mol-1 , SO2(g)+1/2O2(g) =SO3(g) △H2=-99 KJ·mol-1
(5) S(s)+O2(g) =2SO2(g)△H1=-296
KJ·mol-1 , SO2(g)+1/2O2(g) =SO3(g) △H2=-99 KJ·mol-1

 3 S(s)+9/2O2(g)=3SO3(g) △H=3(△H1+△H2)=-1185
KJ·mol-1
3 S(s)+9/2O2(g)=3SO3(g) △H=3(△H1+△H2)=-1185
KJ·mol-1


 解析:
解析:





 (1)本小题考查反应物总能量高于生成物总能量为放热反应,可得到A和C所表示的意义,E为活化能与反应热无关,但是用催化剂可以降低活化能;
(1)本小题考查反应物总能量高于生成物总能量为放热反应,可得到A和C所表示的意义,E为活化能与反应热无关,但是用催化剂可以降低活化能;
 (2)图中表示的是2molSO2的反应,因此△H=-99×2KJ·mol-1;
(2)图中表示的是2molSO2的反应,因此△H=-99×2KJ·mol-1;
 (3)依题意即可写出:SO2 +V2O5=SO3+2VO2 4VO2+ O2=2V2O5;
(3)依题意即可写出:SO2 +V2O5=SO3+2VO2 4VO2+ O2=2V2O5;
 (4)依据速率之比等于化学计量数之比
(4)依据速率之比等于化学计量数之比
56. 答案:
答案:






 (1)a d
(1)a d

 (2)② ③ ④
(2)② ③ ④

 (3)品红溶液褪色;瓶壁有淡黄色粉末和无色的小液滴
(3)品红溶液褪色;瓶壁有淡黄色粉末和无色的小液滴

 (4)
(4) 变大
变大

 (5)b
(5)b

 (6)S H2O
(6)S H2O
 解析:(1)若用启普发生器制取气体,所选试剂应为块状固体和液体,且反应不需要加热,故a、d正确,c错误。硝酸具有强氧化性,与硫化亚铁反应得不到H2S,b项错。
解析:(1)若用启普发生器制取气体,所选试剂应为块状固体和液体,且反应不需要加热,故a、d正确,c错误。硝酸具有强氧化性,与硫化亚铁反应得不到H2S,b项错。
 (2)要控制硫化氢气体产生速率必须选用分液漏斗。
(2)要控制硫化氢气体产生速率必须选用分液漏斗。
 (3)开始氧气充足,H2S燃烧生成SO2和H2O,后来氧气不足,燃烧产物为S和H2O,描述反应现象要从SO2、S和H2O三个方面考虑。
(3)开始氧气充足,H2S燃烧生成SO2和H2O,后来氧气不足,燃烧产物为S和H2O,描述反应现象要从SO2、S和H2O三个方面考虑。
 (5)a中增加的装置起不到任何作用。b装置可将启普发生器内的H2S与点燃的H2S分隔开,能防止爆炸。c、d装置中生成的H2S无法排出,故错误。
(5)a中增加的装置起不到任何作用。b装置可将启普发生器内的H2S与点燃的H2S分隔开,能防止爆炸。c、d装置中生成的H2S无法排出,故错误。
 (6)当硫化氢在空气中的体积分数为30%时,O2在混合气体中的体积分数为70%×
(6)当硫化氢在空气中的体积分数为30%时,O2在混合气体中的体积分数为70%× =14%,O2不足,发生反应2H2S+O2
=14%,O2不足,发生反应2H2S+O2 2S+2H2O。
2S+2H2O。
55.
 答案:Ⅰ.(1)容量瓶
答案:Ⅰ.(1)容量瓶

 (2)2 5 6 2 8 502
(2)2 5 6 2 8 502

 (3)酸式
(3)酸式

 滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色
滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色

 (4)
(4)

 (5)偏高
(5)偏高

 解析:1)仪器的选用根据题意应该选用容量瓶。(2)残缺方程式配平首先确定缺什么,分析可知缺的是02,根据电子转移守恒,配平化学方程式。
解析:1)仪器的选用根据题意应该选用容量瓶。(2)残缺方程式配平首先确定缺什么,分析可知缺的是02,根据电子转移守恒,配平化学方程式。


 (3)由于高锰酸钾标准溶液具有强氧化性,所以只能使用酸式滴定管。滴定到达终点的现象是:滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色。(4)根据配平的化学方程式计算出过氧化氢的量,最后计算出原过氧化氢溶液中过氧化氢的质量分数为
(3)由于高锰酸钾标准溶液具有强氧化性,所以只能使用酸式滴定管。滴定到达终点的现象是:滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色。(4)根据配平的化学方程式计算出过氧化氢的量,最后计算出原过氧化氢溶液中过氧化氢的质量分数为 。(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高。
。(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,有一部分溶液占据了气泡的体积,并没有滴入锥形瓶,则测定结果偏高。

 答案Ⅱ.(各1分,共4分)
答案Ⅱ.(各1分,共4分)
|
实验内容 |
实验方法 |
实验现象 |
|
验证氧化性 |
取适量饱和硫化氢溶液于试管中,滴入  过氧化氢溶液。 过氧化氢溶液。  (取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液。) (取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液。) |
产生淡黄色沉淀或溶液变浑浊。  (溶液变蓝色。) (溶液变蓝色。) |
|
验证不稳定性 |
取适量过氧化氢溶液于试管中,加热,  用带火星的木条检验。 用带火星的木条检验。  (取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中。) (取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中。) |
产生气泡,木条复燃。  (溶液变浑浊或有浅黄色沉淀产生) (溶液变浑浊或有浅黄色沉淀产生) |

 解析:(1)验证氧化性,选用具有还原性的饱和硫化氢溶液,产生淡黄色沉淀硫或溶液变浑浊;或者选用有还原性的碘化钾淀粉溶液,有碘单质生成,溶液变蓝色。(2)验证不稳定性,取适量过氧化氢溶液于试管中,加热,用带火星的木条检验有氧气生成;或者取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中,溶液变浑浊或有浅黄色沉淀产生。
解析:(1)验证氧化性,选用具有还原性的饱和硫化氢溶液,产生淡黄色沉淀硫或溶液变浑浊;或者选用有还原性的碘化钾淀粉溶液,有碘单质生成,溶液变蓝色。(2)验证不稳定性,取适量过氧化氢溶液于试管中,加热,用带火星的木条检验有氧气生成;或者取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中,溶液变浑浊或有浅黄色沉淀产生。
54. 答案:
答案:





 C 浓硫硫和木炭 产生反应物
C 浓硫硫和木炭 产生反应物
 B 无水硫酸铜 检验是否有水
B 无水硫酸铜 检验是否有水
 A 品红
检验SO2
A 品红
检验SO2
 A 酸性KMnO4 除去SO2
A 酸性KMnO4 除去SO2
 A 澄清石灰水 检验CO2的存在。
A 澄清石灰水 检验CO2的存在。
 解析:
解析: 成套装置包括反应装置,检验装置和尾气处理装置。C中加入浓硫硫和木炭作为反应物的发生器,产物中必须先检验水,因为在检验其他物质时会在其它试剂中混入水,可选用装置B,放入无水硫酸铜,若变蓝则说明有水。接着检验SO2气体,用装置A,放入品红检验,若品红褪色,则说明有SO2气体产生,再用装置A,放入酸性KMnO4溶液以除去SO2,最后再用装置A,放入澄清石灰水来检验CO2的存在,因SO2也可以使澄清石灰水变浑,故先要除去SO2。
成套装置包括反应装置,检验装置和尾气处理装置。C中加入浓硫硫和木炭作为反应物的发生器,产物中必须先检验水,因为在检验其他物质时会在其它试剂中混入水,可选用装置B,放入无水硫酸铜,若变蓝则说明有水。接着检验SO2气体,用装置A,放入品红检验,若品红褪色,则说明有SO2气体产生,再用装置A,放入酸性KMnO4溶液以除去SO2,最后再用装置A,放入澄清石灰水来检验CO2的存在,因SO2也可以使澄清石灰水变浑,故先要除去SO2。
53. 答案:(1)H2O、H+、SO42-中的某一种粒子能够使CuO溶解
答案:(1)H2O、H+、SO42-中的某一种粒子能够使CuO溶解
 (2)水不能使氧化铜溶解,而是另外的H+、SO42-两种粒子中的一种粒子使CuO溶解
(2)水不能使氧化铜溶解,而是另外的H+、SO42-两种粒子中的一种粒子使CuO溶解
 (3)Na2SO4(或K2SO4等),稀硫酸
(3)Na2SO4(或K2SO4等),稀硫酸
 (4)氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O,SO42-两种粒子都不能使CuO溶解
(4)氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O,SO42-两种粒子都不能使CuO溶解
 (5)硝酸或盐酸等
(5)硝酸或盐酸等
 解析:(3)在Ⅱ中加入稀硫酸后氧化铜溶解,还不能确定是H+或SO42-中的某一种粒子能够使CuO溶解,可再加入SO42-验证。
解析:(3)在Ⅱ中加入稀硫酸后氧化铜溶解,还不能确定是H+或SO42-中的某一种粒子能够使CuO溶解,可再加入SO42-验证。
52. 答案:(1)bc
答案:(1)bc
 (2)b
(2)b
 (3)消耗的O2物质的量:
(3)消耗的O2物质的量:
 生成的SO3物质的量:
生成的SO3物质的量:
 SO2和SO3的物质的量和:
SO2和SO3的物质的量和:
 反应前的SO2物质的量:
反应前的SO2物质的量: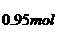
 SO2的转化率:
SO2的转化率: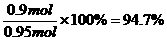
 (4)在给定的条件下,溶液呈强酸性,BaSO3不会沉淀。因此BaSO4的质量
(4)在给定的条件下,溶液呈强酸性,BaSO3不会沉淀。因此BaSO4的质量
 解析:化学平衡是动态平衡,处于平衡状态的化学反应,并没有停止反应,化学平衡状态的“定”,指的是平衡状态时反应物中各组分的质量分数、物质的量、物质的量分数、总压强、浓度等保持不变,而平衡时的上述各种量的比较关系取决于多种条件,不一定是相等的。且平衡状态的正逆反应速率一定相同。向装置中再充入N2和改变反应的催化剂,不能使化学平衡移动,升高温度使化学平衡移动逆向移动,
解析:化学平衡是动态平衡,处于平衡状态的化学反应,并没有停止反应,化学平衡状态的“定”,指的是平衡状态时反应物中各组分的质量分数、物质的量、物质的量分数、总压强、浓度等保持不变,而平衡时的上述各种量的比较关系取决于多种条件,不一定是相等的。且平衡状态的正逆反应速率一定相同。向装置中再充入N2和改变反应的催化剂,不能使化学平衡移动,升高温度使化学平衡移动逆向移动,
 消耗的O2物质的量:
消耗的O2物质的量: 。
。
 生成的SO3物质的量:
生成的SO3物质的量:
 SO2和SO3的物质的量和:
SO2和SO3的物质的量和:
 反应前的SO2物质的量:
反应前的SO2物质的量: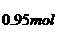
 SO2的转化率:
SO2的转化率: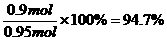
 在给定的条件下,溶液呈强酸性,BaSO3不会沉淀。因此BaSO4的质量
在给定的条件下,溶液呈强酸性,BaSO3不会沉淀。因此BaSO4的质量
51. 答案:
答案:





 (1)H2+S
(1)H2+S H2S(写成可逆反应也正确)。
H2S(写成可逆反应也正确)。
 (2)H2SO3 + 2H2S
(2)H2SO3 + 2H2S 3S + 3H2O
3S + 3H2O
 (3)C+2H2SO4(浓)
(3)C+2H2SO4(浓) CO2 ↑+2SO2 ↑+2H2O或Cu+2H2SO4(浓)
CO2 ↑+2SO2 ↑+2H2O或Cu+2H2SO4(浓) CuSO4 +SO2 ↑+2H2O
CuSO4 +SO2 ↑+2H2O
 (4)①H2SO3 +2OH-
(4)①H2SO3 +2OH- SO32-+2H2O ②大于;Na2SO3溶液中SO32-发生水解使溶液显碱性。③增大;升高温度促进Na2SO3溶液的水解。
SO32-+2H2O ②大于;Na2SO3溶液中SO32-发生水解使溶液显碱性。③增大;升高温度促进Na2SO3溶液的水解。
 解析:固态单质A能与空气中的氧气反应生成气体物质B,则A可能为C或S等,假定为S,则B为SO2,C为SO3,它们的相对分子质量为64∶80=4∶5,恰好与题意相符(同时也证明A不是C),则D为H2SO4,它是一种重要的工业原料,与题意也相符,进一步证明A为S。E为H2SO3。
解析:固态单质A能与空气中的氧气反应生成气体物质B,则A可能为C或S等,假定为S,则B为SO2,C为SO3,它们的相对分子质量为64∶80=4∶5,恰好与题意相符(同时也证明A不是C),则D为H2SO4,它是一种重要的工业原料,与题意也相符,进一步证明A为S。E为H2SO3。
50. 答案(1)支管口有白雾,试管中出现绿色,品红试纸褪色,铜片部分溶解。
答案(1)支管口有白雾,试管中出现绿色,品红试纸褪色,铜片部分溶解。
 (2)收集多余的SO2气体,防止污染空气;
(2)收集多余的SO2气体,防止污染空气;
 (3)在反应后的试管中、塑料袋中加适量的碱吸收SO2气体
(3)在反应后的试管中、塑料袋中加适量的碱吸收SO2气体
 SO2+2OH-
SO2+2OH- H2O+SO32-或SO2+OH-
H2O+SO32-或SO2+OH- HSO3-
HSO3-
 解析:当铜片接触热浓硫酸时,有大量的白雾产生(白雾是由于二氧化硫气体与水结合形成亚硫酸小液滴缘故)并沿支管口喷在品红试纸上,使品红试纸的红色开始褪色,而且原来无色硫酸溶液开始变绿,当品红试纸完全褪成白色后,把铜片向上提使其离开浓硫酸溶液,反应马上停止。
解析:当铜片接触热浓硫酸时,有大量的白雾产生(白雾是由于二氧化硫气体与水结合形成亚硫酸小液滴缘故)并沿支管口喷在品红试纸上,使品红试纸的红色开始褪色,而且原来无色硫酸溶液开始变绿,当品红试纸完全褪成白色后,把铜片向上提使其离开浓硫酸溶液,反应马上停止。
49. 答案:
答案:








 (1)
(1)
 (2)④ ② ① ③
(2)④ ② ① ③
 (3)验证
(3)验证 的存在 充分吸收
的存在 充分吸收 验证
验证 是否已被吸收完全
是否已被吸收完全
 (4)无水硫酸铜 水 由于产物通过①③时会带出水蒸气,所以②必须放在①、③之前
(4)无水硫酸铜 水 由于产物通过①③时会带出水蒸气,所以②必须放在①、③之前
 (5)澄清的石灰水
(5)澄清的石灰水 
 解析:上述反应中的生成物有三个:SO2、CO2、H2O,在检验这三种产物时要避免相互干扰,如检验CO2时一般用澄清石灰水,而SO2也会使澄清的石灰水变浑浊,所以在检验CO2之前必须先除去SO2;同时,在气体通过水溶液后,水蒸气会随之带出,所以必须在通过水溶液之前检验水的存在,由上分析装置的连接顺序是4→2→1→3
解析:上述反应中的生成物有三个:SO2、CO2、H2O,在检验这三种产物时要避免相互干扰,如检验CO2时一般用澄清石灰水,而SO2也会使澄清的石灰水变浑浊,所以在检验CO2之前必须先除去SO2;同时,在气体通过水溶液后,水蒸气会随之带出,所以必须在通过水溶液之前检验水的存在,由上分析装置的连接顺序是4→2→1→3
48. 答案:(1)SO2 +2OH-=SO32-+H2O (2)红色褪去 溶液又恢复红色 氧化
答案:(1)SO2 +2OH-=SO32-+H2O (2)红色褪去 溶液又恢复红色 氧化
 (3)吸收有害气体,防止污染空气
(3)吸收有害气体,防止污染空气
 NaHCO3+SO2=NaHSO3+CO2 (或2NaHCO3+SO2=Na2SO3+2CO2↑+H2O)
NaHCO3+SO2=NaHSO3+CO2 (或2NaHCO3+SO2=Na2SO3+2CO2↑+H2O)
 解析:Cu丝与浓H2SO4在加热条件下生成SO2气体,通入品红溶液,SO2有漂白性,使品红溶液褪色,加热恢复红色;过量的SO2气体,通入H2S溶液中,发生反应:2H2S+SO2
解析:Cu丝与浓H2SO4在加热条件下生成SO2气体,通入品红溶液,SO2有漂白性,使品红溶液褪色,加热恢复红色;过量的SO2气体,通入H2S溶液中,发生反应:2H2S+SO2 2H2O+3S↓,SO2是氧化剂,为防止过量的SO2逸出污染空气,用NaOH溶液吸收,如用NaHCO3溶液代替NaOH也可以,因NaHCO3溶液能与SO2反应。
2H2O+3S↓,SO2是氧化剂,为防止过量的SO2逸出污染空气,用NaOH溶液吸收,如用NaHCO3溶液代替NaOH也可以,因NaHCO3溶液能与SO2反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com