
题目列表(包括答案和解析)
4.(姜堰市罗塘中学2009-2010学年第一学期期中考试高三化学试题)硅和氮均是自然界含量丰富的元素,其单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用。
试回答下列问题:
⑴向大气中排放NOx可能导致的环境问题有 ▲ (答两点)。已知,足量NaOH溶液能完全吸收NO2生成氮的含氧酸盐,试写出该反应的离子方程式:
▲ 。
⑵光导纤维的使用,让人们的生活更加丰富精彩。 ▲ 是制备光导纤维的基本原料。
⑶氮化硅陶瓷是一种新型无机非金属材料,其化学式为 ▲ ,可由硅粉(用Al2O3和Y2O3作助剂)在氮气中高温烧结而成。由于使用的硅粉表面含二氧化硅,在反应中需加入碳粉。在烧结过程中,二氧化硅、碳、氮气以物质的量之比3:6:2反应生成两种化合物,该反应的化学方程式为 ▲ 。
⑷硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源。与“氢能源”比较,“硅能源”具有 ▲ 等更加优越的特点,从而得到全球的关注和期待。
(5)三硅酸镁(2MgO·3SiO2·nH2O)被用来治疗胃溃疡,是因为该物质不溶于水,服用后能中和胃酸,作用持久。写出三硅酸镁与胃酸(盐酸)反应的化学方程式: ▲ 。
(1)酸雨、光化学烟雾、臭氧层破坏(2分,只要答出任意两点,答出一点给一分),
2NO2+2OH- = NO3-+NO2-+H2O(2分)
3.甲、乙、丙、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)
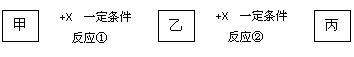


试回答下列问题:
(1)若X是强氧化性单质,则甲可能是 ▲ 。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向丙的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀。则乙的化学式为 ▲ ;丙溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示) ▲ 。
检验此丙溶液中金属元素价态的操作方法是 ▲ 。
(3)若甲、乙、丙为含有金属元素的无机化合物,X为强电解质,甲溶液与丙溶液反应生成乙;反应①的离子方程式为 ▲ ,
或 ▲ 。
(1)abc (2分)
(2)FeCl3(2分) Fe3+ + Fe = 3Fe2+,防止Fe2+被氧化(2分)。
用试管取少量丙溶液,滴加KSCN溶液,无颜色变化,再滴加氯水(或硝酸),溶液呈血红色,证明原溶液中有Fe2+存在。(答出要点得分)(2分);
(3)Al3+ + 3OH- = Al(OH)3↓(2分), AlO2- + H+ +H2O = Al(OH)3↓(2分)
(其他正确答案可参照本标准给分)
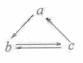
2.(姜堰市罗塘中学2009-2010学年第一学期期中考试高三化学试题)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
|
a |
b |
c |
|
A |
Al |
AlCl3 |
 Al(OH)3 Al(OH)3 |
|
B |
NO |
NO2 |
HNO3 |
|
C |
Si |
SiO2 |
H2SiO3 |
|
D |
H2SO4 |
SO2 |
SO3 |
1.(姜堰市罗塘中学2009-2010学年第一学期期中考试高三化学试题)下列叙述正确的是
A.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
B.Na2O2与水反应,红热的Fe与水蒸气反应均能生成气体
C.Li、C、P分别在足量氧气中燃烧均生成一种相应氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
10.(江苏省江浦高级中学高三化学2010第一轮复习模块检测)2000年在河南发现世界级特大金红石(含TiO2)矿床。钛和钛合金及其重要化合物,在许多领域具有广泛、重要的应用,被称为2l世纪的金属。
(1)钛元素的同位素有:2246Ti;2247Ti;2248Ti;2249Ti;2250Ti,则下列说法正确的是
A.据此可知中子数可能为30 B.据此可算出钛元素的相对原子质量为48
C.钛元素在元素周期表中位于第四周期 D.钛与铁(26Fe)同为第Ⅷ族元素
(2) 钛原子电子排布式为:
(3)TiO2 (二氧化钛)是高级的白色颜料,它可用下列反应制得:
第一步:FeTiO3+2H2SO4═TiOSO4+FeS04+2H20第二步:TiOSO4+2H2O═TiO2·H2O+H2SO4-Q(Q>0)
制氧化钛的关键是第二步反应。根据平衡移动原理,为使第二步反应能够顺利进行。应采用
等措施。
(1)C (2)略
(3)加热,加水,加碱
9.(江苏省黄桥中学2010届高三期中考试(化学))根据下列短周期元素性质的数据判断,下列说法正确的是
 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径/10-10 m |
0.66 |
1.36 |
1.23 |
1.10 |
0.99 |
1.54 |
0.70 |
1.18 |
|
最高或最低化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
-2 |
|
|
-3 |
-1 |
|
-3 |
|
A.元素①⑧形成的化合物具有两性 B.元素⑦位于第二周期Ⅴ族
C.元素④⑤形成的化合物是离子化合物 D.元素③的最高价氧化物对应水化物碱性最强
8.(江苏省高淳中学2010届高三上学期调研(化学))下列粒子的结构示意图中,表示硫原子的是
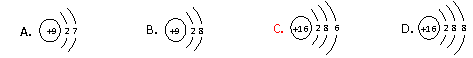
7.(江苏省高淳中学2010届高三上学期调研(化学))放射性的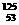 I对治疗肿瘤有一定疗效。该原子的原子核内的中子数是
I对治疗肿瘤有一定疗效。该原子的原子核内的中子数是
|
A.19 |
B.53 |
C. 72 |
D.125 |
6.(江苏省高淳中学2010届高三上学期调研(化学))海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)工业上从海水提溴的过程中涉及下列反应:Cl2 + 2NaBr = Br2 + 2NaCl。在该反应中,作为氧化剂的物质是 (填化学式);若反应中生成了1 mol Br2,则需消耗 mol NaBr。
(2)在光照条件下,氯气和氢气反应过程如下:
①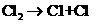 ②
②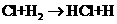 ③
③ ……
……
反应②中形成的化合物的电子式为 ;
反应③中被破坏的化学键属于 键(填“极性”或“非极性”)。
(3)在同周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是 (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第 周期 族。
(4)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是 。
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的稳定性按HF、HCl、HBr、HI的顺序依次减弱
c.卤素单质与氢气化合按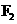 、
、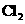 、
、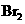 、
、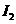 的顺序由难变易
的顺序由难变易
(1)Cl2 …………………………………………………………………1分
2 ……………………………………………………………………1分
(2) ……………………………………………………………1分
……………………………………………………………1分
非极性 ……………………………………………………………………1分
(3)S>Cl ……………………………………………………………1分
三 ……………………………………………………………………1分
IA ……………………………………………………………………1分
(4)a b ……………………………………………………………………1分
5.(江苏省赣榆一中2010届高三12月阶段考试化学)原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数为2n2-1.下列有关X的说法中不正确的是
A.X最高价氧化物对应的水化物可能显碱性
B.X可能形成化学式为KXO2的钾盐
C.X原子的最外层电子数和核电荷数肯定为奇数
D.X能与某些金属元素形成离子化合物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com