
题目列表(包括答案和解析)
14.(江苏省赣榆一中2010届高三12月阶段考试化学)下图所示各物质是由 1 一 20 号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出。已知 C 、 H 是无色有刺激性气味的气体, D 是一种黄绿色的气体单质,物质 J 可用于饮水消毒。反应 ② 和 ④ 是化工生产中的重要反应,反应 ⑤ 是实验室制备气体 C 的重要方法。

请回答下列问题:
( l )物质 E 的电子式是 ;物质 J 的名称为 。
( 2 )反应④的化学方程式为
反应 ⑤ 的化学方程式为
( 3)物质 A 由三种元素组成, 1 molA 与水反应可生成 1 molB 和 2 molC , A的化学式为
(1) 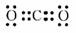 次氯酸钙
次氯酸钙
(2)2 Cl2+ 2Ca (OH )2=== Ca ( ClO )2+ CaCl2+H2O
Ca (OH )2+ 2NH4Cl2 ===CaCl2+ 2NH3↑+2H2O
( 3 ) CaCN2
13.(江苏金陵中学高三年级期中考试题--化学)下列现象或事实可有同一原理解释的是A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.氯水和活性炭使红墨水褪色
C.漂白粉和水玻璃长期暴露在空气中变质
D. 乙炔和乙烯使溴的四氯化碳溶液褪色
12.(江苏金陵中学高三年级期中考试题--化学)下列反应中会有沉淀产生的是 A.将二氧化硫气体通入酸性HMnO4溶液中
B.将二氧化硫气体通入碘水中
C.将二氧化硫气体通入BaCl2溶液中
D.将少量二氧化硫气体通入Ba(OH)2溶液中
11.(江苏金陵中学高三年级期中考试题--化学)下列物质能通过化合反应直接制得的是:①FeCl2 ②H2SO4 ③NH4NO3 ④HCl ( )
A.只有①②③ B.只有②③ C.只有①③④ D.全部
10.(江苏金陵中学高三年级期中考试题--化学)A为甲、乙两种短周期元素组成的化合物,其摩尔质量为100g·mol-1,甲元素的原子最外层电子数与K层电子数相等,E在通常状况下为气体,其水溶液显碱性,K为乙元素的单质。C为单质,其原子在周期表中半径最小。D为气体,对空气的相对密度为1.103。在适当条件下,它们相互之间有如下图所示的转化关系:

试填写下列空白:
(1)甲元素的单质在空气中燃烧除得到A外,还可得到 ,物质F的电子式为 。
(2)反应“E+D→G+B”的化学方程式为 。它是
工业中的重要反应之一。
(3)C和D在一定条件下还能形成另一种化合物I,I是 (填“极性”或“非极性”)分子,它能与一种弱酸反应生成强酸,该反应的离子方程式为 。
9.(如皋市2010届高三综合测试)下列现象或反应的原理解释正确的是 ( D )

8.(如皋市2010届高三综合测试)已知稀溴水和稀氯化铁溶液都呈黄色,若在足量的稀氯化亚铁溶液中,加入1-2 滴液溴,振荡后溶液呈黄色,现对溶液呈黄色的原因进行探究。
(1)仅限选用的仪器和试剂有:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙;酸性高锰酸钾溶液、氢氧化钠溶液、四氯化碳、硫氰化钾溶液、硝酸银溶液、淀粉碘化钾溶液,完成以下实验探究过程:
[提出假设]
假设①:溶液呈黄色不是发生化学反应所致,是溶液中 引起的(填微粒的化学式,下同)。
假设②:溶液呈黄色是发生化学反应所致,是溶液中 引起的。
[设计实验方案]
为了验证上述假设①和假设②的推断,请用简要的文字说明你的实验方案:
假设①方案: 。
假设②方案: 。
(2)根据高中所学的知识判断,你认为 (填“假设①”或“假设②”)的推断是正确的;若选用淀粉碘化钾溶液验证你的假设是否可行? (填“可行”或“不可行”),理由是_______________________________ 。
(3)若向稀溴化亚铁溶液中通入过量氯气,反应的离子方程式为:
。
(1)①Br2;②Fe3+ (每空2分,共4分)
假设①方案:向黄色溶液加入CCl4,振荡,静置,下层溶液呈橙红色。(2分)
假设②方案:向黄色溶液滴加KSCN溶液,溶液变为(血)红色 (2分)
(2)假设② (1分);不可行(1分);因为Br2和Fe3+都能把Iˉ氧化成I2使溶液都变蓝,无法得出结论。(2分)
(3)2 Fe2+ + 4 Brˉ + 3Cl2 == 2 Fe3+ +2 Br2 + 6Clˉ (2分)
7.(江苏省丹阳高级中学2010届高三上学期期中考试(化学))A、B、C、D是中学常见的纯净物,它们之间的转化关系如图所示:

(1).若A是由短周期中原子半径最大的元素构成的单质;D由短周期元素组成,既可溶于NaOH溶液又可溶于盐酸,则D的化学式为 。
(2).若A常温下为红棕色气体,B是含氧酸盐,D不溶于盐酸,则D的化学式为 ;将等物质的量的C与A通入NaOH溶液无气体剩余,写出该反应的离子方程式: 。
(3).若C是元素M的气态氢化物,且C能与M的最高价氧化物的水化物反应生成盐E;B是一种正盐,与E含有相同的阳离子;D不溶于稀硝酸。A与B反应的离子方程式是 。
(1)Al(OH)3 (2)H2SiO3(或H4SiO4) NO+NO2+2OH - =2NO2- + H2O
(3)Ba2++2OH-+2NH4++SO42-=BaSO4↓+2NH3↑+2H2O
6.(江苏省丹阳高级中学2010届高三上学期期中考试(化学))以下物质间的每步转化,存在不能通过一步反应实现的是 ( )
A.S→SO2→H2SO4→MgSO4 B.Fe→FeCl2→Fe(OH)2→Fe(OH)3
C.Al→Al2O3→Al(OH)3→NaAlO2 D.N2→NO→NO2→HNO3
5.(姜堰市罗塘中学2009-2010学年第一学期期中考试高三化学试题)已知稀溴水和氯化铁溶液都呈黄色,某化学活动小组进行实验探究。
李强、王刚两同学分别在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液呈黄色。
(1)李强同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是: ▲ (填粒子的化学式);王刚同学则认为这是发生化学反应所致,试写出对应的离子方程式: ▲ 。
(2)如果要验证王刚同学判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
实验可供选用试剂: A.碘化钾淀粉溶液 B.氢氧化钠溶液 C.硝酸银溶液
D.硫氰化钾溶液 E.四氯化碳 F.酸性高锰酸钾溶液
|
实验方案 |
所选用试剂(填代号) |
实验现象 |
|
方案一 |
▲ |
▲ |
|
方案二 |
▲ |
▲ |
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入少量氯气,则首先被氧化的离子是
▲ (填粒子的化学式);若在稀溴化亚铁溶液中通入过量氯气,则相应的离子方程式为 ▲ 。
①Br2 (1分);2Fe2++Br2=2Fe3++2Br- (2分)
②(每空1分,共4分)
|
|
选用试剂 |
实验现象 |
|
第一种方法 |
D |
溶液变红 |
|
第二种方法 |
E |
有机层无色 |
③Fe2+ (1分);2Fe2++4Br-+3Cl2 2Fe3++2Br2+6Cl- (2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com