
题目列表(包括答案和解析)
12.(江苏省赣榆一中2010届高三12月阶段考试化学)下列化学实验或操作能够达到目的的是
A 不加热的情况下,可以用铜片鉴别稀硝酸、稀硫酸和稀盐酸
B 乙酸乙酯中混有乙酸,可选用稀的 NaOH 溶液洗涤,然后将两层液体分开
C 将 10 gCuSO4·5H2O 溶解在 90g水中可以配制成质量分数为 10 %的 CuSO4溶液
D 淀粉在酸性条件下水解后,加入过量氢氧化钠溶液,再滴加几滴硫酸铜溶液,加热可以检验生成的葡萄糖
11.(江苏省赣榆一中2010届高三12月阶段考试化学)具备基本的化学实验技能是进行科学探究的基础和保证。下列有关实验操作正确的是 C
A B C D
10.(江苏省赣榆一中2010届高三12月阶段考试化学)化合物 KxFe(C2O4)y· 3H2O ( Fe 为 +3 价)是一种光敏材料,实验室可以用如下的方法来制备这种材料并测定这种材料的组成。
Ⅰ.制备

( 1 )结晶时应将溶液用冰水冷却,这样操作的原因是
( 2 )操作 a 的名称是 .
Ⅱ.组成测定
称取一定质量的晶体置于锥形瓶中,加入足量的蒸馏水和稀 HZSO 4 ,将 C2O42-转化为 H2C2O4后用 0 .1000 mol/LKMnO4溶液滴定,当消耗 KMnO4溶液 24.00mL 时恰好完全反应;再向溶液中加入适量的还原剂,恰好将 Fe3+完全转化为 Fe2+,用相同浓度的 KMnO4溶液继续滴定,当 Fe2+完全氧化时,用去 KMnO4溶液 4.00mL 。第二次滴定的离子方程式为
(3)配制 100mL0.1000 mol/LKMnO4溶液及滴定实验中所需的玻璃仪器除烧杯,玻璃棒、胶头滴管、量筒、锥形瓶外还有 (填仪器名称)。
( 4)该化合物 KxFe(C2O4)y· 3H2O中x=
( 1 )用冰水冷却可降低KxFe(C2O4)y· 3H2O的溶解度,析出更多的晶体( 2 分)
( 2 )过滤、洗涤( 2 分) MnO4-十 5Fe2+ + 8H+ ==Mn2++ 5Fe3+ + 4H2O ( 2 分)
( 3 ) 100 mL 容量瓶( 1 分)、酸式滴定管( l 分)
( 4 ) 3 ( 2 分)
9.(江苏省丹阳高级中学2010届高三上学期期中考试(化学))除去下列物质中少量杂质的方法正确的是 ( )
A.除去溴乙烷中中混有的溴杂质,加入适量NaOH溶液,振荡分液
B.除去KNO3晶体中混有的KCl杂质,加水溶解、蒸发结晶、过滤
C.除去Na2CO3晶体中混有的NaHCO3杂质,置于坩埚中充分加热
D.除去苯中溶有的少量苯酚:加入稍过量浓溴水反应过滤
8.(江苏省丹阳高级中学2010届高三上学期期中考试(化学))进行化学实验,观测实验现象,通过分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是 ( )
A.在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中含有SO42-
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口,说明此位置指示的是被蒸馏出物质的沸点。
C..溴水中通入SO2后,颜色褪去,说明SO2表现了漂白性
D.浓硝酸在光照条件下变黄,说明浓硝酸不稳定生成有色产物能溶于浓硝酸
7.(江苏省丹阳高级中学2010届高三上学期期中考试(化学))中学化学教材中,常借助于图像的这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理。下列有关化学图像表现的内容正确的是 ( C )

6.(江苏省丹阳高级中学2010届高三上学期期中考试(化学))下列是与硫元素相关的一系列实验:根据下图所示实验回答下列问题:

(1)试管C口部的棉团上发生反应的离子方程式是 。
(2反应一段时间后,将B试管中的溶液加热,可以观察到 。试管C中溶液变浑浊,则证明SO2具有 性。
(3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的化学方程式是 。
(4)如将B试管换成D试管,并从直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是 、 、 、 (要求填二种化合物和二种单质的化学式)。
(5)取下C试管,试管中溶液浑浊,煮沸后,再加入Na2S溶液并加热,溶液变澄清,经测定溶液中主要存在一种摩尔质量为128g/mol的阴离子(反应①)。向该澄清液中加入氯水,溶液仍然澄清(反应②),加入氯化钡可得一种不溶于稀盐酸的白色沉淀,写出反应①和反应②的离子方程式
(1)SO2 +2OH-=SO32-+H2O (1分)
(2) 溶液由无色变成红色 (1分) 氧化 (1分)
(3)吸收有害气体,防止污染空气 (1分)
NaHCO3+SO2=NaHSO3+CO2 (或2NaHCO3+SO2=Na2SO3+2CO2↑+H2O) (1分)
(4)NH3 NO2 ClO2 Cl2 、O3 O2(3分)
(5) 3S+S2- = S42- S42-+13Cl2+12H2O = 26Cl-+4SO42-+24H+(3分)
5.(江苏金陵中学高三年级期中考试题--化学)某校化学研究性学习小组的同学在学习了金属的知识后,为了解Cu的常见化合物性质,运用类比学习的思想提出如下的问题,进行探究。请你协助该小组的同学完成下列研究。
用类比学习的思想提出如下的问题,进行探究。请你协助该小组的同学完成下列研究。
[提出问题]
①Cu金属活泼性小于Al,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②通常情况下,+2价Fe稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?
③CuO能被H2、CO等还原,也能被NH3还原吗?
[实验方案]
(1)为解决问题①,需用到的药品有CuSO4溶液、 (填试剂),同时进行相关实验。
(2)解决问题②的实验步骤和现象如下:取98gCu(OH)2固体,加热至80°C~100°C时,得到黑色固体粉末,继续加热到1000°以上,黑色粉末全部变成红色粉末A。冷却后称量,A的质量为72g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在。据此可推得,A的化学式为 。
(3)为解决问题③,设计的实验装置为(夹持及尾气处理装置未画出):

实验中观察到CuO变为红色物质,无水CuSO4变蓝色。同时生成一种无污染的气体。
[实验结论]
(1)Cu(OH)2具有两性。证明Cu(OH)2具有两性的实验现象是 。
(2)根据“实验方案(2)”,得出的+1介Cu和+2价Cu稳定性大小的结论是:
在高于1000°C时, 价Cu稳定;在溶液中 价Cu稳定。
(3)CuO能被NH3还原。该反应的化学方程式为 。
(1)NaOH溶液 HCl溶液
(2)Cu2O
[实验结论]
(1)Cu(OH)2既溶于酸又溶于碱
 (2)+1 +2
(2)+1 +2
(3)2Mg+3CuO 3Cu+3H2O+N2
4.(如皋市2010届高三综合测试)关于下列各装置图的叙述中,不正确的是( )

A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
24.(10分)通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对环境的积极意义在于_______________________________。
(2)最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
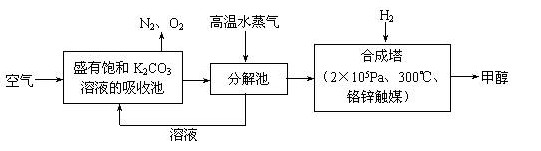
①吸收池中反应的化学方程式为_____________________________________。
②在合成塔中,若有4.4kg CO2与足量H2恰好完全反应,可放出4947
kJ的热量,试写出合成塔中发生反应的热化学方程式________________________________。
(3)小李同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积(Ksp)分别为4.96×10-9、2.58×10-9。
小李应该选用的试剂是___________________,实验时测定的数据除空气的体积外,还需要测定____________________________________________________________。
福建省福州三中2010届高三上学期月考
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com