
题目列表(包括答案和解析)
7.PbO2在酸性溶液中能将Mn2+氧化成MnO4-,本身被还原为Pb2+。取一支试管,加入适量PbO2固体和适量的稀H2SO4后滴入2mL 1mol/L MnSO4溶液。下列说法错误的是 ( )
A.充分振荡后静置,溶液颜色变为紫色
B.上述实验中不能用盐酸代替硫酸
C.若上述实验完全反应,消耗PbO2的物质的量为0.01mol
D.在酸性条件下,PbO2的氧化性比MnO4-的氧化性强
6.将标准状况下,将VL A气体(摩尔质量为M g/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶液的物质的量浓度(mol/L)为 ( )
A.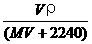 B.
B.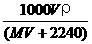
C.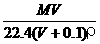 D.1000VρM(MV+2240)
D.1000VρM(MV+2240)
5.下列各组离子在指定溶液中一定能大量共存的是 ( )
①无色溶液中:K+、Na+、Cr2O72-、SO42-
②pH=11的溶液中:CO32-、Na+、NO3-、Al(OH)4-
③加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+
④在由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、I-
⑤在溶液中能大量共存,加入NaOH后加热既有气体放出又有沉淀生成的溶液:Ca2+、HCO3-、NH4+、AlO2-
⑥能使酚酞变红色的溶液:Na+、C1-、S2-、SO32-
A.①③⑤ B.②④⑤ C.②④⑥ D.④⑤⑥
4.用NA表示阿伏加德罗常数,下列叙述中不正确的是 ( )
A.在标准状况下,NA个甲基(-CH3)和NA个羟基(-OH)所含电子数相等
B.1mol Fe与足量氯气反应时,铁失去的电子数目为3NA
C.120g由NaHSO4和KHSO3组成的混合物中含硫原子数目为NA
D.1molCH3+中含有电子数为10NA
3.下列离子方程式书写正确的是 ( )
A.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O
B.亚硫酸氢钠水解:HSO3-+H2O
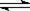 SO32-+H3O+
SO32-+H3O+
C.氧化铁溶于氢碘酸:Fe2O3+6H+ = 2Fe3++3H2O
D.用石墨电极电解NaCl溶液:2Cl-+2H2O  2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
2.在V L硫酸铁溶液中,含有Wg的SO42-,这种溶液中Fe3+的物质的量浓度为 ( )
A.W/144V B.W/64V C.W/96V D.3W/56V
1.下列对“摩尔(mol)”的叙述不正确的是 ( )
A.摩尔是一个物理量
B.摩尔是一个单位,用于计量物质所含微观粒子的多少
C.摩尔既能用来计量纯净物,又能用来计量混合物
D.1mol任何气体所含的气体分子数目都相等
16、(10分) 乙醇汽油是将乙醇和普通汽油按一定体积比混合而成,其密度与乙醇几乎相等,其中氧的质量分数为3.5%。请回答下列问题:
(1)乙醇汽油中乙醇的体积分数约为 。
(2)为减少氮的氧化物排放,将燃烧汽油的汽车改为以天然气为燃料电池的电动车,电池总反应为:CH4+2O2+2KOH==K2CO3+3H2O,则该电池的负极反应为 。
(3)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4+4NO2 = 4NO+CO2+2H2O;CH4+4NO = 2N2+CO2+2H2O
 若用标况下4.48 L CH4还原NO2至N2,整个过程中转移的电子数为 。
若用标况下4.48 L CH4还原NO2至N2,整个过程中转移的电子数为 。
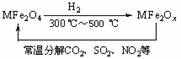
(4)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M = Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得。常温下,它能使汽车尾气中的酸性氧化物分解除去。转化流程如图所示:
请写出MFe2Ox分解SO2的化学方程式
(不必配平)。
(5)请列举推广使用乙醇汽油的优点(至少回答两点): 。
15、(12分)元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)第四周期过渡元素的明显特征是形成多种多样的配合物。
① CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式)。
② 金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列 。
a. 水 b. 四氯化碳 c. 苯 d. 硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 。
(3)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是 。
a.直线形;三角锥形 b.V形;三角锥形 c.直线形;平面三角形 d.V形;平面三角形
14.根据下列有关图象,说法正确的是
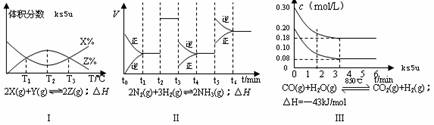 A.由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0
A.由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0
B.由图Ⅱ知,反应在t6时,NH3体积分数最大
C.由图Ⅱ知,t3时采取降低反应体系压强的措施
D.Ⅲ在10L容器、850℃时反应,由图知,到4min时,反应放出51.6kJ的热量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com