
题目列表(包括答案和解析)
3、在pH=1的无色透明溶液中,能大量共存的离子组为:
A.Na+ I- SO42- Mg2+ B.SO32- K+ NO3- Cl-
C.Cr2O72- K+ NO3- Cl- D.K+ Na+ CO32- SO42-
2、下列离子方程式书写正确的是:
A.铜和稀硫酸反应:Cu+2H+=Cu2++H2↑
B.向NaHCO3溶液中滴加少量石灰水:Ca2++OH-+HCO3-=CaCO3↓+H2O
C.Cl2和H2O反应:Cl2+H2O=2H++Cl-+ClO-
D.石灰水中通足量CO2:OH-+CO2=HCO3-
1、NA表示阿伏加德罗常数,下列说法正确的是:
A.常温常压下,7.1gCl2和足量的NaOH反应,转移电子数0.2NA
B.标准状况下,11.2L氩气含原子数NA
C.32gO2和O3混合气体含氧原子数2NA
D.18gH2O和18gD2O所含电子数均为10A
11(15分)浓H2SO4和木炭在加热时发生反应的化学方程式是
2H2SO4(浓)+C  CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
 请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
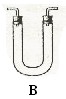
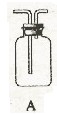
将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
|
选用的仪器 (填字母) |
加入的试剂 |
作用 |
|
|
|
|
12(16分)实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:

(1)溶解大理石时,用硝酸而不同硫酸的原因是_______________________________;
(2)操作Ⅱ的目的是______________,溶液A(溶质是共价化合物)是___________;
(3)写出检验滤液中是否含铁离子方程式:_____________________________________
______________________________________________________________________;
(4)写出加入碳酸铵所发生反应的离子方程式:________________________________;
写出滤液B的一种用途:_________________________;
(5)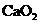 中一般含
中一般含 。试按下列提示完成
。试按下列提示完成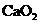 含量分析的实验设计。
含量分析的实验设计。
试剂:氢氧化钠标准溶液、盐酸标准溶液、酚酞 仪器:电子天平、锥形瓶、滴定管
实验步骤:
① ;②加入 ;③加入酚酞,用氢氧化钠标准溶液滴定。
13(19分)某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将 氧化成
氧化成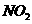 ,而稀硝酸不能氧化
,而稀硝酸不能氧化 。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
。由此得出的结论是浓硝酸的氧化性强于稀硝酸。

可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与 反应,能与
反应,能与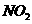 反应
反应

(1)实验应避免有害气体排放到空气中,装置③、④、⑥中乘放的药品依次是
;
(2)滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
;
(3)装置①中发生反应的化学方程式是 ;
(4)装置②的作用是 ,发生反应的化学方程式是 ;
(5)该小组得出的结论的试验现象是
;
(6)试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别涉及了一下4个试验来判断两种看法是否正确。这些方案中可行的是(选填序号字母) 。
a. 加热该绿色溶液,观察颜色变化
b. 加水稀释绿色溶液,观察颜色变化
c. 向该绿色溶液中通入氮气,观察颜色变化
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体,观察颜色变化
广东省增城中学2010届高三化学晚练
10、(双选)溴水中存在着如下的平衡: ,若要使溴水的颜色变浅,可采取的措施是
,若要使溴水的颜色变浅,可采取的措施是
A.加压 B.加入NaF晶体 C.通入SO2气体 D.通入HF气体
班级 学号
姓名 成绩
9、(双选)下列化学反应的离子方程式正确的是
A.AgNO3溶液中加入过量氨水:Ag++NH3·H2O=AgOH+NH4+
B.Fe3O4溶解于稀硝酸中:Fe3O4 + 8H+ = 3Fe3+ + 4H2O
C.在硫酸氢钾溶液中加入Ba(OH)2溶液至pH=7:
2H++SO42-+Ba2++2OH–== BaSO4↓+2H2O
D.石灰乳与MgCl2溶液反应:Mg2+ + Ca(OH)2 = Ca2+ + Mg(OH)2
8、对数据的分析归纳可得到科学的结论和规律。下列某同学对数据的利用情况,其中不正确的是
A.根据非金属单质与氢气化合生成1 mol产物时反应热的大小推测生成物的稳定性
B.用沸点数据推测用蒸馏法分离两种液体混合物的可能性
C.用熔点数据分析不同分子的稳定性
D.用同周期元素的原子(离子)半径数据推断某些原子(离子)氧化性或还原性的相对强弱
7、据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学方程式为:5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是
A.上述反应是放热反应
B.产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾)
C.因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替
D.上述反应中消耗3molP时,转移电子的物质的量为15mol
6、下列各装置中,夹紧②、③、④中的弹簧夹,并作相关操作,会漏气的装置是:
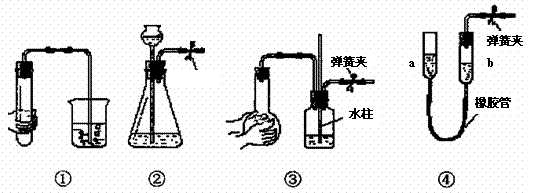 A.对装置①,双手移去后.导管中水面与烧杯水面相平
A.对装置①,双手移去后.导管中水面与烧杯水面相平
B.对装置②,长颈漏斗内液面高度保持不变
C.对装置③,长导管内形成一段水柱
D.对装置④,上移a管后,a、b两端液面形成了一段稳定的高度差
5、假设与猜想是科学探究的先导,在下列假设(或猜想)引导下的探究活动肯定没有实际意义的是
A.探究浓硫酸与铜在一定条件下反应产生的黑色物质中可能有CuS
B.探究SO2和Na2O2反应可能有Na2SO4生成
C.探究Na与水的反应可能有O2生成
D.向滴有酚酞的NaOH溶液中通入 Cl2,探究红色褪去的原因是溶液的酸碱性变化还是HClO的漂白性所致
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com