
题目列表(包括答案和解析)
20.(8分)有人设想合成具有以下结构的烃分子。

(1)结构D显然是不可能合成的,原因是 。
(2)在结构A的每两个碳原子之间插入一个CH2原子团,可以形成金刚烷的结构,写出金刚烷的分子式 。
(3)B的一种同分异构体是最简单的芳香烃,能证明该芳香烃中的化学键不是单双键交替排列的事实是 。
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(4)C的一种属于芳香烃的同分异构体是生产某塑料的单体,写出合成该塑料的化学方程式 。
19.(12分)有下列转代关系:
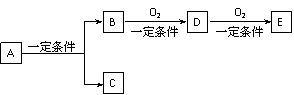
(1)若C是可用来自来水消毒的气体,D、E是氧化物,D能化为E时增加氧的质量是总质量的25.8%,则A是 (写化学式)并写出A在一定条件下生成的C的化学方程式 。
(2)若E是酸酐,且为无色易挥发的晶体,A为气态氢化物,则A与D反应生成B的化学方程式为 。
(3)若A是氯代烃,B是含氧化合物,且在同系物中是相对分子质量第二小的化合物;E能使紫色石蕊试液显红色,则A的结构简式为 。A、B、D、E中易溶于水的是 。(写结构简式)
(4)若B是无氧化合物, E为红棕色的气体,则B→D反应的化学方程式:
。
18.(10分)下表是部分短周期元素的原子半径及主要化合价:
|
元素代号 |
W |
R |
X |
Y |
Z |
Q |
|
原子半径/nm |
0.037 |
0.186 |
0.074 |
0.075 |
0.077 |
0.110 |
|
主要化合价 |
+1 |
+1 |
-2 |
-3,+5 |
+2、+4 |
-3、+5 |
试回答下列问题:
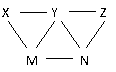
(1)五种元素中原子半径最大的元素在周期表中位置是 。
(2)Y的氢化物比Q的氢化物沸点高的原因是 。
(3)X或与R按1∶1的原子个数比形成化合物甲,甲中存在的化学键有 ;X可与W组成含18e-的化合物乙,则乙的电子式为 ;X可与Z组成一种有恶臭味的气体丙,丙分子中各原子最外层均满足8e-结构,且含有非极性键。1 mol丙气体可与2 mol氧气完全反应,生成一种气体,且反应前后气体的总体积不变,该生成物能使澄清石灰水变浑浊,请写出丙分子的结构式 。
17.(14分)以下是有关SO2、Cl2的性质实验。
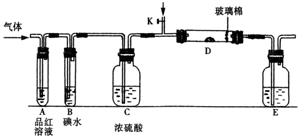 (1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若装置D装的是铁粉,通入Cl2与铁粉充分反应时现象为 ;若装置D中装的是五氧化二钒(催化剂)。通入SO2时,打开K通入适量O2的化学反应方程式为 。
②若装置B中装有5.0 mL 1.0×10-3mol/L在碘水,当通入足量Cl2完全反应后,共转移了5.0×10-5mol电子,该反应的化学方程式为 。
③E中盛有 溶液。
(2)某同学将足量的SO2通入一支装有氧化钡溶液的试管,未见沉淀生成,若向该试管中加入适量(填字母) ,则可以看到白色沉淀产生。
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4∶3;当Cl2的与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。
16.下列化学方程式或离子方程式不正确的是( )
A.S与Cu反应 Cu+S CuS
CuS
B.酸雨放置过程中pH变小 2H2SO3+O2═2H2SO4
C.亚硫酸氢钙溶液与澄清的石灰水混合 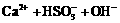 ═CaSO3↓+H2O
═CaSO3↓+H2O
D.向Na2S和Na2SO3的混合溶液中滴加稀H2SO4 [n(Na2S)∶n(Na2SO3)=2∶1]
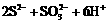 ═3S↓+3H2O
═3S↓+3H2O
15. 现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互反应,图中每条连线两端的物质可以发生反应。下列判断不合理的是( )
现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互反应,图中每条连线两端的物质可以发生反应。下列判断不合理的是( )
A.X一定为H2SO4
B.Y一定为K2CO3
C.Z可能为氯水
D.M、N必定各为BaCl2、FeSO4中的一种
14.二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。
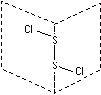 常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红溶液褪色的气体。下列说法中错误的是( )
常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红溶液褪色的气体。下列说法中错误的是( )
A.S2Cl2的结构式Cl-S-S-Cl
B.S2Cl2的含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可为2S2Cl2+2H2O═SO2↑+3S↓+4HCl
13.检验某未知溶液是否含有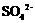 ,下列操作最合理的是( )
,下列操作最合理的是( )
A.加入HNO3酸化的Ba(NO3)2溶液
B.加入盐酸酸化的BaCl2溶液
C.先用盐酸酸化,若有沉淀产生,过滤,在滤液中再加BaCl2溶液
D.先加BaCl2溶液,若有沉淀产生,再加盐酸
12.下列反应中,调节反应物用量或浓度,不会改变反应产物的是( )
A.铁在硫蒸气中燃烧 B.H2S在空气中燃烧
C.二氧化硫通入澄清石灰水 D.硫酸中加入锌粉
11.下列有关浓H2SO4性质的叙述中,错误的是( )
A.浓硫酸具有脱水性,因而能使蔗糖炭化
B.在反应HCOOH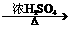 CO↑+H2O中,浓H2SO4只表现脱水性
CO↑+H2O中,浓H2SO4只表现脱水性
C.在反应Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性
CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性
D.浓硫酸具有吸水性,因而能使CuSO4·5H2O转化为CuSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com