
题目列表(包括答案和解析)
8.11.87 g金属锡跟l00
mL l2 mol/L  共热一段时间,完全反应后测得溶液中的
共热一段时间,完全反应后测得溶液中的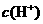 = 8 mol/L,溶液的体积仍为l00 mL,放出的气体在标准状况下为8.96 L。由此推断氧化产物可能是
= 8 mol/L,溶液的体积仍为l00 mL,放出的气体在标准状况下为8.96 L。由此推断氧化产物可能是
A.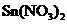 B.
B.
C.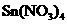 D.
D.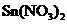 和
和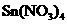
第二卷
7.已知:T℃时,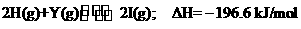 。T℃时,在一压强恒定的密闭容器中,加入4 mol H和2 mol Y反应,达到平衡后,放出354 kJ的热量。若在上面的平衡体系中,再加入1 mol I气体,T℃时达到新的平衡,此时气体H的物质的量为
。T℃时,在一压强恒定的密闭容器中,加入4 mol H和2 mol Y反应,达到平衡后,放出354 kJ的热量。若在上面的平衡体系中,再加入1 mol I气体,T℃时达到新的平衡,此时气体H的物质的量为
A.0.8 mol B.0.6 mol C.0.5 mol D.0.2 mol
6.常温下的下列混合溶液中,各离子浓度的大小顺序正确的是
A.10 mL
pH=13的氨水与10 mL pH=1的盐酸混合:
B.10 mL 0.1
mol/L 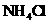 溶液与5 mL 0.2 mol/L NaOH溶液混合:
溶液与5 mL 0.2 mol/L NaOH溶液混合:
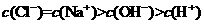
C.10 mL 0.1
mol/L  溶液与10 mL pH=13的NaOH混合:
溶液与10 mL pH=13的NaOH混合:
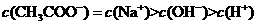
D.10 mL 0.5
mol/L  溶液与6 mL pH=0的盐酸混合:
溶液与6 mL pH=0的盐酸混合:
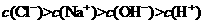
5.有一澄清透明的溶液,只可能含有大量的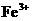 、
、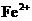 、
、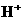 、
、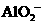 、
、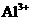 、
、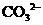 、
、 七种离子中的几种,向该溶液中逐滴加入一定量1 mol/L NaOH溶液的过程中,开始没有沉淀,而后才有沉淀。则下列判断正确的是
七种离子中的几种,向该溶液中逐滴加入一定量1 mol/L NaOH溶液的过程中,开始没有沉淀,而后才有沉淀。则下列判断正确的是
A.溶液中可能含有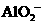 B.溶液中可能含有
B.溶液中可能含有
C. 溶液中一定不含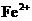 和
和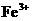 D.溶液中可能含有
D.溶液中可能含有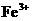 ,但一定不含
,但一定不含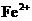
4.A、B、C、D都是周期表中前20号元素,已知A的阳离子和C的阴离子具有相同的核外电子排布,且能形成组成为AC的化合物;C和D属同主族,其中C的核外电子数是D的核内质子数的2倍。B和D是同周期元素且A和B能形成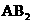 型化合物。下列说法中正确的是
型化合物。下列说法中正确的是
A.D元素处于元素周期表中第二周期Ⅵ族
B. 分子一定是极性分子
分子一定是极性分子
C.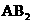 中可能既有离子键又有共价键
中可能既有离子键又有共价键
D.四种元素的原子半径大小一定是
3.下列各晶体熔沸点高低的比较,正确的是
A.硅 金刚石
金刚石 石英砂 B.
石英砂 B.
C.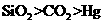 D.
D.
2.阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
A.4 g重水(D2O)中所含中子数为0.2×6.02×1023
B.32g含有少量臭氧的氧气中,共含有氧原子1.204×1024
C.4.48 L H2和O2的混合气体中所含分子数为0.2×6.02×1023
D.0.1 molNa2O2 溶解于足量的水中,转移电子数为0.2×6.02×1023
1.化学用语是学习化学的工具和基础。下列有关化学用语的使用正确的是 ( )
A.用食醋除去水壶内的水垢:CaCO3+2H+=Ca2++CO2↑+H2O
|
 H2CO3+2OH-
H2CO3+2OH-
C.用铁作阳极,电解饱和食盐水的离子方程式:Fe+2H2O Fe(OH)2 + H2↑
D.表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(1);△H=-571.6KJ·mol-1
20. (12分)
(12分)
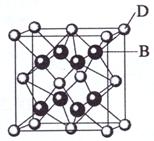
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。
请回答:
(1)A元素的名称是 ;
(2)B的元素符号是 ,C的元素符号是 ,B与A形成的化合物比C 与A形成的化合物沸点高,其原因是
(3)E属元素周期表中第 周期,第 族的元素,其元素名称是 ,它的+2价离子的电子排布式为 :
(4)从图中可以看出,D跟B形成的离子化合物的化学式为 ;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出算式)。
19. (10分)硝酸铜受热易分解:2Cu(NO3)2
 2CuO+4NO2↑+O2↑,当温度达到800℃时,CuO开始分解:4CuO
2CuO+4NO2↑+O2↑,当温度达到800℃时,CuO开始分解:4CuO
 2Cu2O+
O2↑,至1000℃以上,CuO完全分解(加热过程中忽略2NO2⇌N2O4,2NO2=2NO+O2等反应)。
2Cu2O+
O2↑,至1000℃以上,CuO完全分解(加热过程中忽略2NO2⇌N2O4,2NO2=2NO+O2等反应)。
现取5.64gCu(NO3)2无水晶体,在一定温度下使其分解,将生成的气体及时导出并用足量的NaOH溶液充分吸收。
(1)若该质量的无水硝酸铜经加热完全分解,其中的铜元素全部转化为氧化铜,则氧化铜的质量是_____________。
(2)若该质量的无水硝酸铜完全分解,铜元素全部转化为氧化亚铜,反应过程中生成的气体被足量的NaOH溶液充分吸收后,还有多余的气体,则多余的气体是______________(填分子式),其体积(标准状况)是_____________L,
(3)若该质量的无水硝酸铜分解后的残留固体中含有1.60g CuO,则残留固体的质量可能是______________________g。
(4)设该质量的无水硝酸铜在分解过程中,得到的残留固体质量为xg,生成的气体中NO2和O2的体积比为y,求y与x的关系式: ;
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com