
题目列表(包括答案和解析)
6.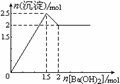 右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是
右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是
A.MgSO4 B.Al2(SO4)3
C.KAl(SO4)2 D.NaAlO2
5.溶液中有如下反应(未配平):FeSO4+NaClO3+H2SO4→Fe2(SO4)3+NaCl+H2O
有关叙述正确的是:
A.当有1mol电子转移时,消耗硫酸1mol
B.消耗3mol Fe2+,有0.5mol ClO3-被氧化
C.反应中氧化剂和还原剂物质的量之比为6:1
D.若用浓HNO3代替NaClO3,当生成等量的Fe3+时,n(HNO3)>n(NaClO3)
4.下列反应中同位素示踪表示正确的是
A.2Na218O2 + 2H2O == 4Na18OH + O2↑
B.2KMnO4 + 5H218O2 + 3H2SO4 == K2SO4 + 2MnSO4 + 518O2↑ + 8H2O
 C.NH4Cl + 2H2O
NH3· 2H2O + HCl
C.NH4Cl + 2H2O
NH3· 2H2O + HCl
D.K37ClO3 + 6HCl == K37Cl + 3Cl2 ↑+ 3H2O
3.(07江苏9)下列离子方程式书写正确的是
A.过量的SO2通入NaOH溶液中:SO2+2OH-=SO32-+H2O
B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2
C.NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O
D.NaHCO3溶液中加入过量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32-
2.某溶液中含有HCO3-、SO32-、SO42-、Cl-和Na+,若向其中通入Cl2后溶液中离子浓度增大的是
A.HCO3- B.SO42- C.SO32- D.Na+
1.关注食品安全、关爱生命健康是开展生命、生存、生活“三生教育”的一项重要内容。下列有关食品安全的说法正确的是
A.食品添加剂一般对人体无害,可任意添加
B.用二氧化硫漂白过的银耳不仅色泽美观,而且营养更丰富
C.在食盐中加入碘酸钾有利于防止甲状腺肿大
D.往婴幼儿奶粉里添加三聚氰胺可以提高奶粉中蛋白质的含量
4.某芳香族化合物A,苯环上只有一个取代基,完全燃烧只生成二氧化碳和水,一定条件下存在如下图所示的转化关系:
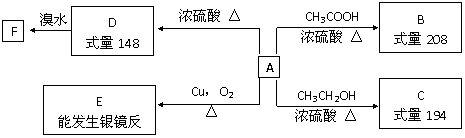
请回答下列问题:
⑴A的摩尔质量为______,在一定条件下B可能发生的化学反应的类型有_______(填序号)。
①水解反应。②取代反应。③加成反应。④消去反应。⑤加聚反应。
⑵C的结构简式为_______________,E的结构简式为_________________。
⑶写出下列转化的化学方程式:
①A→B:______________________________________________________________。
②D→F:______________________________________________________________。
⑷符合下列三个条件的A的同分异构体的数目有__________个
①含有二取代苯环结构。②与A有相同的官能团。③能与FeCl3溶液发生显色反应。
安庆市示范高中2010届高三上学期四校元旦联考
3.盐酸、硫酸和硝酸是中学阶段常见的三种酸。请就三种酸与金属铜反应的情况, 回答下列问题:(1)稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解,该反应的离子方程式为 。
某同学未加入氧化剂,而是设计了一个实验装置,也能使铜很快溶于稀盐酸。请在方格中画出该装 置
置
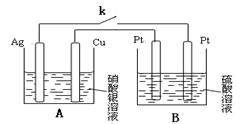
(2)由4根同质量的电极材料(Ag Cu Pt)组成下列装置。下列装置A为 池(填写”原电”或”电解”),发生氧化反应的电极反应式为: ,B池中阳极的电极反应式为:______________________________。当关闭电键k一段时间,发现Ag棒与 Cu棒质量差为28g时,则装置B产生气体的总质量为 g(电解质溶液足量)。
(3)将等质量的铜片分别与等体积、过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出可能是Cu2+浓度不同引起的,你同意这种看法吗 ? (填 “同意”或“不同意”),理由是
2. 与
与 是两种重要的酸式盐。
是两种重要的酸式盐。
(1) 圆体溶于水显酸性,而
圆体溶于水显酸性,而 固体溶于水显碱性,请用离子方程式并配以必要的文字说明表示
固体溶于水显碱性,请用离子方程式并配以必要的文字说明表示 固体溶于水显碱性的原因
固体溶于水显碱性的原因
(2)常温下把l mL 0.2 mol/L的 溶液加水稀释成2 L溶液,此时溶液中由水电离产生的
溶液加水稀释成2 L溶液,此时溶液中由水电离产生的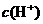 为
。
为
。
(3) 和
和 两溶液混合反应的离子方程式为
。
两溶液混合反应的离子方程式为
。
(4)向 溶液中逐滴加入
溶液中逐滴加入 溶液至呈中性,请写出发生的离子方程式
溶液至呈中性,请写出发生的离子方程式
;在以上溶液中,继续滴加 溶液,此时发生的离子方程式为
。
溶液,此时发生的离子方程式为
。
(5)若将等体积、等物质的量浓度的 溶液和
溶液和 溶液混合,反应的离子方程式为
。
溶液混合,反应的离子方程式为
。
1.A、B、C、D四种短周期元素的原子序数依次增大,A元素的气态氢化物与A元素的最高价氧化物对应的水化物能反应生成盐;B、C、D同周期,它们的最高价氧化物对应的水化物两两之间都能反应生成盐和水,B和D可组成化合物BD,回答下列问题。
(1)B的最高价氧化物对应的水化物与C的氧化物在溶液中反应的离子方程式为:
。
(2)B、D的最高价氧化物对应的水化物在稀溶液中反应,若生成0.25mol水时放出Q kJ的热量,则该反应的热化学方程式为 。
(3)在BHCO3的水溶液中,c(B+)-c(H2CO3)= 。
(4)在一定条件下,将2molA2和3molH2在一固定体积的密闭容器中反应达到平衡状态,此时容器中混合气体的平均相对分子质量为15.5,则H2的转化率为 。若平衡后,再按n(A2):n(H2):n(AH3)=3:3:2向该密闭容器中充入气体,当重新达到平衡后,A2
在平衡混合气中的百分含量较原平衡 (填“大”、“小”或“不变”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com