
题目列表(包括答案和解析)
1、在酸性溶液中能大量共存而且为无色透明的溶液是( )
A、Na+、K+、HCO3-、NO3- B、K+、Fe2+、NH4+、NO3-
C、K+、Na+、NO3-、OH- D、NH4+、Al3+、SO42-、NO3-
9.阿扎西隆(azasetron)适用于治疗由服用药物引起的恶心、呕吐等消化道症状。文献资料显示,它可由水杨酸甲酯(a)为原料合成,部分合成路线如下:

试回答下列问题
(1)上述反应中不属于取代反应的是 [选填序号:①②③④⑤⑥⑦]。
(2)反应②的试剂是: 。
(3)水杨酸甲酯发生一硝基取代时,反应的可能产物中较多的两种是 (填序号)。
|
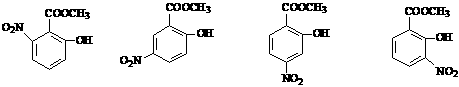
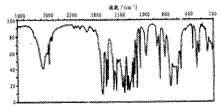
(4)水杨酸甲酯的某图谱如下,它可能是: (A.核磁共振氢谱 B.质谱 C.红外光谱)
 (5)水杨酸甲酯的同分异构体很多,其中能与碳酸氢钠溶液放出二氧化碳,再加入氯化铁溶液又显紫色的同分异构体有 种。
(5)水杨酸甲酯的同分异构体很多,其中能与碳酸氢钠溶液放出二氧化碳,再加入氯化铁溶液又显紫色的同分异构体有 种。
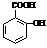
(6)水杨酸甲酯是水杨酸与甲醇形成的酯,水杨酸( )在一定条件下也能进行缩聚,写出在催化剂作用下水杨酸缩聚的化学方程式 。
江苏省东台市五烈镇中学2010届高三化学周练
8.在热的稀硫酸溶液中溶解了11.4 g FeSO4。当加入50 mL 0.5 mol·L-1 KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy氮氧化物气体逸出。

(1)推算出x=___________ ,y=___________。(2)配平该化学方程式(系数填写在上式方框内)。
(3)反应中氧化剂为___________。(4)用短线和箭头标出电子转移的方向和总数。
7.某结晶水合物的化学式为A·nH2O,其相对分子质量为M,在25℃时,ag晶体溶于bg水中即达饱和,形成密度为ρg/mL的溶液,下列表达式正确的是 ( )
A.饱和溶液的物质的量浓度为:1000a(M-18n)/M(a+b)mol/L
B.饱和溶液中溶质的质量分数为:100a(M-18n)/M(a+b)%
C.饱和溶液的体积为:(a+b)/ρL
D.25℃时,A的溶解度为:a(M-18n)/(bM+18an)g
6.用NA表示阿伏加德罗常数,下列说法正确的是( )
A.1mol CH3+ 所含的电子数目为6NA
B.72gC5H12中含有C−C键的数目一定为4NA
C.活泼金属与盐酸反应时,每放出1 mol H2,其电子转移的数目为2NA
D.常温常压下,22.4L NH3所含的电子数目为10NA
5.下列反应的离子方程式书写错误的是 ( )
A.溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
B.苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3-
C.铁屑溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
D.碳酸氢铵溶液与足量烧碱溶液反应:HCO3-+OH-=CO32-+H2O
4.Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反应,完全反应后,测得溶液中NaClO与NaClO3的物质的量之比为4︰1,则溶液中NaCl与NaClO的物质的量之比为 ( )
A. 1︰1 B. 5︰1 C. 9︰4 D. 11︰2
3.用NA表示阿伏加德罗常数。下列叙述正确的是 ( )
A.100mL3mol/L盐酸与5.6gFe充分反应转移0.3NA个电子
B.6g尿素与葡萄糖的混合物在足量氧气中完全燃烧生成0.2NA个水分子
C.12gC60( )中含有NA个共价键
)中含有NA个共价键
D.10mL5mol/L(NH4)2SO4溶液中含有NH4+数目为0.1NA个
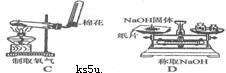
2.下列各图所示的实验原理、方法、装置和操作正确的是 ( A )

1.下列说法正确的是 ( )
A.一定温度、压强下,气体体积由其分子的大小决定
B.不同的气体,若体积不等,则它们所含的分子数一定不等
C.把100mL3mol·L-1的H2SO4跟100mLH2O混合,硫酸的物质的量浓度变为1.5mol·L-1
D.把100g20%的NaCl溶液跟100gH2O混合后,NaCl溶液的质量分数是10%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com