
题目列表(包括答案和解析)
8、将氢气、甲烷、乙醇等物质在氧气中燃烧时的化学能直接转化为电能的装置叫燃料电池。燃料电池的基本组成为电极、电解质、燃料和氧化剂。此种电池能量利用率可高达80%(一般柴油发电机只有40%左右),产物污染也少。下列有关燃料电池的说法不正确的是( )
A.上述燃料电池的负极反应材料是氢气、甲烷、乙醇等物质
B.氢氧燃料电池常用于航天器,是因为该电池的产物为水,经处理之后可供宇航员使用
C.乙醇燃料电池的电解质常用KOH,该电池的负极反应为:C2H5OH-12e-=2CO2↑+3H2O
D.甲烷燃料电池的正极反应为:O2+2H2O+4e-=4OH
7、X、Y、Z是3种短周期元素,其中X、Z位于同一主族,X、Y处于同一周期。X原子的最外层电子
数是其电子层数的3倍。X原子的核外电子数比Y原子少1。下列说法正确的是( )
A.元素非金属性由弱到强的顺序为Z<Y<X
B.3种元素中X元素的最高价氧化物对应的水化物的酸性最强。
C.3种元素的气态氢化物中,Y气态氢化物沸点最高。
D.其对应的阴离子半径由大到小的顺序为Zn->Ym->Xn-
6、下列实验操作: ⑴用托盘天平称取5.2gNaCl;⑵用50mL量筒量取5.2mL盐酸;⑶用蒸发皿加热KNO3溶液制取KNO3晶体;⑷用100mL容量瓶配制50mL0.1mol/LH2SO4溶液;⑸用带玻璃塞的棕色试剂瓶存放浓HNO3;⑹用煤油液封保存锂、钠、钾单质。其中错误的是( )
A.(2)(3)(5) B.(2)(4)(5) C.(1)(4)(6) D.(2)(4)(6)
5、下列变化不属于水解反应的是( )
①NH3+H2O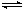 NH4++OH-;②HCO3-+H2O
NH4++OH-;②HCO3-+H2O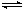 H2CO3+OH-;③AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-;
H2CO3+OH-;③AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-;
④Al3++3HCO3-=Al(OH)3↓+3CO2↑;⑤HCO3-+H2O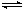 H3O++CO32-;⑥NH4cy++2H2O
H3O++CO32-;⑥NH4cy++2H2O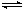 NH3·H2O+H3O+。
NH3·H2O+H3O+。
A.①③⑤ B.②③⑤ C.①④⑤ D.①③
4、下列叙述不正确的是
A.常温下浓硫酸可贮存在铁制或铝制容器中,说明常温下铁和铝与浓硫酸不反应
B.将Cl2和SO2分别通入到品红溶液中,均能使品红溶液褪色
C.反应AgCl + NaBr AgBr + NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水
AgBr + NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水
D.硝酸银溶液通常保存在棕色试剂瓶中,是因为硝酸银见光易分解
3、相互反应时,无论何种试剂过量离子方程式都正确的是
 A.盐酸与NaAlO2溶液:
A.盐酸与NaAlO2溶液: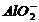 +H++H2O
Al(OH)3↓
+H++H2O
Al(OH)3↓
 B.石灰水与磷酸二氢钠溶液:2H2PO
B.石灰水与磷酸二氢钠溶液:2H2PO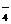 +3Ca2++4OH- Ca3(PO4)2↓+4H2O
+3Ca2++4OH- Ca3(PO4)2↓+4H2O
 C.明矾溶液与小苏打:Al3++3HCO
C.明矾溶液与小苏打:Al3++3HCO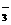 Al(OH)3+3CO2↑
Al(OH)3+3CO2↑
 D.硫酸氢钠溶液和氢氧化钡:SO
D.硫酸氢钠溶液和氢氧化钡:SO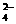 + 2H+ +Ba2+ + 2OH- BaSO4↓
+ 2H2O
+ 2H+ +Ba2+ + 2OH- BaSO4↓
+ 2H2O
2、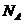 为阿伏加德罗常数,下列叙述正确的是
为阿伏加德罗常数,下列叙述正确的是
A.3.5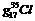 原子中所含中子数为1.7
原子中所含中子数为1.7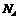 B.一定条件下,1
B.一定条件下,1
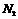 与足量
与足量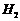 反应,可生成2
反应,可生成2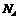 个
个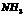 分子
分子
C.在含1 碳原子的石墨中,“C-C”键数为3
碳原子的石墨中,“C-C”键数为3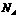 D.
D.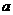

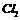 与足量烧碱溶液完全反应转移的电子数为
与足量烧碱溶液完全反应转移的电子数为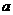
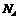
1、化学与生活是紧密相联的,下列关于生活与化学的说法正确的是
A.随着人们生活节奏的加快,方便的小包装食品已被广泛接受,为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常放入生石灰
B.现在用的清洁燃料主要有两类:一类是压缩天然气,另一类为液化石油气,前者属于碳氢化合物,后者是烃的衍生物。
C.环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于有机物
D.保护加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉
16、我国规定饮用水质量标准必须符合下表要求:以下是源水处理成自来水的工艺流程示意图
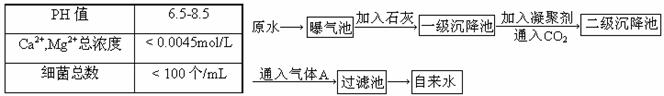
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式____ _________
(2)凝聚剂除去悬浮固体颗粒的过程_____(填写编号,多选倒扣)①只有物理过程 ②只是化学过程 ③是物理和化学过程 FeSO4·7H2O常用的凝聚剂,它在水中最终生成_____ ______沉淀。
(3)通入二氧化碳的目的是__________ _______和_______ ______。
(4)气体A通常使用氯气,氯气的作用是基于其和水反应的产物之一具有______________性,请写出氯气与水反应的离子反应方程式 。
(5)下列物质中能作为氯气的代用品的是 (填写编号,多选倒扣)
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
15、(1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有 种。
(2)第ⅢA、ⅤA族元素组成的化合物AlN、AlP、AlAs等是人工合成的平等体材料,其晶体结构与单晶硅相似,As原子的电子排布式为 。在AlN晶体中,每个Al原子与 个N原子相连,与同一个Al原子相连的N原子构成的空间构型为 。在四大晶体类型中,AlN属于 晶体。
(3)在极性分子NCl3中,N原子的化合物为―3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是
(填化学式)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com