
题目列表(包括答案和解析)
2.硅及其化合物在材料领域中的应用广泛。下列叙述不正确的是
A.硅单质可用来制造太阳能电池 B.二氧化硅是制造光导纤维的材料
C.石英( )可用来制作工艺品 D.硅单质是制造玻璃的主要原料
)可用来制作工艺品 D.硅单质是制造玻璃的主要原料
1.下列说法正确的是
A.氧化还原反应的本质是元素化合价发生变化
B.氧化反应和还原反应是同时发生的
C.物质所含元素化合价降低的反应是氧化反应
D.还原剂是一种能够得到电子的物质
31.(12分)看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)

(1)如果在虚线部分增加收集装置,上图中装置可用于实验室制取氨气,请回答以下问题:
①可以用 方法收集氨气,如果用烧瓶收集氨气,请用文字叙述如何检
验氨气己收集满 ;
②利用①中收集的氨气可以完成喷泉实验,是因为氨气具有 的物理性质;
③写出实验室制氨气的化学反应方程式 ;
(2)上图装置还可以用于完成某些固体物质受热分解的实验。请回答:
①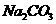 和
和 这两种物质中有一种可以用上图装置进行受热分解的实验。该物质受热分解的化学反应方程式为:
;
这两种物质中有一种可以用上图装置进行受热分解的实验。该物质受热分解的化学反应方程式为:
;
②为了验证①中该物质受热分解产生的所有气体产物,在虚线处应连接(表述时请指明
使用仪器,仪器中盛装的试剂和仪器的连接顺序)
;
③请提出一点有关实验过程中安全问题的建议:
;
④如果将12.6 g的该物质加热分解,加热一段时间后,测得剩余固体质量为9.5 g,则
已经分解的该物质的质量为 g。
第II卷(必修模块一综合能力测试题共50分)
30.(12分)回答下列关于铁元素及其化合物的知识:
(1)除去铁粉中混有的铝粉可以选用的试剂为 (填序号)。
A.稀盐酸 B,氢氧化钠溶液 C.浓硫酸 D.硝酸
需要进行的分离操作是 ,涉及的主要的离子反应方程式为
;
(2)向一支装有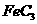 溶液的试管中滴加NaOH溶液,现象为
,
溶液的试管中滴加NaOH溶液,现象为
,
其中含铁元素的产物的化学式是 ;
(3)为了检验某未知溶液是否含有Fe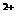 离子,两位同学分别设计了以下实验方案加以证明。
离子,两位同学分别设计了以下实验方案加以证明。
方案一:向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红
色,证明该未知溶液含有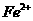 离子;
离子;
方案二:向另一支装有该未知溶液的试管中先滴加KSCN溶液,无现象,再通入氯气,
溶液变为红色,证明该未知溶液含有Fe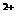 离子;
离子;
则请回答:①你认为哪个方案较为合理 ;
②写出Fe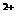 与氯气反应的离子方程式
;
与氯气反应的离子方程式
;
⑧实验室在保存含有Fe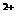 离子的溶液时,为了防止Fe
离子的溶液时,为了防止Fe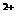 离子变质,经常向其中加入铁粉,
离子变质,经常向其中加入铁粉,
其原因是(用离子方程式表示) ;
(4)鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有Fe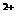 ,鲜榨的苹果汁在空气中会
,鲜榨的苹果汁在空气中会
由淡绿色的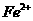 变为棕黄色的Fe
变为棕黄色的Fe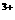 ,则这个变色的过程中Fe
,则这个变色的过程中Fe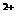 被 ;若在榨汁的
被 ;若在榨汁的
时候加入适量的维生素C,可有效防止这种现象的发生。这说明维生素C具有 。
A.氧化性 B.还原性 C.酸性 D.碱性
29.(8分)将一小块金属钠投入水中,发生反应的化学方程式为 ;
则:(1)可观察到的实验现象是 (填字母);
a.钠沉到水底 b.钠熔成小球
c.小球四处游动 d.向反应后的溶液中滴加酚酞试剂,溶液变为红色
(2)在实验室中,通常将金属钠保存在 中;
(3)氢氧化钠溶液吸收氯气的化学方程式为 。
28.(6分)(1)碳与浓硫酸在加热的条件下发生的反应为:
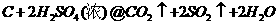 ,其中碳元素的化合价
(填
,其中碳元素的化合价
(填
“升高”或“降低”),被 (填“氧化”或“还原”,下同):碳单质作
剂,具有 性。
(2)将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后再加入适量浓硫酸,迅速
搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并产生刺激性气味的气
体。根据上述实验现象,说明浓硫酸具有 (填序号)。
①强氧化性 ②脱水性 ③吸水性 ④酸性
27.(4分)2mol 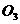 和3mol
和3mol 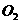 的质量(填“相等”、“不相等”或“无法判断”)
的质量(填“相等”、“不相等”或“无法判断”)
分子数之比为 ;所含氧原子的数目之比为 ;标准状况下。
体的体积之比为 。
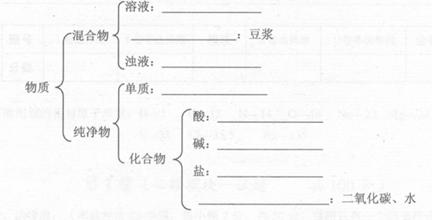
26.(8分)现有下列物质:A.豆浆;B.食盐水;C.铁;D.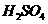 ; E.氢氧化钠固体
; E.氢氧化钠固体
F.纯碱;G.泥水;H.二氧化碳;I.水。请将它们的序号或所属类别填充到
下列横线上。
25.相同物质的量的镁和铝分别与足量的盐酸反应,所生成的氢气在标准状况下的体积比是
A.1:1 B.3:2 C.2:3 D.8:9
24.下列溶液中的 浓度与50mL l mol/L
浓度与50mL l mol/L  溶液中的
溶液中的 浓度相等的是
浓度相等的是
A.100mL 1 mol/L 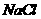 溶液 B.75mL l mol/L
溶液 B.75mL l mol/L  溶液
溶液
C.150mL 3mol/L KCl溶液 D.50mL 2mol/L 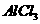 溶液
溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com