

题目列表(包括答案和解析)
22.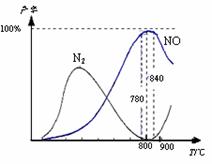 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如右图
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如右图
4NH3(g)+5O2(g) 4NO(g)+6H2O(g)+ 905 kJ ①
4NO(g)+6H2O(g)+ 905 kJ ①
4NH3(g)+3O2(g) 2N2(g)+6H2O(g)+ 1268 kJ ②
2N2(g)+6H2O(g)+ 1268 kJ ②
下列说法中正确的是
A.工业上氨催化氧化生成 NO时,温度应控制在780-840℃之间
B.工业上采用物料比n(O2)/n(NH3)在1.7-2.0,主要是为了提高反应速率
C.加压可提高NH3生成NO的转化率
D.N2氧化为NO的热化学方程式为:N2(g)+O2(g) 2NO(g)- 181.5 kJ
2NO(g)- 181.5 kJ
第Ⅱ卷(共84分)
21.CsICl2是一种碱金属的多卤化物,这类物质在化学反应中既可表现氧化性又可表现还原性,有关该物质的说法正确的是
A.Cs显+3价,I、Cl均显-1价 B.Cs显+1价,Cl显+1价,I显-1价
C.在CsICl2溶液中通入Cl2,有单质碘生成 D.在CsICl2溶液中通入SO2气体,有硫酸生成
20.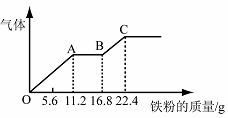 某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。
下列分析或结果错误的是
A.原混合酸中NO3-物质的量为0.2 mol
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+→3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.H2SO4浓度为5 mol·L-1
19.世界上60%的镁是从海水中提取的,其主要步骤如下:
①把贝壳制成石灰乳;②在海水中加入石灰乳,过滤,洗涤沉淀物;③将沉淀物与盐酸反应,结晶、过滤;④在氯化氢热气流中干燥晶体;⑤电解上述晶体的熔融物。
下列说法正确的是
A.镁元素在元素周期表中位于第三周期、ⅡA族
B.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净
C.在氯化氢热气流中干燥晶体的目的是加快干燥速度
D.步骤⑤也可以采用电解该晶体水溶液的方法
18. 下列化学实验事实及其解释都正确的是
下列化学实验事实及其解释都正确的是
A. 将饱和氯水滴到淀粉碘化钾试纸上出现如图现象,说明低浓度氯水能将I-氧化成I2,高浓度氯水能将I2进一步氧化成碘的化合物
B. 将过量CO2通入Ca(ClO)2溶液得澄清溶液,说明H2CO3的酸性比HClO弱
C. 用饱和Na2CO3溶液可将BaSO4转化为BaCO3,说明Ksp(BaSO4)>Ksp(BaCO3)
D. 铝箔在酒精灯火焰上加热熔化但不滴落,说明铝箔表面氧化铝膜熔点高
17.将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,生成的盐溶液中NaNO3的物质的量为(已知:2NO2+2NaOH→NaNO2+NaNO3+H2O ,NO+NO2+2NaOH→2NaNO2+H2O。)
A.0.2 mol B. 0.4 mol C.0.6 mol D. 0.8 mol
16.X、Y、Z、W是原子序数依次增大的短周期元素,且均在不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。下列说法错误的是
A.原子半径:Y>Z>W
B.YW3水溶液蒸干可得YW3固体
C.XW2熔点为-107℃,沸点为12.5℃,说明固态XW2为分子晶体
D.ZW2分子结构为 ,说明ZW2是极性分子
,说明ZW2是极性分子
15.将Na2O2、HCl和Al2O3起溶于一定量的水中,完全反应后测得所得溶液中只含有Na+、AlO2一、Cl一 (不考虑AlO2一的水解和H2O的电离),则Na2O2、HCl、Al2O3的物质的量之比不可能是
A.2∶2∶1 B.3∶3∶1 C.3∶4∶1 D.4∶6∶1
14.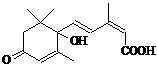 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结构如右图,下列关于该物质的说法正确的是
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结构如右图,下列关于该物质的说法正确的是
A.其分子式为C15H22O4
B.1 mol该物质与NaOH溶液反应,最多消耗2 mol NaOH
C.既能发生加聚反应,又能发生缩聚反应
D.既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色
13.设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的有
① 0.25molNa2O2中含有的阴离子数为0.5NA
② 7.5gSiO2晶体中含有的硅氧键数为0.5NA
③ 1 mol α-氨基乙酸(甘氨酸)分子中存在10 NA对共用电子
④ 250mL2mol/L的氨水中含有NH3·H2O的分子数为0.5NA
⑤ 3.0 g淀粉和葡萄糖混合物中共含碳原子数为0.1NA
⑥ 18g D2O(重水)完全电解,转移NA个电子
⑦ 标准状况下,2.24L CHCl3含有的分子数为0.1NA
⑧ 电解精炼铜时,当阳极溶解32 g铜时,转移的电子数为NA个
A.2个 B.3个 C.4个 D.5个
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com