
题目列表(包括答案和解析)
5.A、B、C、D、E、F为短周期六种元素,原子序数依次增大,其中A与E同主族且能形成离子化合物EA,B与F同主族,E与F同周期。D的核电荷数是B的最外层电子数2倍,单质F是一种重要的半导体材料。则下列推断中不正确的是
A.由A、C、D三种元素组成的化合物可以是离子化合物
B.F与D形成的化合物熔点高,可以与某种酸反应
C.原子半径由大到小的顺序是:E>F>C>D
D.五种元素中最高价氧化物对应的水化物酸性最强的是D
4.下列物质中,既能与NaOH溶液反应,又能与盐酸反应,还能发生水解反应的是
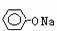 ① AlCl3 ② NaHSO4
③ (NH4)2CO3 ④
⑤ NaHCO3
① AlCl3 ② NaHSO4
③ (NH4)2CO3 ④
⑤ NaHCO3
A.① ④ ⑤ B.③ ⑤ C.④ ⑤ D.全部
3.NA代表阿伏加德罗常数,下列说法正确的是
A.1 L 0.1 mol/L Na2CO3溶液中CO32-和HCO3-总数为0.1 NA
B.22.4L氢气和4g氦气均含有NA个分子
C.含2 NA共价键的CnH2n+2分子的物质的量为2/(3n+1)mol
D.0.1mol铁与0.1molC12充分反应,转移的电子数为0.3NA
2. 在陆地生态系统研究中,2H、13C、15N、18O、34S等常用做环境分析指示物。下列说法正确的是
A. 34S原子核内中子数为16
B.在相同条件下1H216O比1H218O更易挥发
C.13C和15N原子核内的质子数相差2
D.2H+的酸性比1H+的酸性更强
1.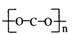 下列有关新技术的开发应用叙述正确的是
下列有关新技术的开发应用叙述正确的是
A.我国首创用CO2合成可降解的塑料聚二氧化碳,该塑料的结构简式为
B.有人建议用液氨作为清洁的汽车燃料,燃烧的最终的产物为氮气和水
C.“纳米泡沫”被称为第五形态的单质碳形似海绵并有磁性,与石墨化学性质完全不同
D.超临界CO2可从天然动植物中萃取、分离生物活性成分,它与一氧化碳互为同素异形体
16.(1)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸 Ki = 1.75×10-5
碳酸 Ki 1= 4.30×10-7 Ki 2 = 5.61×10-11
亚硫酸 Ki 1= 1.54×10-2 Ki 2 = 1.02×10-7
① 写出碳酸的第一级电离平衡常数表达式:Ki = _________________
② 在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:_____>_____>_____
③ 若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是______(填序号)
A. c(CH3COO-) B. c(H+) C. Kw D. 醋酸电离平衡常数 E. 醋酸的电离度
 (2)一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数
(2)一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数
Ksp=cm(An+)×cn(Bm-),称为难溶电解质的离子积。在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。已知有关物质的颜色和溶度积如下:
|
物质 |
AgCl |
AgI |
Ag2S |
|
颜色 |
白 |
黄 |
黑 |
|
KSP(25℃) |
1.8×10-10 |
1.5×10-16 |
1.8×10-50 |
下列叙述不正确的是
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
C.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同
D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同
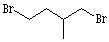
15.环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂)
|
结构简式 |
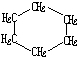 |
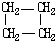 |
Br-CH2-CH2-CH(CH3)-CH2-Br |
|
键线式 |
 (环己烷) (环己烷) |
 (环丁烷) (环丁烷) |
 |
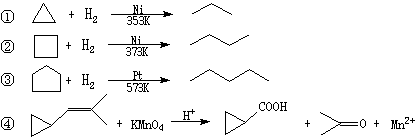
回答下列问题:
(1)环烷烃与 是同分异构体。
(2)从反应①-③可以看出,最容易发生开环加成反应的环烷烃是 (填名称),判断依据为 。
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为 (不需注明反应条件)
(4)写出鉴别环丙烷与丙烯的一种方法,试剂 ;现象与结论 。
14.第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
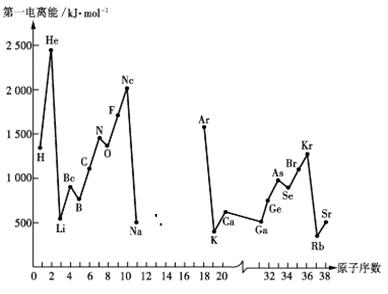
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na--Ar元素中,Al的第一电离能的大小(最小)范围为 <Al< (填元素符号)。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是______________;
(3)上图中第一电离能最小的元素在周期表中的位置是________________________;
(4)根据对角线规则,Be、Al元素最高氧化物水化物的性质相似,它们都具有 性,其中Be(OH)2显示这种性质的离子方程式是:________________________ ___、______________________________________。
(5)单质C不可能具有的性质是
A.具有良好的导电性
B.熔沸点很高
C.硬度较小
D.易与Br单质反应,形成的化合物分子是极性分子。
13.随着生活水平的提高,人们越来越关注自身的健康。以下是探讨化学物质与人体健康的有关问题:
(1)发育出现障碍,患营养缺乏症,这主要是由于摄取_________(填“蛋白质”、“脂肪”或“维生素”)不足引起的。
(2)微量元素与人体健康密切相关,若膳食结构不合理,摄入某种微量元素不足,就会引起某些疾病,例如身材矮小,腰背弯曲可能是由于缺________,_________元素是合成甲状腺激素的重要原料;人体铁元素摄入量不足可能会导致_________。
(3)人体摄入过多的食物时,会引起胃酸分泌过多,胃酸的pH下降,使人体感到不适,此时应服用消酸剂,双羟基铝酸钠就是一种常用的消酸剂,其化学式为NaAl(OH)2CO3,由于Al3+在人体内难以代谢,含量过高可导致老年痴呆症等疾病,为防止人体摄入过量铝元素,请提一条合理的建议___________________________________ 。
12.碱性锌锰电池比普通锌锰电池性能好,是民用电池的升级换代产品之一。碱性锌锰电池的电解质是KOH,其总反应式为 Zn + 2MnO2 + 2H2O = 2MnOOH + Zn(OH)2下列说法错误的是( )
A.电池工作时锌作负极发生氧化反应
B.电池正极反应为:2MnO2 + 2H2O+2e- = 2MnOOH + 2OH-
C.碱性锌锰电池属于二次电池
D.外电路每通过0.2mole-,锌的质量理论上减少6.5g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com