
题目列表(包括答案和解析)
32、(10分 ) A、B、D、E是周期表中前20号元素,它们的原子序数依次增大。EA2与水反应产生可燃性气体和白色浆状物,向该浆状物中通入AB2气体可得另一白色不溶物。B、D同主族,D的阴离子与E的阳离子具有相同的核外电子排布。请回答:
(1)写出EA2电子式 已知AD2与AB2的结构相似,AD2的结构式为
(2)EA2与水反应化学方程式
(3)镁条在AB2中燃烧的现象______________________________________
(4)将D单质放入浓HNO3中加热,生成红棕色气体和一种强酸,化学反应方程式为
(5)A可形成二元弱酸H2A2O4。0.1 molH2A2O4与100 mL 2 mol/L的KOH溶液反应后,溶液中的离子浓度由大到小的排列顺序是
31、(7分 ) 焊接金属时常用的焊接液为氯化铵,其作用是消除焊接金属表面的铁锈。
(1)配平化学方程式:
□Fe2O3 +□NH4Cl→□Fe+□FeCl3+□N2↑+□H2O
(2)有同学认为该反应产物中不可能有Fe生成,其原因是Fe会与Fe3+发生氧化还原反应生成Fe2+;有同学观察反应方程式后认为反应完全可以进行,因为
(3)生产中也可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,
溶液中发生的化合反应的化学方程式______________________________ 。
(4)下列哪个装置可防止铁棒被腐蚀_____________ 。w.&w.^w.k.s.5*u.c.#o
w.&w.^w.k.s.5*g src="file:///H:\zip_cooco_htm\\files\down\test\2\409\386409\1010jiajiao_0.files\image028.jpg">
(5)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:
 请回答:若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为________________mol
请回答:若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为________________mol
30、关于下列四套装置的叙述正确的是( )
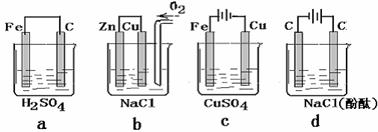
A a 装置中电流由Fe棒经导线流向C(石墨)棒;电解质溶液中的H+向C(石墨)一端移动
B b装置中反应的电极方程式分别为:负极:Zn-2e-=Zn2+ 正极:O2+2H2O+4e-=4OH-
C c装置中通电一段时间后,铜电极质量减轻,铁电极上附着有一层红色的铜;当电路上通过2mol电子时,两电极(原质量相等)的质量的差值为120克
D通电一段时间后两电极上析出气体的成分不同但物质的量相同, d 装置中右侧的C(石墨)电极周围的电解质溶液先变红色,
Ⅱ卷(非选择题 w.&w.^w.k.s.5*u.c.#o共60分)
29、下列化合物中,既有离子键,又有非极性共价键的是 ( )
A.CaC2 B.SiC C.H2O D.CH3COONa
28.某浓度的硝酸与过量铁粉反应时生成了4.48LN2O气体(标准状况下),若改与铝反应(生成NO气体),则最后可溶解的铝的质量是
A.13.5g B.9g C.27g D.8.9g
27、A、B两种烃,它们的碳元素质量分数相同,有关A、B的叙述中正确的是
A.A和B不可能是烷烃
B.A和B不可能互为同系物
C.A和B化学性质一定相似
D.A和B分子中C、H原子个数比不可能为1∶3
25、下列各组离子在溶液中能大量共存,当溶液呈强酸性时,有气体产生;而当溶液呈强碱性时,又能生成沉淀。该组离子可能是
A.Na+、Cu2+、NO3-、CO32- B.NH4+、K+、Cl-、HCO3-
C.Mg2+、NH4+、SO42-、CH3COO- D.Fe2+、Na+、SO42-、NO3-
24、 右图是关于反应A2(g)+3B2(g)
右图是关于反应A2(g)+3B2(g)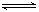 2C(g);△H <0的平衡移动图象,影响平衡移动的原因可能是(
)
2C(g);△H <0的平衡移动图象,影响平衡移动的原因可能是(
)
A.升高温度,同时加压
B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度
D.增大反应物浓度,同时使用催化剂
23、下列有关晶体的说法正确的是(w.&w.^w.k.s.5*u.c.#o )
A.右图是铜的某种氧化物的晶胞结构示意图,则其化学式为CuO
B.氢键一定比分子间作用力强
C.沸点:CsCl>NaCl>H2O>HCl>HF
D.固体不导电,熔融状态下和溶于水都能导电的固体不可能是分子晶体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com