
题目列表(包括答案和解析)
17.(11分)
实验室制取氯气方法很多,通常有如下三种:
(1)用二氧化锰与浓盐酸共热制取氯气。如果将过量二氧化锰与20 mL 12 mol/L的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。产生该结果的主要原因是:① ,② 。
(2)高锰酸钾与浓盐酸反应可制取氯气,其反应的化学方程式为:
。若消耗0.1 mol氧化剂,则被氧化的还原剂的物质的量为 mol。
 (3)氯酸钾晶体与浓盐酸反应可用于制取氯气,该反应中
(3)氯酸钾晶体与浓盐酸反应可用于制取氯气,该反应中
氧化产物和还原产物的物质的量之比为 。
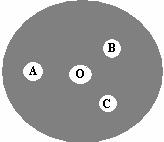
现按如下操作进行有关氯气的制备及性质实验:在一片下衬白纸的圆形玻璃片上(如右图),A点滴一滴0.1 mol/L KI溶液,B点滴一滴FeSO4(含KSCN)溶液,C点滴一滴NaOH(含酚酞)溶液,O点放少量KClO3晶体。向KClO3晶体滴加一滴浓盐酸,立即用表面皿盖好。试回答下列问题:
①A点反应的离子方程式为 ;
②B点的现象为 ;
③C点的溶液由红色变为无色,是因为中和褪色还是漂白而褪色,请你设计实验证明之。 。
16.在40 mL稀硫酸中加入1.6 g氧化铁后溶液仍呈酸性,再加入5 g 铁粉后,滴入硫氰化钾溶液,没有红色出现,此时溶液尚残留铁粉1.64 g,原硫酸溶液的物质的量浓度是 A.4 mol/L B.3.5 mol/L C.3 mol/L D.2 mol/L
第Ⅱ卷(非选择题 共60分)
用黑色墨水的签字笔或钢笔直接答在答题卡上每题对应答题区域内,答在试题卷上无效。
15.类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
|
|
已 知 |
类 推 |
|
A |
将Fe加入CuSO4溶液中 Fe+Cu2+=Cu+Fe2+ |
将Na加入到CuSO4溶液中 2Na+Cu2+=Cu+2Na+ |
|
B |
稀硫酸与Ba(OH)2溶液反应至中性 2H++SO 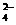 +Ba2++2OH-=BaSO4↓+2H2O +Ba2++2OH-=BaSO4↓+2H2O |
NaHSO4溶液与Ba(OH)2溶液反应至中性 2H++ SO 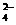 +Ba2++2OH-=BaSO4↓+2H2O +Ba2++2OH-=BaSO4↓+2H2O |
|
C |
铁和氯气反应 2Fe+3Cl2  2FeCl3 2FeCl3 |
铁和碘单质反应 2Fe +3I2  2FeI3 2FeI3 |
|
D |
向Ca(ClO)2溶液中通入少量CO2 Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
向Ca(ClO)2溶液中通入少量SO2 Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
14.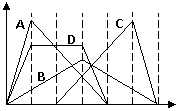 右图中横坐标为加入反应物的物质的量,纵坐标为产生沉
右图中横坐标为加入反应物的物质的量,纵坐标为产生沉
淀的物质的量。下列选项编号对应的曲线编号错误的是
A.向NaAlO2溶液中逐渐滴入HCl至过量
B.向澄清石灰水中通入CO2至过量
C.向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量
D.向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至过量
13.下列实验中所选用的仪器或操作合理的是
A. 用托盘天平称量5.85 g氯化钠晶体
B. 用湿润pH试纸测定某H2SO4溶液pH
C. 可用酸式滴定管量取25.00 mL高锰酸钾溶液
D.用瓷坩埚灼烧碳酸钠晶体
12.W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7∶17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
A.氢化物的稳定性:HnX>HnW,是因为HnX 分子间存在氢键
B.原子序数:W>Y>Z>X
C.离子的还原性:X>W
D.原子半径:Y>Z>X
11.某无色溶液中含有:①Na+、②Ba2+、③C1-、④Br-、⑤SO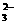 、⑥SO
、⑥SO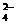 离子中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
离子中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
|
步骤 |
操作 |
现象 |
|
① |
用pH试纸检验 |
溶液的pH大于7 |
|
② |
向溶液中滴中氯水,再加入CC14振荡,静置 |
CC14层呈橙色 |
|
③ |
向②所得溶液中加入Ba(NO3)2溶液和稀HNO3 |
有白色沉淀产生 |
|
④ |
过滤,向滤液中加入AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是
A.肯定含有离子的①④⑤ B.肯定没有的离子是②⑤
C.可能含有的离子是①②⑥ D.不能确定的离子是①③⑥
10.将一定质量的铜粉加入到100 mL某浓度的稀硝酸中,充分反应后,容器中剩有m1 g铜粉,此时共收集到NO气体448 mL(标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止容器剩有铜粉m2 g,则(m1-m2)为
A.5.76 B.2.88 C.1.92 D.0
9.膳食纤维具有突出的保健功能,是人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如右图所示。下列有关芥子醇的说法正确的是
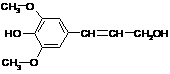 A.芥子醇的分子式是C11H14O4,属于芳香烃
A.芥子醇的分子式是C11H14O4,属于芳香烃
B.芥子醇分子中所有碳原子不可能在同一平面
C.芥子醇不能使酸性KMnO4溶液褪色
D.芥子醇可以发生氧化反应、取代反应、加成反应
8.下列说法正确的是
A.常温下0.1 mol/L的下列溶液①NH4Al(SO4)2、②NH4Cl、③NH3·H2O、④CH3COONH4溶液中c(NH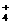 )由大到小的顺序是:②>①>④>③
)由大到小的顺序是:②>①>④>③
B.常温下0.4 mol/L HB溶液 和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则溶液中粒子浓度大小顺序为:c(HB)>c(Na+)>c(B-)>c(H+)>c(OH-)
C.pH=2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,相同温度时,四种溶液中由水电离的c(H+)相等
D.用惰性电极电解足量的CuSO4溶液一段时间,加入一定量的Cu(OH)2可以恢复至原来的浓度和体积
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com