
题目列表(包括答案和解析)
30.(16分)
铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。有关含铬化合物的相互转化关系如下

回答下列问题:
(1)上述反应中需用氧化剂的是 (填编号)。
(2)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应和溶液中进行的反应的离子方程式:阳 极 阴 极
溶液中
(3)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式 。
(4)已知Ag2CrO4和AgCl的Ksp分别为9.0×10-12、1.56×10-10,向含有相同浓度的Na2CrO4和NaCl的混合溶液中逐滴加入硝酸银溶液,首先生成的沉淀是 。
(5)要将Fe3+溶液中的杂质离子Cr3+除去,可加入过量NaOH溶液,过滤后再用酸溶解。写出有关的离子方程式 。
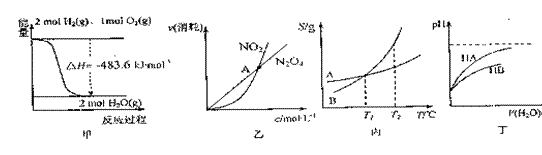 22.下列关于图4的各项叙述正确的是:
22.下列关于图4的各项叙述正确的是:
A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ·mol-1
 B.乙表示恒温恒容条件下发生的可逆反应2NO2(g) N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中A点对应的状态为化学平衡状态
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g) N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中A点对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数仍为B=A
D.丁表示常温下,稀释HA、HB两种酸的浓溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
23.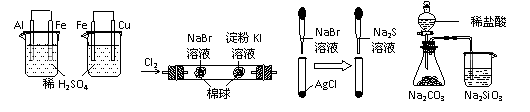 根据下列实验现象,所得结论正确的是:
根据下列实验现象,所得结论正确的是:
A B C D
|
实
验 |
实验现象 |
结 论 |
|
A |
左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Fe>Cu |
|
B |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
|
C |
白色固体先变为淡黄色,后变为黑色 |
溶解性 :AgCl>AgBr>Ag2S |
|
D |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:Cl>C>Si |
12.下列叙述正确的是:
A.将二氧化硫气体通入浅黄色的溴水中使其颜色褪去,说明二氧化硫具有漂白性
B. SiO2为碳族元素的非金属氧化物为酸性氧化物,故不能与任何酸发生化学反应
C.用砂纸打磨过的铝箔放在酒精灯焰上不燃烧,说明铝不易与O2反应
D.向装有NaHCO3溶液的两支试管中各滴入CaCl2和MgCl2的饱和溶液,后者有沉淀呈现
11.短周期元素A、B、C原子序数依次递增,它们的原子的最外层电子数之和为10。A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数。下列叙述正确的是:
A.原子半径A<B<C B.A的氢化物的稳定性小于C的氢化物
C.B的氧化物的熔点比A的氧化物高 D.A与C可形成离子化合物
10.有关下图所示化合物的说法不正确的是:
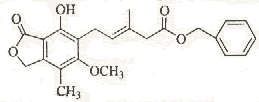
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1 mol该化合物最多可以与3 molNaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
9.在下述条件下,一定能大量共存的离子组是: A.无色透明的水溶液中:K+、Ba2+、I-、MnO4- B.含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ C.c(HCO3-)=0.1mol·L-1的溶液中:Na+、K+、CO32-、Br- D.强碱性溶液中:ClO-、S2-、HSO3-、Na+
7.某合作学习小组讨论辨析:①漂白粉和酸雨都是混合物②煤和石油都是可再生能源 ③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 ④不锈钢和目前流通的硬币都是合金 ⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 ⑥豆浆和雾都是胶体。上述说法正确的是:
A.①②④ B.①⑤⑥ C.①③④⑥ D.②③④⑤
102.该反应为吸热反应,所以反应物的总能量要低于生成物的总能量。
(2)请提出可提高其反应速率且增大NH3生成量的建议:升高温度,增大反应物N2的浓度,不断移出生成物脱离反应体系。
解释:该反应正反应是吸热反应,升高温度,使化学平衡向正反应方向移动,从而增大NH3生成量,升高温度也能提高反应速率;增大反应N2浓度,加快反应速率,并使化学平衡向右移动;不断移出生成物脱离反应体系,使平衡向右移动,增大NH3生成量。
(3) ①该条件下N2的平衡转化率:66.7%
②该条件下反应2NH3(g) ==== N2(g) +3H2(g)的平衡常数为0.005
解释:由三行式法计算可知,起始时,c(N2)=0.3mol/l.平衡时,c(N2)=0.1mol/l; c(H2)=0.2mol/l; c(NH3)=0.4mol/l 。
①所以N2的平衡转化率=(0.3-0.1)/0.3*100%=66.7%
②反应2NH3(g) ==== N2(g) +3H2(g)的平衡常数K= c(N2)* c(H2)^3/ c(NH3)^2=0.005
9.
⑴78 100
⑵取滤液少许,加入NaOH,加热,生成的气体能使润湿的红色石蕊试纸变蓝(合理即给分)
⑶Al(OH)3 Al2O3 Fe2O3 ⑷K2SO4 (NH4)2SO4
⑸BaCl2 过滤 洗涤 干燥 ⑹
(1)BD(4分)
(2)一定有NO3-、Al3+、SO42-(2分);一定无Fe3+、Ba2+、HCO3-(2分)
(3)②3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O(4分)
③Al3++3NH3·H2O=Al(OH)3↓+3NH4+(4分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com