
题目列表(包括答案和解析)
21.从下列实验事实所引出的相应结论正确的是( )
|
选项 |
实验事实 |
结论 |
|
A |
其它条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越短 |
当其它条件不变时,增大反应物浓度化学反应速率加快 |
|
B |
在化学反应前后,催化剂的质量和化学性质都没有发生改变 |
催化剂一定不参与化学反应 |
|
C |
在常温下N2很难与金属化合 |
氮元素的非金属性很弱 |
|
D |
NaOH晶体不能导电 |
NaOH是非电解质 |
20.下列判断正确的是( )
A. 冰熔化时,分子内氢键被破坏
B. 白磷与红磷在一定条件下互相转化,发生的是物理变化
C. 酸性氧化物在固态时,一定是分子晶体
D. 三氧化硫晶体熔化时,一定没有破坏化学键
19.在20世纪90年代末期,科学家发现并证明碳有新的单质形态C60存在。后来人们又相继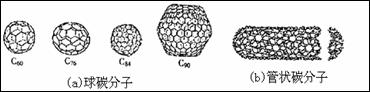 得到了C70、C76、C84、C90、C94等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰富了碳元素单质的家族。下列有关碳元素单质的说法错误的是( )
得到了C70、C76、C84、C90、C94等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰富了碳元素单质的家族。下列有关碳元素单质的说法错误的是( )
A.金刚石和石墨的熔点肯定要比C60高
B.熔点比较:C60<C70<C90
C.球碳分子、管状碳分子、洋葱状碳分子都是碳的同素异形体
D.金刚石、石墨晶体为非分子形式的粒子存在,属于原子晶体;C60、C70、管状碳分子和洋葱状碳分子为分子形式的粒子存在,属于分子晶体
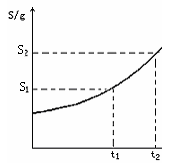
18.摩尔质量为Mg/mol的某物质(不含结晶水)的溶解度曲线如下图,现有t2℃300g该物质的溶液,蒸发掉50g水后,恢复到原温度,溶液恰好达到饱和,此饱和溶液的密度为ρg/mL,则下列说法不正确的是( )
A.该饱和溶液的质量分数为: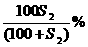
B.该饱和溶液的物质的量浓度为: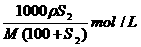
C.将该饱和溶液降温至t1℃时,析出的晶体的质量为: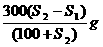
D.原溶液的质量分数为: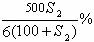
17.下列叙述正确的是( )
A.因为液态氟化氢中存在氢健,所以其分子比氯化氢更稳定
B.由碳氮原子形成的某种化合物比金刚石还坚硬,其主要原因是碳氮键比碳碳键更短
C.S8和NO2 都是共价化合物,NH4Cl和CaC2都是离子化合物
D.若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数有可能为m+10
16.向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)  bZ(g);△H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。下列说法正确的是( )
bZ(g);△H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。下列说法正确的是( )
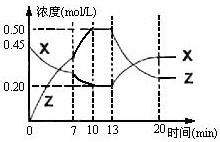
A.用X表示0~10min内该反应的平均速率为0.025 mol/(L·min)
B.根据上图可求得方程式中a:b=2:1
C.0-10min 容器内气体的压强逐渐增大
D.第13min时曲线变化的原因可能是增加了Z的量
15.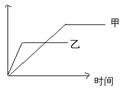 可用右侧示意图表示的是( )
可用右侧示意图表示的是( )
|
|
反应 |
纵坐标 |
甲 |
乙 |
|
A |
等质量钾、钠分别与水反应 |
H2质量 |
钠 |
钾 |
|
B |
相同质量氨气,在同一容器中 2NH3  N2+3H2;△H>0 N2+3H2;△H>0 |
氨气的转化率 |
400℃ |
500℃ |
|
C |
体积比1:3的N2、H2,在体积可变的恒压容器中N2+3H2 2NH3; 2NH3; |
氨气的浓度 |
活性高的催化剂 |
活性一般的催化剂 |
|
D |
2molSO2与1molO2,在相同温度下2 SO2+
O2 2 SO3 2 SO3 |
SO3的物质的量 |
10个大气压 |
2个大气压 |
14.今有两种正盐的稀溶液,分别是amol/LNaX溶液和bmol/L NaY溶液,下列说法不正确的是( )
A.若a=b,pH(NaX)>pH(NaY),则相同浓度时,酸性:HX>HY
B.若a=b,并测得c(X-)=c(Y-)+c(HY),则HX是强酸,HY是弱酸
C.若a>b,测得c(X‑)=c(Y-),则可推出溶液中c(HX) > c(HY),且相同浓度时,酸性HX<HY
D.若两溶液等体积混合,测得c(X-)+c(Y-)+c(HY) +c(HX)=0.1mol/L,则可推出a=b=0.1mol/L
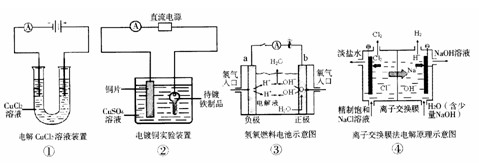
13.下列关于下列各图的说法,正确的是( )
A.①装置中阴极处产生的气体能够使湿润淀粉KI试纸变蓝
B.②装置中待镀铁制品应与电源正极相连
C.③装置中电子由b极流向a极
D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
12.有浓度均为0.1mol/L①醋酸溶液②氯化铵溶液③硫酸溶液各25mL。下列说法正确的是( )
A.三种溶液pH大小的顺序是①>②>③
B.若将三种溶液稀释相同倍数,pH变化最大的是①
C.三种溶液中由水电离产生的氢离子浓度大小顺序是②>①>③
D.若分别加入25mL 0.1mol/L的氢氧化钠溶液后,pH最大的是①
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com