
题目列表(包括答案和解析)
8.发生下列转变时,对应的方程式正确的是
A.碳酸钡粉末中加入稀硫酸:BaCO3+2H+=Ba2++CO2↑+H2O
B.用铂电极电解氯化镁溶液:2Cl-+2H2O=Cl2↑+H2↑+2OH-
C.过量的铁粉与浓硝酸反应:Fe+4H++2NO3-=Fe2++2NO2↑+2H2O
D.NaCO3溶液中,HCO3-的电离方程式为:HCO3-+H2O H3O++CO32-
H3O++CO32-
7. 在由水电离产生的c(H+)=1×10-13mol/L的溶液中,一定能大量共存的离子组是
①K+、Cl-、NO3-、HCO3-; ②K+、Fe2+、I-、NO3-; ③Na+、Cl-、NO3-、SO42-
④Na+、Al3+、Cl-、CO32-; ⑤K+、Ba2+、Cl-、NO3-。
A.①③ B.③⑤ C.③④ D.②⑤
6.
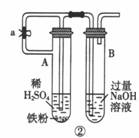
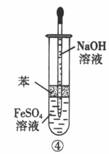
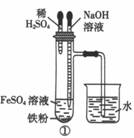 下列各图示中的实验能较长时间看到Fe(OH)2白色沉淀的是
下列各图示中的实验能较长时间看到Fe(OH)2白色沉淀的是
A.只有①② B.只有②③ C.只有③④ D.①②③④
5.若电能与化学能的转化装置(电解池或原电池)中发生的总反应离子方程式Cu+2H+=Cu2++H2↑,则关于该装置的有关说法正确的是
A.该装置可能是原电池,也可能电解池
B.该装置只能是原电池,且电解质溶液为硝酸
C.该装置只能是电解池,电解质溶液不可能是盐酸
D.该装置只能是电解池,且金属铜为该电解池的阳极
4.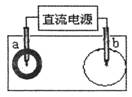 取一张用饱和NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现某电极与试纸接触处出现一个双色同心圆,内圆为白色,外圆呈浅红色。则下列说法错误的是
取一张用饱和NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现某电极与试纸接触处出现一个双色同心圆,内圆为白色,外圆呈浅红色。则下列说法错误的是
A.b电极是阴极 B.a电极与电源的正极相连接
C.电解过程中,水是氧化剂 D.b电极附近溶液的pH变小
3.溶液、胶体和浊液这三种分散系的本质区别是
A.是否是大量分子或离子的集合体 B.分散质粒子直径大小
C.是否能通过滤纸或半透膜 D.是否均一、稳定、透明
2.
 如图是第29届奥林匹克运动会纪念币金、银币的背面。下列关于该纪念币的说法不正确的是
如图是第29届奥林匹克运动会纪念币金、银币的背面。下列关于该纪念币的说法不正确的是
A.该纪念币为纯金、纯银制成
B.该纪念币在国内具有流通性,但不是其主要功能
C.流通硬币应具有一定的硬度、耐磨损和抗腐蚀性
D.我国发行的第五套人民币中的一元硬币材料是钢芯镀镍合金,其材料的实际价值略低于其面值
1.生活中遇到的某些问题,常常涉及化学知识,下列各项叙述正确的是
A.“加碘盐”“高钙牛奶”“富硒营养吕”等食品中的碘、钙、硒是指单质
B.家庭可以用明矾将自来水净化成纯净水饮用保障身体健康
C.医疗上进行胃部造影前,患者服用的“钡餐”是硫酸钡悬浊液
D.红砖中铁元素的含量比青砖中铁元素的含量高
22.(8分)在电解食盐水之前,需要提纯食盐水.(1)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是 ( ) ①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的碳酸钠溶液 ⑤加过量的氯化钡溶液 A、①④②⑤③ B、④①②⑤③ C、②⑤④①③ D、⑤②④③①
(2)写出电解食盐水的离子方程式 ;
其产生的一种有毒气体在常温下用NaOH溶液吸收,写出相关的化学方程
式 ,当消耗NaOH 80克时,转移的电子数为 个。
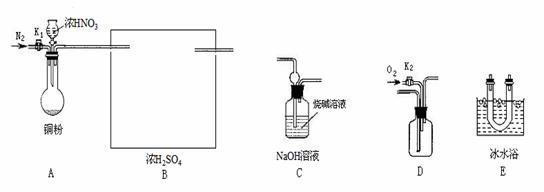
21.(13分)某校研究性学习小组选择使用下列仪器和药品,验证铜和适量浓硝酸反应除生成NO2气体外,还生成少量的NO。(实验中使用的N2和O2的用量可自由控制)。
 已知:①NO + NO2 +
2OH-= 2NO2-+ H2O ②气体液化温度 NO2 21℃ NO -152
已知:①NO + NO2 +
2OH-= 2NO2-+ H2O ②气体液化温度 NO2 21℃ NO -152
请回答:
(1)装置B的作用是 ,在下图方框内画出B装置。
(2)写出装置的连接顺序(填字母),A接B接 。
(3)实验开始前要先打开A装置中的活塞K1,持续通一段时间氮气后再关闭活塞K1,目的是 。A装置中的反应停止后,打开D中的活塞K2,并通入氧气,若反应中确有NO产生,则D中出现的现象是 。
(4)如果O2过量,则装置C中发生反应的离子方程式 。
(5)若铜粉中混入了少量银,已知铜粉质量为a g,反应后固体完全溶解,要测定铜粉中铜的质量分数,利用A装置中反应后的溶液进行简单的实验操作,就可以达到实验目的。试简述实验方案_________________ __ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com