
题目列表(包括答案和解析)
6.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染。下列做法不符合绿色化学理念的是
A.研制水溶剂涂料替代有机溶剂涂料
B.用可降解塑料生产包装盒或快餐盒
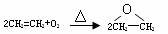 C.用反应: 制备环氧乙烷
C.用反应: 制备环氧乙烷
D.用反应:Cu +2H2SO4(浓)→CuSO4+SO2↑+2H2O 制备硫酸铜
5.化学家将研究气体与固体(或液体)在界面上所发生的物理化学现象的科学称为表面化学。对下列现象的研究不属于表面化学范畴的是
A.铁在潮湿的空气中生锈 B.电解饱和食盐水时两电极上的反应
C.氯化银在水中的溶解平衡 D.氮气与氢气在铁触媒作用下化合
4.下图表示的是某物质所发生的
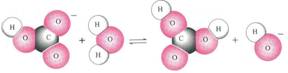
A.取代反应 B.水解反应 C.中和反应 D.电离过程
3.下列物质中,导电性最差的是
A.氯化钾晶体 B. 石墨棒 C. 盐酸溶液 D. 熔融氢氧化钠
2.下列化学用语或模型图表示正确的是
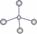 A.甲烷的球棍模型:
B.S2-的最外层核外电子排布式为:3S23P4
A.甲烷的球棍模型:
B.S2-的最外层核外电子排布式为:3S23P4
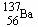 C.乙炔的最简式: CH≡CH D.质子数为56,质量数为137的钡原子:
C.乙炔的最简式: CH≡CH D.质子数为56,质量数为137的钡原子:
1.化学与生活、社会密切相关。下列说法正确的是
A.用NaOH溶液雕刻工艺玻璃上的纹饰
B.Na2O可用于呼吸面具中作为氧气的来源
C.工业上硝酸可用于制化肥、农药、炸药和染料等
D.向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量
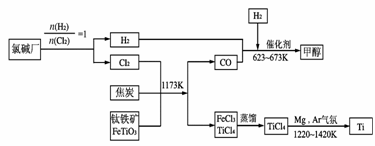
28.(10分)金属钛被称为铁和铝之后崛起的第三金属,它是空间技术、航
 海、化工、医疗上不可缺少
海、化工、医疗上不可缺少
的材料。为了提高资源的利
用率,减少环境污染,可将
氯碱厂、炼钛厂和甲醇厂组
成产业链,其关系如下图所
示。请回答下列问题:
(1)写出钛铁矿经氯化法得到四氯化钛的化学方程式_________________________。
(2)TiCl4暴露在潮湿空气中冒白烟,白烟主要为白色的二氧化钛的水合物H2TiO3,试写出该反应的化学方程式:_________________________________。
(3)已知:①Mg(s)+Cl2(g)=MgCl2(s) △H=一641 kJ·mol-1
②1/2Ti(s)+Cl2(g)=1/2TiCl4(l) △H=一385 kJ·mol-1
则Mg 与TiCl4反应的热化学方程式为 ,
该反应在氩气氛中进行的理由是 。
(4)在上述产业链中,合成96 t 甲醇理论上需额外补充H2 t (不考虑生
产过程中物质的任何损失)。
贵州省清华实验学校2010届高三下学期3月月考
27.(10 分 )糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志。长期摄入高热量食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖 ( C6H12O6)。下列说法正确的是 ( 错选倒扣分 )
A.葡萄糖属于碳水化合物,分子可表示为 C6(H2O)6,则每个葡萄糖分子中含6个H2O
B.糖尿病人尿糖也高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
C.葡萄糖可用于制镜工业
D.淀粉水解的最终产物是葡萄糖
(2)木糖醇 [ CH2OH(CHOH)3CH2OH]是一种甜味剂,糖尿病人食用后不会升高血糖。请预测木糖醇的一种化学性质 ( 写反应方程式 ):
(3)糖尿病人不可饮酒,酒精在肝脏内可被转化成有机物 A。A 的实验结果如下:
I、通过样品的质谱测得 A 的相对分子质量为 60
II、核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值 (信号),根据 峰值 (信号) 可以确定分子中氢原子的种类和数目。例如:乙醇 (CH3CH2OH) 有三种氢原子 (图1)。经测定,有机物 A 的核磁共振氢谱示意图如图2
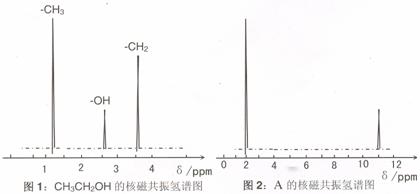
III、将 A 溶于水,滴入石器试液,发现溶液变红。
试推导写出 A 的结构简式为 。
(4)糖尿病人宜多吃蔬菜和豆类食品。蔬菜中富含纤维素,豆类食品中富含蛋白质。下列说法错误的是: (填序号,错选倒扣分)
A.蛋白质都属于天然有机高分子化合物,蛋白质都不溶于水
B.用灼烧闻气味的方法可以区别合成纤维和羊毛
C.人体内不含纤维素水解酶,人不能消化纤维素,因此蔬菜中的纤维素对人没有用处
D.紫外线、医用酒精能杀菌消毒,是因为使细菌的蛋白质变性
E.用天然彩棉制成贴身衣物可减少染料对人体的副作用
(5)香蕉属于高糖水果,糖尿病人不宜食用。乙烯是香蕉的催熟剂,可使澳的四氯化碳溶液褪色,试写出该反应的化学方程式:
26.(12 分 )金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大。
(1)钢铁的表面发蓝、发黑处理是常用的防腐方法。下列反应是主要反应之一。
请配平方程式:口 Na2FeO2+ 口 NaNO2+ 口 = 口 NaFeO2+ 口 NH3↑+ 口 NaOH
 (2)钢铁的“钝化”处理也能达到防腐目的,经
(2)钢铁的“钝化”处理也能达到防腐目的,经
冷、浓 HNO3 处理后,其表面有一层致密氧化物保
护膜,但是加热或在稀 HNO3中 就不能 “钝化”。
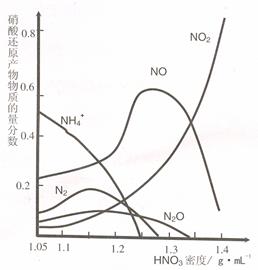
不同浓度的 HNO3 与铁反应的还原产物很复杂,
其分布曲线如图。
① 图示可知,密度为 1.05g·mL-1 的硝酸与铁
反应时,其最多的还原产物是 ;密度大于1.35 g·mL-1的硝酸与铁反应时,其还原产物主要是 NO2;分析HNO3 与铁反应的规律是:
。
② mg 铁与含 n g HNO3的硝酸溶液恰好完全反应,若硝酸的还原产物只有 NO, 则 m 的取值可能是 (填字母编号 )
A.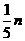 B.
B.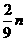 C.
C.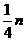 D.
D.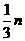 E.
E.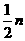
③工业上一般不用冷浓硝酸进行铁表面处理,其可能的原因是: 。
(3)金属 (M) 的腐蚀是因为发生反应: M-ne-→Mn+,除了上述表面处理的方法外,下列方法也能起到防腐作用的是 (填字母编号)
A.在铁中掺入铭、镇等金属,改变其内部结构,制成不锈钢
B.在铁制品表面镀辞
C.提高铁中含碳量,制成生铁
D.将水库铁闸门与直流电源的负极相连
25.(7 分 )水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C (s) + H2O(g)≒CO (g) +H2 (g);△H =+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
|
容器编号 |
c(H2O)/mol·L-1 |
c(CO)/mol·L-1 |
c(H2)/mol·L-1 |
V正、V逆比较 |
|
I |
0.06 |
0.60 |
0.10 |
V正=V逆 |
|
II |
0.06 |
0.50 |
0.40 |
? |
|
III |
0.12 |
0.40 |
0.80 |
V正<V逆 |
|
IV |
0.12 |
0.30 |
? |
V正=V逆 |
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为 ;向该容器中补充 a mol 炭,水蒸气的转化率将 (填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为 。
(3)己知:C (s) + 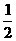 O2(g)=CO (g);△H = -110.5kJ·mo1-1
O2(g)=CO (g);△H = -110.5kJ·mo1-1
CO(g) + 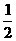 O2(g) =CO2 (g);△H =-283.0 kJ·mo1-1
O2(g) =CO2 (g);△H =-283.0 kJ·mo1-1
H2
(g) + 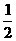 O2 (g) =H2O (g);△H = -241.8kJ·mo1-1
O2 (g) =H2O (g);△H = -241.8kJ·mo1-1
那么,将2.4 g 炭完全转化为水煤气,然后再燃烧,整个过程△H = kJ·mo1-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com