
题目列表(包括答案和解析)
8.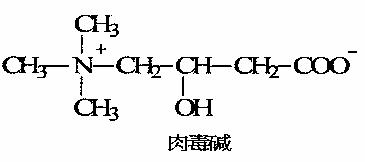 肉毒碱是具有多种生理功能的氨基酸类物质,又名维生素Bt,是一种类维生素。1927年测定了它的结构,1958年发现其能促进脂肪代谢,1985年被指定为“多功能营养品”。下列有关肉毒碱的说法不正确的是 ( )
肉毒碱是具有多种生理功能的氨基酸类物质,又名维生素Bt,是一种类维生素。1927年测定了它的结构,1958年发现其能促进脂肪代谢,1985年被指定为“多功能营养品”。下列有关肉毒碱的说法不正确的是 ( )
A.肉毒碱的分子式为:C7H15NO3
B.肉毒碱能与氢氧化钠反应但不能与盐酸反应
C.一定条件下肉毒碱能发生酯化反应、消去反应、取代反应
D.H核磁共振谱(1H-NMR)证明分子中的3个甲基上的氢属等效氢
7.HgCl2的稀溶液可用作消毒剂。已知HgCl2的熔点是277℃,熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力,则下列说法正确的是 ( )
A.HgCl2不属于分子晶体 B.HgCl2属于离子晶体
C.HgCl2不属于电解质 D.HgCl2属于弱电解质
6.设NA表示阿伏加德罗常数,下列叙述正确的
是 ( )
A.71 g氯气被还原得到的电子数为2NA
B.100 mL l mol·L-1的碳酸钠溶液中含有的CO32-数为0.1NA
C.标准状况下,2.24 L苯中含有的碳原子数为0.6 NA
D.用含有少量锌、铁、银等杂质的粗铜作阳极电解精炼,当阴极析出64 g金属时阳极失去的电子数小于2NA
4.共价键、离子键和分子间作用力是粒子之间的三种不同作用力。下列物质的品体中:①Na2O2 ②CO2 ③金刚石 ④NaCl ⑤白磷,含有上述两种作用力的是 ( )
A.①②⑤ B.①②③
C.②④⑤ D.②③⑤
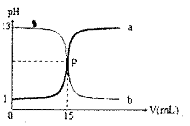 5.右图曲线a和b是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述正确的是( )
5.右图曲线a和b是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述正确的是( )
A.盐酸的物质的量浓度为1 mol·L
B.P点时反应恰好完全,溶液早中性
C.曲线a是盐酸滴定氢氧化钠的滴定曲线
D.酚酞不能用丁本实验的指示剂
3.关于非金属元素Cl、Si、S、N的叙述,正确的是 ( )
A.在通常情况下其单质均为气体
B.其单质均由双原子分子构成
C.都有相应的含氧酸
D.每种元素仪存在一种氧化物
2.我国二氧化碳的排放量位居世界第二,为减少二氧化碳这种温室气体的排放,下列措施:不切实际的是 ( )
A.不使用含碳能源 B.充分利用太阳能
C.大力开发氢能源 D.提高能源利用率
1.2009年10月6日,瑞典皇家科学院宣布,将2009年物理诺贝尔奖授予英籍华裔科学家高锟,表彰他在“有关光在纤维中的传输以用于光学通信方面”取得的突破性成就。光导纤维的主要成分是 ( )
A.Si B.SiO2 C.H2SiO3 D.Na2SiO3
20. (本题包括 个小题,共10分)
复分解反应是中学化学中常见的一种反应类型。
(1)已知在常温下,测得浓度均为0.1mol/L的下列六种溶液的pH:
|
溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
复分解反应存在这样一个规律:一种较强酸与一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑
若换个角度看,它同时还揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请你判断下列反应不能成立的是 (填编号)。
A.CO2+H2O+2NaClO=Na2CO3+2HClO
B.CO2+H2O+NaClO=NaHCO3+HClO
C.CO2+H2O+C6H5ONa→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
E.CH3COOH+NaCN=CH3COONa+HCN
(2)根据前述信息判断,浓度均为0.05mol/L的下列六种物质的溶液中,pH最小的是 (填编号),其pH为 (填数值);pH最大的是 (填编号);
①HClO4 ②CH3COOH ③HCN ④HClO ⑤H2SO4
(3)一些复分解反应的发生还遵循其他的规律。下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液
②工业上将石灰乳与苦卤(主要溶质KCl、MgCl2)混合可得氢氧化镁固体
③蒸馏KCl和NaNO3混合溶液,首先析出NaCl晶体
请根据上述反应,总结出复分解反应发生的另一个规律: 。
将KI溶液与AgCl固体混合搅拌,固体变为黄色。该反应也遵循这一规律,请写出反应的化学方程式: 。
21 (本题共12分)
19. (本题包括2个小题,共16分)
Ⅰ..(3分) 一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验。某研究性学习小组在实验室中配制1mol/L的稀硫酸标准溶液,然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是______________
A、实验中所用到的滴定管、容量瓶,在使用前均需要检漏;
B、如果实验中需用60mL 的稀硫酸标准溶液,配制时应选用100mL容量瓶;
C、容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小;
D、酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大;
E、用甲基橙作指示剂,滴定终点时,溶液颜色从橙色变为红色;
F、配制溶液和中和滴定的两个实验中,若在最后一次读数均俯视读数,则导致实验结果都偏大。
 Ⅱ
.(13分)
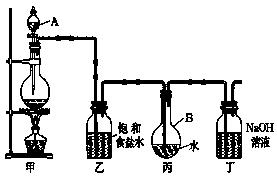
现用如图所示的装置制取较多量的饱和氯水并测定饱和氯水的pH。
Ⅱ
.(13分)
现用如图所示的装置制取较多量的饱和氯水并测定饱和氯水的pH。
回答有关问题:
(1)写出有关化学方程式。
装置甲:____________________________________ ;
装置丁: __________________ 。
(2)证明氯水已饱和的现象是 。
(3)制取结束时,装置丙的液体中含有的微粒是 (用微粒符号表示 );
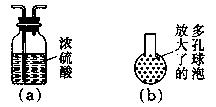
(4)有如下改进措施或建议,请作出评价:
①在装置乙和丙之间增加如图(a)所示的装置,你认为有无必要? 。
②在装置丙的长导管下口处,接如图(b)所示的多孔球泡,这样做的好处是: 。
③若撤去装置乙,直接将装置甲和丙相连。这样做对实验结果的影响是: 。
18.(6分) 由短周期元素组成的A、B两种盐可发生下列变化,且B的焰色反应呈黄色(图中其它生成物未列出)
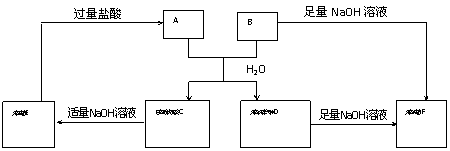
(1).A和B的混合物溶于水发生反应的离子方程式_________________________________.
(2). B、E两溶液混合反应时,可观察到的现象是__________________________,写出其反应的离子方程式__________________________________________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com