
题目列表(包括答案和解析)
22.(6分)海水是人类资源宝库,工业上利用电解饱和食盐水可制得重要化工产品。该电解反应的离子方程式为: 。
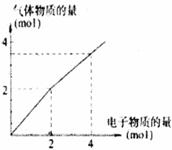
用惰性电极电解一定浓度的食盐水时,通过电子的物质的量与生成气体总物质的量的关系如下图所示(不考虑氯气的溶解)。若电解结束时,通过电子总物质的两为4 mol,电解后恢复至常温,溶液的体积为2L,则溶液的pH为 ,混合气体中氢气的物质的量为 。
21.(9分)熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求。试回答以下问题:
(1)“磨砂”是增加玻璃仪器密封性的一种处理工_艺。在下列仪器中,没有用到“磨砂”工艺处理的有 (填序号)。
a.试管 b.分液漏斗c.带滴管的试剂瓶(滴瓶)d.集气瓶e.酸式滴定管f.碱式滴定管
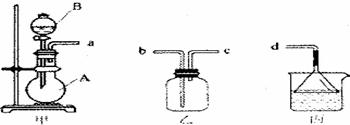 (2)用装置甲、乙、内和乳胶管组成一套装置(气密性已检查),可用于制取并收集
(2)用装置甲、乙、内和乳胶管组成一套装置(气密性已检查),可用于制取并收集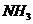 或
或 气体。可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。请回答下列问题:
气体。可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。请回答下列问题:
①若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B均为无色液体,则试剂A为 ,制取该气体利川了B的性质有 、 。
通过丙中紫色石蕊溶液变红或变监,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶甲中应加入的固体试剂A为 ;
②若在乙中收集氨气,气体流经装置的顺序是:a→ → →d(填接口代号)。
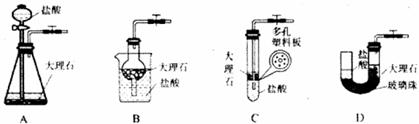 (3)下图中的装置D是实验室制备
(3)下图中的装置D是实验室制备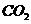 的简易装置图,该该装置制备
的简易装置图,该该装置制备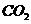 可起到随时使反应发生,也可以随时使反应停止的效果。下图中的装置A、B、C也可起到相同效果的有 (填
可起到随时使反应发生,也可以随时使反应停止的效果。下图中的装置A、B、C也可起到相同效果的有 (填
写编号)。
20.(8分)现有 种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
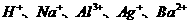 |
|
阴离子 |
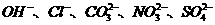 |
已知:①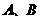 两溶液甲碱性;
两溶液甲碱性;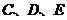 溶液呈酸性。
溶液呈酸性。
② 溶液与
溶液与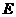 溶液反应既有气体又有沉淀产生;
溶液反应既有气体又有沉淀产生; 溶液与
溶液与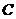 溶液反应只有气体产生 (沉淀包括微溶物,下同)。
溶液反应只有气体产生 (沉淀包括微溶物,下同)。
③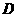 溶液与另外四种溶液反应都能产生沉淀;
溶液与另外四种溶液反应都能产生沉淀;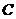 只能与
只能与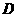 反应产生沉淀。
反应产生沉淀。
试回答下列问题:
(1)  是
是
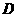 是
(写化学式)
是
(写化学式)
(2)将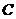 溶液逐滴加入等体积、等物质的量浓度的
溶液逐滴加入等体积、等物质的量浓度的 溶液中,各种离子浓度之间的关系为
溶液中,各种离子浓度之间的关系为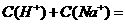 。
。
(3) 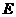 的水溶液呈酸性,用离子方程式解释其原因
。
的水溶液呈酸性,用离子方程式解释其原因
。
19.(8分) 为五种常见的短周期元素,常温下
为五种常见的短周期元素,常温下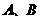 可形成
可形成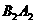 和
和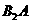 两种液态化合物,
两种液态化合物,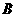 与
与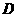 可组成分子
可组成分子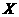 ,也可组成阳离子
,也可组成阳离子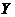 ,
,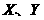 在水溶液中酸、碱性恰好相反,
在水溶液中酸、碱性恰好相反,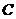 元素的原子比
元素的原子比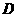 元素多
元素多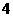 个质子,
个质子,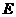 与
与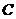 同周期,且
同周期,且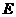 的最高价氧化物的水化物呈两性。
的最高价氧化物的水化物呈两性。
试回答:
(1) 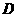 元素在周期表表中的位置为 。
元素在周期表表中的位置为 。
(2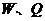 是由
是由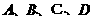 四种元素中任意三种组成的不同类型的强电解质,常温下
四种元素中任意三种组成的不同类型的强电解质,常温下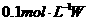 的水溶液的
的水溶液的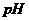 为
为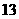 ,
,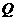 的水溶液呈酸性,且物质的量浓度相同的
的水溶液呈酸性,且物质的量浓度相同的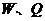 溶液中水的电离程度是前者小于后者。则:
溶液中水的电离程度是前者小于后者。则:
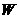 为
,
为
,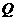 为
(填化学式)。
为
(填化学式)。
 (3)已知工业合成
(3)已知工业合成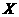 的反应方程式:
的反应方程式: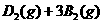
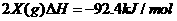 某温度下,将
某温度下,将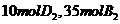 置于
置于 密闭容器中充分反应,
密闭容器中充分反应, 达平衡,反应放热为
达平衡,反应放热为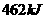 ,计算:该温度下的平衡常数
。
,计算:该温度下的平衡常数
。
18.(9分)某短周期元素 ,其最高价氧化物对应水化物甲与其气态氢化物乙反应可生成盐丙。己知乙的密度是同温同压下
,其最高价氧化物对应水化物甲与其气态氢化物乙反应可生成盐丙。己知乙的密度是同温同压下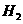 密度的
密度的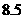 倍。请回答:
倍。请回答:
(1)乙的化学式为 。
(2)甲具有不稳定性,发生分解反应的化学反应方程式为 。实验室保存甲的方法是 。
(3)丙对水的电离起 作用(填“抑制”、“促进”或“不影响”),原因是(用离子方程式表示) 。
(4)现有硫酸和甲的混合液 ,其中硫酸的物质的量浓度为
,其中硫酸的物质的量浓度为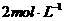 ,甲的物质的量浓度为
,甲的物质的量浓度为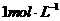 。向该混合液中加入
。向该混合液中加入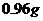 铜粉,假设只生成一种无色气体,则所收集到气体的体积在标准状况下为
铜粉,假设只生成一种无色气体,则所收集到气体的体积在标准状况下为
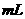
17.(6分)“曲气东输”是西部开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水住高温下反应制得水煤气,水煤气的土要成分是 和
和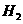 ,二者的体积比为
,二者的体积比为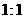 。已知
。已知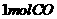 气体完全燃烧生成
气体完全燃烧生成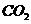 气体放出
气体放出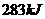 热量;
热量; 氢气完全燃烧生成液态水放出
氢气完全燃烧生成液态水放出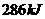 热量;
热量;
 完全燃烧生成
完全燃烧生成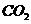 气体和液态水放出
气体和液态水放出 热量。
热量。
(1)写山氢气完全燃烧生成液态水的热化学方程式 。
(2)若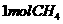 气体完全燃烧生成
气体完全燃烧生成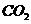 气体和水蒸气,放出的热量
气体和水蒸气,放出的热量
 (填
(填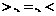 )
)
(3)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为 。(取简单整数比)
16.(9分)下表为长式周期表的一部分,其中的编号代表对应的元素。
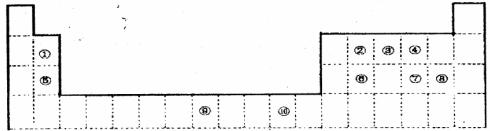
(1)表中属丁d区的元素是 (填编号);
(2)③、④两种元素的电负性人小为③ ④(填“ ”、“
”、“ ”、“
”、“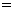 ”,下同),它们的第一电离能大小为③ ④。
”,下同),它们的第一电离能大小为③ ④。
(3)②、⑤、⑧元素的单质熔点高低的顺序是 (用编号表示)。
(4)③元素的氢化物住水中的溶解度比同族元素的其它氢化物人得多的原因是
(5)⑥与⑧形成的分子最外层都满足8电子稳定结构,则在分子中⑥原子的杂化轨道的形式是 。分子空间构型是 。
(6)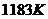 以下,⑨元素形成品体的基本结构单元如图1所示,
以下,⑨元素形成品体的基本结构单元如图1所示,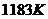 以上基本结构单元转变为如图2所示,在两种晶体中最邻近的原子间距离相等。
以上基本结构单元转变为如图2所示,在两种晶体中最邻近的原子间距离相等。
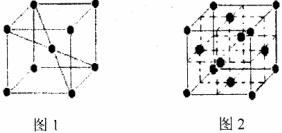
在图2中,与一个⑨原子等距离且最近的⑨原子的个数是 ;图1与图2中含有的⑨原子个数之比为 。
15.常温下有体积相同的四种液体:
①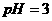 的
的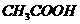 溶液;
②
溶液;
②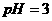 的
的 溶液;
溶液;
③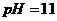 的氨水; ④
的氨水; ④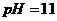 的
的 溶液。
溶液。
下列说法正确的是
A.②和③混合,所得混合溶液的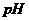 大于7
大于7
B.③与④分别用等浓度的硫酸中和,消耗硫酸的体积:③=④
C.①与②分别与足量的镁粉反应,生成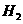 的量:①
的量:① ②
②
D.若将四种溶液稀释100倍,溶液的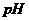 大小顺序是:③
大小顺序是:③ ④
④ ①
① ②
②
第Ⅱ卷:(非选择题,共55分)
14.常温下,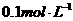 某一元酸
某一元酸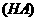 溶液
溶液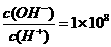 ,下列叙述正确的是
,下列叙述正确的是
A.该一元酸溶液的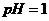
B.该溶液中由水电离山的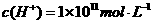
C.该溶液中水的离子积常数为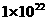
D.用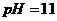 的
的 溶液
溶液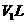 与
与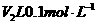 该一元酸
该一元酸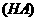 溶液混合,若混合溶液的
溶液混合,若混合溶液的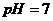 ,则
,则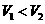
13.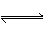 某温度下住一容积不变的密闭容器中
某温度下住一容积不变的密闭容器中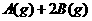
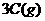 达到平衡时,
达到平衡时,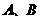 和
和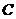 的物质的量分别为
的物质的量分别为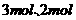 和
和 ,若温度不变,向容器内的平衡混合物中雨加入
,若温度不变,向容器内的平衡混合物中雨加入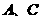 各
各 ,此时该平衡移动的方向为
,此时该平衡移动的方向为
A.向左移动 B.向右移动 C.不移动 D.无法削断
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com