
题目列表(包括答案和解析)
9.能够使反应Cu+2H2O=2Cu(OH)2+H2↑发生的是 ( )
A.铜片作阴、阳电极,电解氯化铜溶液
B.铜片作阴、阳电极、电解硫酸钾溶液
C.铜片作原电池的负极,碳棒作原电池的正极,氯化钠作电解质溶液
D.铜锌合金在潮湿的空气中发生电化学腐蚀
8.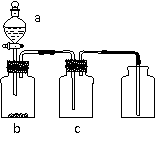 用下图装置制取,提纯并收集表中的四种气体(a,b,c表示相应仪器中加入的试剂),其中可行的是 ( )
用下图装置制取,提纯并收集表中的四种气体(a,b,c表示相应仪器中加入的试剂),其中可行的是 ( )
|
|
气体 |
a |
b |
c |
|
A |
NO2 |
浓硝酸 |
铜片 |
NaOH溶液 |
|
B |
SO2 |
浓硫酸 |
Cu |
酸性KMnO4溶液 |
|
C |
NH3 |
浓氨水 |
生石灰 |
碱石灰 |
|
D |
CO2 |
稀盐酸 |
CaCO3粉末 |
浓硫酸 |
7. 在下列溶液中、各组离子一定能够大量共存的是 ( )
A.在含有大量AlO2的溶液中: NH4+、Na+、Cl-、H+
B.加入铝粉生成H2的溶液:K+、Cu+、SO2-、ClO
C.c(H+)=10-13mol·L-1的溶液中:NO3- 、Ba2+、Cl、Br
D.在pH=1的溶液中:K+、I-、Cl、NO
6.在浓盐酸中H2AsO3与SnCl2反应的离子方程式为:
3SnCl2-12Cl+2H2AsO-6H+=3SnCl+2As+M
关于该反应的说法正确的组合是 ( )
①氧化剂是H2AsO2
②还原性Cl-、As
③M为OH
④每生成0.1molAs,反应中转移电子的物质的量为0.3mol
A.①②③ B.①④ C.①②④ D.只有①
4.下列稀溶液置于空气中,一段时间后,pH变小的是(不考虑溶质的挥发) ( )
①H2SO4 ②Ca(OH)2 ③氯水
④Na2SO3 ⑤H2S
A.①②③④ B.①③④ C.①③⑤ D.②④⑤
 5.在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物 ( )
5.在核磁共振氢谱中出现两组峰,其氢原子数之比为3:2的化合物 ( )
3.同温同压下两个容积相等的贮气瓶,一个装有H2气体,另一个装有O2和N2的混合气体,则两瓶内的气体一定不相同的是 ( )
A.气体的物质的量 B.气体质量
C.分子总数 D.原子数
2.下列叙述不正确的是 ( )
A.氯水溶液通常保存在棕色试剂瓶中,是因为次氯酸见光易分解
B.将Cl2和SO2分别通入到品红溶液中,均能使品红溶液褪色
C.反应AgCl+NaBr-=AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水
D.常温下浓硫酸可贮存在铁制或铝制容器中,说明常温下铁和铝与浓硫酸不反应
1.下列说法中正确的是 ( )
A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
B.蔗糖、硫酸钡和水分别属于非电解南、强电解质和弱电解质
C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到
D.沼气、天气然和水煤气分别属于化石能源、可再生能源和二次能源
23.(10分)U、V、W、X、Y、Z属于周期表中前18号元素,原子序数依次
增大。已知:
① WU4++XU-=WU3 + U2X,各种反应物和生成物的电子总数都与Y+相等;
② Z的单质在X2中燃烧的产物可使品红溶液褪色;
③ V的单质在X2中燃烧可生成VX和VX2两种气体;
④ Y的单质是一种金属,该金属与X2反应可生成Y2X和Y2X2两种固体。
请回答下列问题:
(1)W与X的氢化物分子结合氢离子的能力较强的是 ,方程式表示 。
(2)V、W、X形成的10电子氢化物中,沸点最高的是(写化学式) 。
(3)U2X2与FeSO4按物质的量之比1:2溶于稀硫酸中,离子方程式为________
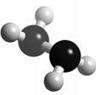
(4)已知右图的球棍模型所表示的是由U、W两种元素组成的共价化合物A,
则A的分子式为 。A与氧气及氢氧化钾溶液还可构成燃料电池,电池正极的电极反应为: [

22.(每空4分)下列图1中B是一种常见的无色无味的液体。C是一种有磁性的化合物,E是一种无色无味的有毒气体。根据下列图1、图2,回答下列问题:
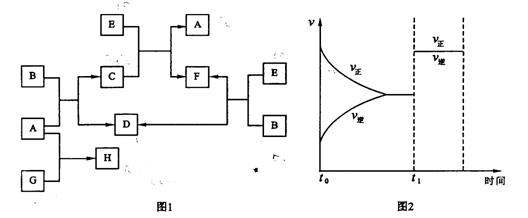
(1)写出A+B→C+D的化学方程式 ;
(2)在101kPa和150℃时,可逆反应E(g)+ B(g) F(g) + D(g)
F(g) + D(g)
反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原
因可能是(填选项字母) ;
A.升高温度 B.增大压强 C.加入催化剂
(3)若G是一种黄色固体单质,16 g G和足量的A反应放出的热量为
QkJ(Q > 0),写出这个反应的热化学方程式 。
(4)若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式 ;少量H的浓溶液滴入沸水中,继续煮沸,生成了一种红褐色的液体,请用离子方程式表示该过程 。
(5)请写出C与足量的稀盐酸反应的离子方程式__________________
附加题(共10分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com