
题目列表(包括答案和解析)
15.下列实验装置图完全正确的是 ( )
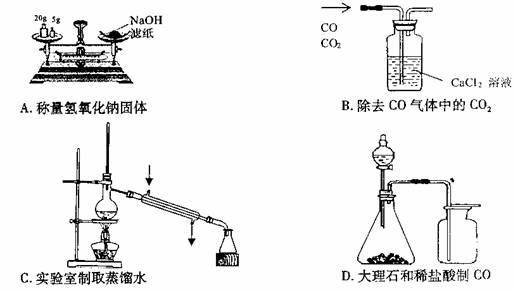
第Ⅱ卷
14.关于下列四个图像的说法中正确的是 ( )
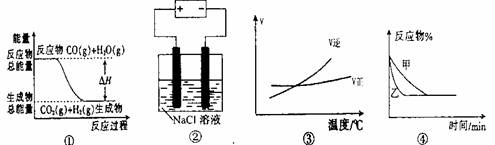
 A.图①表示可逆反应“CO(g)+H2O(g)
CO2(g)+H+(g)”中的AH>0
A.图①表示可逆反应“CO(g)+H2O(g)
CO2(g)+H+(g)”中的AH>0
B.图②是在电解氯化钠稀溶液的电解池中,阴、阳两极收集到的气体体积之比一定为1:1
 C.图③表示可逆反应“A+(g)+3B+(g)
2AB3(g)”的AH<0
C.图③表示可逆反应“A+(g)+3B+(g)
2AB3(g)”的AH<0
 D.图④表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大
D.图④表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大
13.下列反应的离子方程式错误的是 ( )
A.醋酸和足量的氢氧化钠溶液反应:H++OH-=H2O
B.溴化亚铁溶液中通入足量的氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
C.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O
D.碳酸氢铵稀溶液中加入过量的石灰水:
Ca2++HCO3-+2OH-+NH4+=CaCO3↓+NH3·H2O+H2O
12.2009年甲型H1N1流感疫情在全球暴发,继“非典”之后,又一场抗击全球性传染病的战斗打响了。我国莱茵生物公司从中药八角中提取莽草酸,再经过多步反应合成的达菲因此变得供不应求。已知莽草酸和达菲的结构式如下:
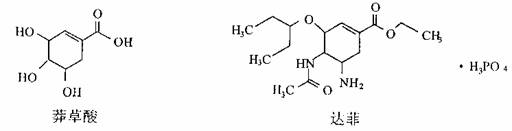
下列关于莽草酸和达菲的判断不正确的是 ( )
A.它们都能使溴的四氯化碳溶液褪色
B.莽草酸的分子式为C7H10O5
C.达菲在热的NaOH溶液中不能稳定存在
D.莽草酸和达菲的分子中含有羟基、羧基、氨基、苯环等结构
11.若NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.含有NA个氖原子的氖气在标准状况下的体积约为11.2L
B.2.3gNa被O2完全氧化时,失去电子数为0.1N。
C.2Llmol·L-1的盐酸中所含氯化氢分子数约为2NA
D.标准状况下,5.6LCCl4含有的分子数为0.25NA
10.下列说法中正确的是 ( )
A.汽油燃烧时将全部的化学能转化为热能
B.向饱和AgCl溶液中加入盐酸,Kap变大
C.若存在简单阴离子R2-,则R一定属于VIA族
D.最外层电子数较少的金属元素,一定比最外层电子数较它多的金属元素活泼性强
9.下列有关物质分类或归类正确的一组是 ( )
①液氨、液氯、干冰、碘化银均为化合物
②氢氟酸、盐酸、水玻璃、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质
④碘酒、牛奶、豆浆、漂粉精均为胶体
⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐
A.①和② B.②和③ C.③和④ D.②③⑤
21.(8分)钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C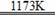 2TiCl4+2FeCl3+6CO
2TiCl4+2FeCl3+6CO
TiO2+2Cl2+2C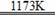 TiCl4+2CO
TiCl4+2CO
将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:
TiCl4+2Mg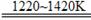 Ti+2MgCl2
Ti+2MgCl2
MgCl2和过量Mg用稀盐酸溶解后得海绵状钛,再在真空熔化铸成钛锭。
请回答下列问题:
(1)基态钛原子的价电子排布式为 。
(2)与CO互为等电子体的离子为 (填化学式)。
(3)在CH2Cl2、C6H6、CO2、C2H4中,碳原子采取sp1杂化的分子有 。
(4)TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于 (填“原子”、“分子”或“离子”)晶体。
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是
 ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 。
;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 。
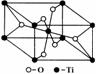
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其
中金红石的晶胞如右图所示,则其中Ti4+的配位数为 。
21. 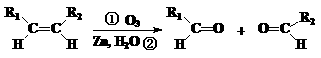 (8分)已知:
(8分)已知:
(1)该反应的生成物中含有的官能团的名称为 ,该类物质在一定条件下能发生 (填序号)。
①银镜反应 ②酯化反应 ③还原反应 ④消去反应 ⑤加成反应
(2)已知HCHO分子中所有原子都在同一平面内,若要使R1CHO分子中所有原子都在同一平面内,R1可以为 (填序号);
①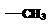 ②
②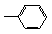 ③
③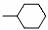
(3)某氯代烃A的分子式为C6H11Cl,它可以发生如下转化:
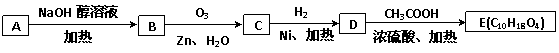
结构分析表明E分子中含两个甲基且没有支链。试回答:
①写出C的分子式 ;写出A的结构简式 。
②写出由D生成E的的化学方程式 。
20. (10分)硫酸工厂周围的空气中有较多的二氧化硫。某研究性学习小组为了测定空气
中二氧化硫的体积分数设计了如下两个方案:
方案一:取标准状态下的空气V L(内含N2、O2、CO2、SO2等),缓慢通过足量溴水,在所得的溶液中加入过量的氯化钡溶液后,过滤,将沉淀洗涤、干燥,称得其质量为m g。
请回答:
(1)加入过量的氯化钡溶液的目的是 。
(2)过滤后,若在滤液中加入硫酸钠溶液,有白色沉淀产生,说明
。
(3)过滤后,一般要用蒸馏水洗涤沉淀2-3次,以除去附在沉淀上的可溶性物质。请说明应通过什么方法验证可溶物质是否已被除尽(要求:实验过程、使用的试剂、现象及结论)
。
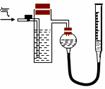
 方案二:如右图所示,装置中反应管内装有碘的淀粉溶液。按设计意图,将空气(内含N2、O2、CO2、SO2等)通过此装置时,其中的SO2被吸收,量气管内增加的体积为其余气体的体积。
方案二:如右图所示,装置中反应管内装有碘的淀粉溶液。按设计意图,将空气(内含N2、O2、CO2、SO2等)通过此装置时,其中的SO2被吸收,量气管内增加的体积为其余气体的体积。
(4)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2的含量 (选填“偏高”、“偏低”或“不受影响”)。
(5)反应管内碘的淀粉溶液可以用下列 (填代号)代替。
A.NaOH溶液 B.酸性KMnO4溶液 C.Na2SO3溶液 D.BaCl2溶液
(6)研究小组经过讨论发现方案二的设计中有一个明显的缺陷影响了测定结果(不属于操作错误),你认为该缺陷是 。
以下为选作题,考生只需从中任选一题作答,若两题均做,则以前一个题目得分为准。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com