
题目列表(包括答案和解析)
1.对于易燃易爆有毒有腐蚀性的化学物质,往往会在其包装上贴危险警告标签。下图所列物质与危险警告标签对应错误的是 ( )
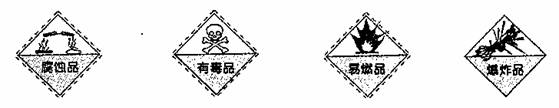
A.浓硫酸 B.金属汞 C.四氯化碳 D.硝酸铵
21.物质与结构试题(略)(山东省沂水三中 高三化学组 邢瑞斌提供 欢迎交流)
临沂市2010年高三年级质量检查考试
20.(10分)[化学一有机化学基础}
分子式为C12H1402的有机物F广泛用于香精的调香剂。
 为了合成该有机物,某实验室的科技人员设计了下列合成路线
为了合成该有机物,某实验室的科技人员设计了下列合成路线
试回答下列问题:
(1)A物质在 核磁共振氢谱中能呈现 种峰;
核磁共振氢谱中能呈现 种峰;
C物质的官能团名称
(2)上述合成路线中属于取代反应的是 (填编号);
(3)反应④的化学方程式为
(4)G是E的同分异构体,且G属于芳香族化合物,能跟FeCl3溶液发生显色反应,苯环上的一氯代物有两种。G的结构简式为
19.(7分)某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验 以下实验:将pH==2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
以下实验:将pH==2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
(1)HA为 酸,HB为 酸(填"强"或“弱")
 (2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为
(用酸、碱化学式表示);
(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为
(用酸、碱化学式表示);
将稀释后的HA溶液利MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为 (填"大于"、"小于"或"等于")
(3)若b+c=14,则MQH为 碱(填"强"或"弱")。将稀释后的HB溶液和MOH溶液取等体积混合,所得很合溶液的pH 7(填"大于"、"小于"或"等于")
18.(11分)氨气在农业和国防工业都有很重要的作用,历史上诺贝尔化学奖曾经有3次颁给研究氮气与氢气 合成氨的化学家。
合成氨的化学家。
(1)右图表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答:
①写出氮气与氢气合成氨的热化学反应方程式:
②对于合成氨的反应下列说法正确的是 (填编号)
A.该反应在任意条件下都可以自发进行
B.加入催化剂,能使该反应的E和△H都减小

 (3)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下吧氢气和用氦气稀释的氮气,分别通人一个加热到500℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质理用吸附在它内外表面上的金属但多晶薄膜像电噪,实现了常压、570℃条件下高转化率的电解法合成氮(装置如图)。
(3)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下吧氢气和用氦气稀释的氮气,分别通人一个加热到500℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质理用吸附在它内外表面上的金属但多晶薄膜像电噪,实现了常压、570℃条件下高转化率的电解法合成氮(装置如图)。
请回答:铠电极是电解池的 极(填"阳"或"阴"),该极上的电极反应式是
17.(10分)A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B元素的最高价氧化物的水化物与其氢化物能相互反应生成盐;A元素与C元素可形成两种液态化合物,其原子个数比分别为1:1和2:1,旦分子中电子总数分别为18和10;D元素的主族序数等于其周期数;E元素原子的最外层电子数是其电子层数的2倍。
(1)写出D元素的原子结构示意图 ;E元素在周期表中位置
(2)C和E两种元素相比较,非金属性较强的是(填元素符号) ,可以验证该结论的是 (填写编号)
A.比较这两种元素的常见单质的沸点 B.比较这两种元素的单质与氢气化合的难易
C.比较这两种元素的气态氢化物的稳定性
(3)写出D的氢氧化物在水中发生酸式电离的电离方程式:
欲使上述体系中D的简单阳离子浓度增加,可加入的物质是
(4)B元素与C元素形成的化合物中,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的B的含氧酸盐的化学式是
16.(12分)Fe元素是地壳中最丰富的元素之一,在金属中仅次于铝,铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe304+4CO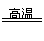
 3Fe+4C02,若有1mol
3Fe+4C02,若有1mol
Fe304参加反应,转移电子的物质的量是 mol.
 (2)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(2)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(3)钢铁的电化腐蚀简单示意图如下,将该图稍作修
改即可成为钢铁电化学防护的简单示意图,请在下图虚
线框内作出修改,并用箭头标出电子流动方向。
(4)硫酸亚铁晶体(FeS04·7H20)常作医药上的补血剂。课外研究性小组测定该补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
①证明步骤①所得滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加,此过程的现象为:
②若该实验温度下,步骤③中难溶物的溶度积为Ksp=8×l0-38,试计算该物质沉淀完全所需要的pH= (已知溶液中离子浓度小于10-5mol)时,该离子可看做沉淀完全;lg2=0.3)
③步骤④中一系列的操作步骤为:过滤、 、灼烧、冷却、称量。
④若实验过程中无损耗,最后称量得到a克红棕色的固体,则每片补血剂中含铁元素的质
量为 g.(用含a的式子表示)
15. (8分)化学实验中一套装置往往可以完成多个实验,A某同学设计了右图所示装置(夹持仪器省略)进行系列实验。请回答:
(8分)化学实验中一套装置往往可以完成多个实验,A某同学设计了右图所示装置(夹持仪器省略)进行系列实验。请回答:
(1)指出下列仪器的名称:
A
D
(2)若A中为浓氨水,B中为烧碱,C中为AICl3溶液,实验中可观测到B中有气体生成,C中有白色沉淀。
则C中发生反应的离子方程式为
仪器D的作用为
(3)若A中装有浓盐酸,B中装有固体KMn04,C中盛有KI淀粉溶液,实验中可观测到B中出
现黄绿色气体,C中溶液变蓝。依据实验现象可以得到的结论为: 
氧化性由强到弱的顺序:
但该装置的不足之处是:
14.常温下,Ksp(CaS04)=9×l0-6,常温下CaS04在水中的沉淀溶解平衡曲线如图。下列说法正
 确的是
确的是
A.常温下CaS04饱和溶液中,c(Ca2+)、c(SO4-)对应曲线上任意一点
B.b点将有沉淀生成,平衡后溶液中c(SOi-)一定等于3×l0-3mol/L
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
山东省临沂市2010年高三年级质量检查考试
化 学 试 题 2010.3
第II卷(非选择题共58分)
不能答在试卷上,否则无效。
13. 课外学习小组为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能够得到的正确结论是
课外学习小组为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能够得到的正确结论是

A.原溶液中一定含有SO42-离子B.原溶液中一定含有NH4+离子
C.原溶液中一定含有CI-离子D.原溶液中一定含有Fe3+离子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com