
题目列表(包括答案和解析)
7.已知NH4CuSO3与足量的10mol/L硫酸液混合微热,产生下列现象:
①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。
据此判断下列说法正确的是 ( )
A、反应中硫酸作氧化剂 B、NH4CuSO3中硫元素被氧化
C、刺激性气味的气体是氨气 D、1mol NH4CuSO3完全反应转移0.5mol电子
6.下列过程都与热量变化有关,其中表述不正确的是( )
A、CO(g)的燃烧热是283.0KJ/mol,则表示CO(g)燃烧反应的热化学方程式为:
CO(g)+1/2 O2(g)= CO2(g);△H=-283.0KJ/mol
B、稀盐酸和稀氢氧化钠溶液反应的中和热为57.3KJ/mol,则表示稀硫酸与稀氢氧化钡
溶液发生反应的热化学方程式为:H+ (aq) + OH-(aq) = H2O(l);△H=-57.3KJ/mol
C、铝热反应是放热反应,但需要足够的热量才能使反应发生
D、水的电离过程是吸热过程,升高温度,水的离子积增大、PH减小
5.在4℃时向100ml水中溶解了22.4LHCl气体(标准状态下测得)后形成的溶液。下列
说法中正确的是( )
A、该溶液物质的量浓度为10mol/L
B、所得的溶液的体积为22.5L
C、根据题干数据,该溶液物质的量浓度无法求得
D、该溶液中溶质的质量分数因溶液的密度未知而无法求得
4.下列排列顺序正确的是 ( )
①热稳定性:HF>H2O>NH3 ②离子半径:Na+>Mg2+>F-
③酸性:盐酸>碳酸>醋酸 ④结合质子能力:OH- >C6H5O- > HCO3-
A.①③ B.②④ C.①④ D.②③
3.下列有关物质分类或归纳的说法中,正确的一组是( )
①蔗糖和麦芽糖的化学式都可用C12H22O11表示,它们互为同分异构体
②聚乙烯、聚氯乙烯、纤维素都属于合成高分子
③明矾、石膏、冰醋酸、水都是电解质 ④盐酸、漂白粉、水玻璃都是混合物
⑤分馏、干馏、裂化都是化学变化 ⑥植物油、直馏汽油都可与溴水反应
A.①③⑤ B.②④⑥ C.①③④ D.②⑤⑥
2.随着科学技术的不断进步,研究物质的手段和途径越来越多, H3、O4、C60、N5+等
已被发现。下列有关说法中正确的是( )
A、H2与H3属于同分异构体 B、O2与O4属于同位素
C、C60是原子晶体 D、N5+离子中含有34个电子
1.化学知识广泛应用于生产、生活中,下列叙述正确的是 ( )
A、空气中的臭氧对人体健康有益无害
B、液氯罐泄漏时,可将其移入水塘中并加入生石灰
C、由石英制取单晶硅的过程中,不涉及氧化还原反应
D、棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质
31、为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。
为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00 mL,加热至1200C左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(气体体积均折算到标准状况的体积):
|
实验序号 |
样品质量(克) |
NaOH溶液的体积(mL) |
氨气的体积(L) |
|
Ⅰ |
7.4 |
40.00 |
1.68 |
|
Ⅱ |
14.8 |
40.00 |
3.36 |
|
Ⅲ |
22.2 |
40.00 |
1.12 |
|
Ⅳ |
37.0 |
40.00 |
0.00 |
(1)实验过程中有关反应的离子方程式为:
; 。
(2)计算用1.85克样品进行同样实验时,生成氨气在标准状况的体积为 L
(3)计算确定该混合物中(NH4)2SO4和NH4HSO4的物质的量之比 。
(4)欲计算该NaOH溶液的物质的量浓度应选择第 组数据,由此求得NaOH溶液的物质的量浓度为 。
上海市部分重点中学2009学年高三第二次联考
30、已知: IO3-+5I-+6H+→3I2+3H2O。工业上利用NaIO3和NaHSO3反应来制取单质I2。
①NaIO3不足时:2NaIO3+6NaHSO3→2NaI+3Na2SO4+3H2SO4
②NaIO3足量时:4NaIO3+10NaHSO3→2I2+7Na2SO4+3H2SO4+2H2O
现模拟工业制取I2。在含31.2gNaHSO3的溶液中逐滴加入2mol/LNaIO3溶液vmL。
(1)当v= mL时,再滴NaIO3就开始析出I2 。
(2)当v为55mL时,生成的I2的质量为 g。
29、已知①一定下条件下,R-Cl+2Na+Cl-R′→R-R′+2NaCl
②醛和醇可以发生氧化反应,相关物质被氧化的难易次序是:
 R
R
 RCHO最易,R-CH2OH次之, CHOH最难
RCHO最易,R-CH2OH次之, CHOH最难
R
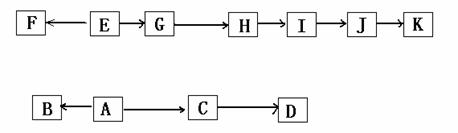 现有某氯代烃A,其相对分子质量为78.5;B与氯气反应生成的一氯代物有两种。有关的
现有某氯代烃A,其相对分子质量为78.5;B与氯气反应生成的一氯代物有两种。有关的
转化关系如下图所示(部分产物及条件均已略去);

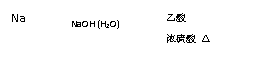
(1)分子式:A ;反应类型:A→C ,E→F ;
(2)结构简式:B ,K ;
(3)反应方程式:A→E 。
G→H 。
(4)D的同分异构体属于羧酸的有四种,其中有2个-CH3基团的有两种。请写出这两
种中的任一种结构简式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com