
题目列表(包括答案和解析)
19.(14分)异嗯草酮是一种色素抑制类除草剂,它的工业合成路线如下:
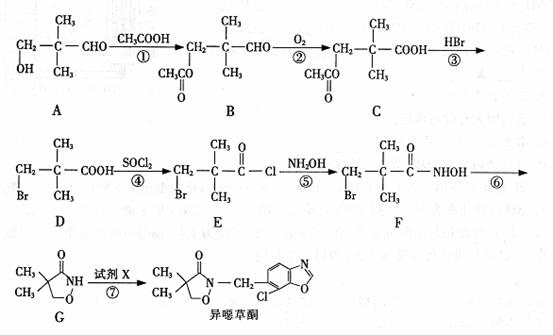
请回答下列问题:
(1)从A一D过程中,反应①的目的是________。
(2)写出满足下列条件的A的一种同分异构体的结构简式 _______。
①与A具有相同的官能团;②分子中具有两个手性碳原子。
(3)物质D与NaOH溶液反应的化学方程式为______。
(4)由G制备异愕草酮的反应中要加入试剂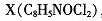 ,X的结构简式为______。
,X的结构简式为______。
(5) 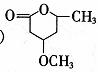 是B的同分异构体。请设计合理方案,完成从
是B的同分异构体。请设计合理方案,完成从
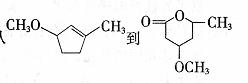
的合成路线(用合成路线流程图表示,并注明反应条件)。
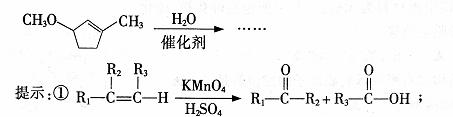
②合成过程中无机试剂任选:
③合成路线流程图示例如下:
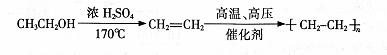
18.(8分)在汽车上安装三效催化转化器,可使汽车尾气中主要污染物(CO、NO;、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
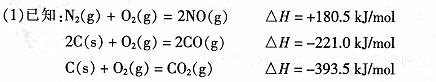
尾气转化的反应之一: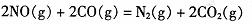 △H= _____ 。
△H= _____ 。
(2)某研究性学习小组在技术人员的指导下,按下列流程探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。
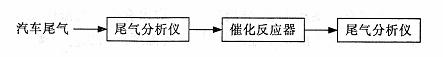
 ①在实验过程中除空燃比不同外,需控制其他条件:汽车尾气的流速、______ 等必须相同。
①在实验过程中除空燃比不同外,需控制其他条件:汽车尾气的流速、______ 等必须相同。
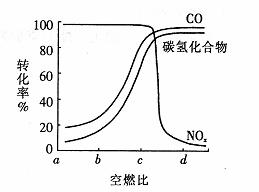
②在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比为________(选填a、6、c、d)时,催化剂对汽车尾气的催化效果最好。
(3)CO分析仪以燃料电池为工作原理,其装置如下图所示,该电池中的电解质为氧化钇一氧化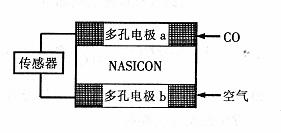 钠,其中
钠,其中 可以在固体介质NASICON中自由移动。下列说法错误的是______。
可以在固体介质NASICON中自由移动。下列说法错误的是______。
A.负极的电极反应式为: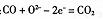
B.工作时电极b作正极, 由电极a移向电极b
由电极a移向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越大
17.(10分)利用化学原理可以对工厂排放的废水进行有效检测和合理处理。
(1)染料工业排放的废水中含有大量有毒的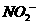 ,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润红色石蕊试纸变蓝的气体)。除去
,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润红色石蕊试纸变蓝的气体)。除去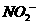 离子的离子方程式是 _______.
离子的离子方程式是 _______.
(2)废水中的N、P元素是造成水体富营养化的主要因素,农药厂排放的废水中常含有较多的
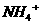 和
和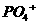 ,一般可以通过两种方法将其除去。
,一般可以通过两种方法将其除去。
①方法一:将Ca(0H)2或CaO投加到待处理的废水中,生成磷酸钙,从而进行回收。当处理后的废水中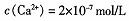 时,溶液中
时,溶液中
(已知埘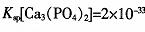 )
)
②方法二:在废水中加入镁矿工业废水,就可以生成高品位的磷矿石--鸟粪石,反应的方程式为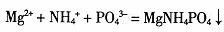 。该方法中需要控制污水的pH为7.5-10,若pH高于10.7,鸟粪石的产量会大大降低。其原因可能是 _____。与方法一相比,方法二的优点是 _____ 。
。该方法中需要控制污水的pH为7.5-10,若pH高于10.7,鸟粪石的产量会大大降低。其原因可能是 _____。与方法一相比,方法二的优点是 _____ 。
(3)三氯乙烯在印刷、纺织等行业应用广泛,为了减少其对环境的影响,可将三氯乙烯在二氧化钛薄膜上催化降解,其反应的机理如下:
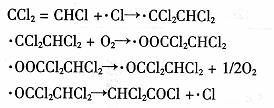
该反应的总化学方程式为 ________ 。
16.(12分)一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
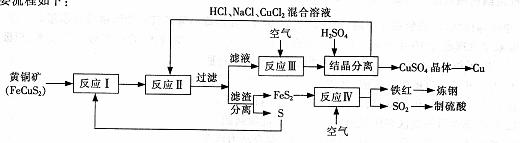
注:反应Ⅱ的离子方程式为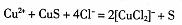
请回答下列问题:
(1)反应I的产物是______(填化学式)。
(2)反应Ⅲ的离子方程式是________。
(3)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是 ________。
(4)炼钢时,可将铁红投入熔融的生铁中,该过程中主要反应的化学方程式是__________.
(5)某硫酸厂为测定反应Ⅳ所得气体中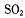 的体积分数,取280 mL(已折算成标准状况)气体样品与足量
的体积分数,取280 mL(已折算成标准状况)气体样品与足量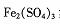 ,溶液完全反应后,用浓度为0.02000 mol/L的
,溶液完全反应后,用浓度为0.02000 mol/L的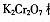 ,标准溶液滴定至终点,消耗
,标准溶液滴定至终点,消耗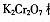 ,溶液25.00mL。已知:
,溶液25.00mL。已知:
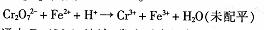
①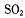 通人
通人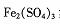 溶液,发生反应的离子方程式为______。
溶液,发生反应的离子方程式为______。
②反应Ⅳ所得气体中SO2的体积分数为______
15.(12分)CoCl2·6H20是一种饲料营养强化剂。以含钴废料(含少量Fe、AL杂质)制取COCl2·6H20的一种新工艺流程如下图:
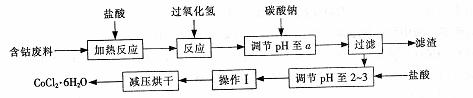
已知:
①钴与盐酸反应的化学方程式为: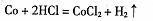
2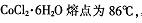 ,易溶于水、乙醚等;常温下稳定无毒,加热至110-120°C~,失去结晶水变成有毒的无水氯化钴。
,易溶于水、乙醚等;常温下稳定无毒,加热至110-120°C~,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:

请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸’’直接溶解含钴废料,其主要优点为_________ 。
(2)加入碳酸钠调节pH至a,a的范围是_______。
(3)操作I包含3个基本实验操作,它们是_______ 和过滤。
(4)制得的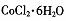 需减压烘干的原因是_______。
需减压烘干的原因是_______。
(5)为测定产品中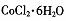 含量,某同学将一定量的样品溶于水,再向其中加入足量的AgN03溶液,过滤,洗涤,并将沉淀烘干后称量其质量。通过计算发现产品中
含量,某同学将一定量的样品溶于水,再向其中加入足量的AgN03溶液,过滤,洗涤,并将沉淀烘干后称量其质量。通过计算发现产品中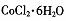 的质量分数大于100%,其原因可能是_______。
的质量分数大于100%,其原因可能是_______。
(6)在实验室中,为了从上述产品中获得纯净的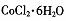 ,采用的方法是________.
,采用的方法是________.
14..500 mL 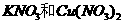 的混合溶液中c
的混合溶液中c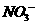 6。O mol/I。,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4.L气体(标准状况)。下列说法正确的是
6。O mol/I。,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4.L气体(标准状况)。下列说法正确的是
A.原混合溶液中c(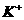 )为2 moL/L
B。上述电解过程中共转移4 mol电子
)为2 moL/L
B。上述电解过程中共转移4 mol电子
C.电解得到的Cu的物质的量为0.5 m01. D.电解后溶液中c(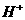 )为4 mol/I。
)为4 mol/I。
13.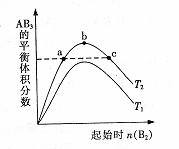 在其他条件不变时,改变某一条件对A:(g)+3B:(g)≠2AB,(g) 化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度)。下列结论正确的是
在其他条件不变时,改变某一条件对A:(g)+3B:(g)≠2AB,(g) 化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度)。下列结论正确的是
A.a、c两点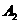 的转化率相等
的转化率相等
B.正反应一定是吸热反应,且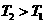
C.b点时,平衡体系中A、B原子数之比为1:3
D.向a点的平衡体系中加入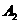 ,可达到b点的平衡状态
,可达到b点的平衡状态
12.下列溶液中各微粒的浓度关系正确的是
A.O.1 mol/l.pH=9的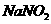 溶液中.:
溶液中.: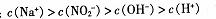
B.等pH的氨水、KOH溶液、 溶液中:
溶液中: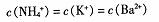
C.向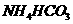 溶液中滴加NaOH溶液至pH=7:
溶液中滴加NaOH溶液至pH=7:
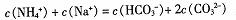
D.将10 mI_0.1mol/I.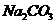 溶液逐滴滴加到10 mL 0.1 moL/l。盐酸中:
溶液逐滴滴加到10 mL 0.1 moL/l。盐酸中:
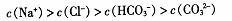
11.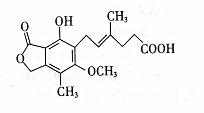 麦考酚酸是一种有效的免疫抑制剂,能有效地防止肾移植排斥,其结构简式如下图所示。下列有关麦考酚酸说法正确的是
麦考酚酸是一种有效的免疫抑制剂,能有效地防止肾移植排斥,其结构简式如下图所示。下列有关麦考酚酸说法正确的是
A.分子式为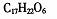
B.不能与 溶液发生显色反应
溶液发生显色反应
C.在一定条件下可发生加成、取代、消去反应
D.1 mol麦考酚酸最多能与3 tool NaOH反应
10.下列说法中正确的是
A.钠的金属性比镁强,故可用Na与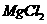 溶液反应制取金属镁
溶液反应制取金属镁
B.明矾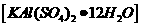 在水中能形成
在水中能形成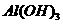 胶体,可用作净水剂 。
胶体,可用作净水剂 。
C.硬水含有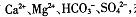 ,煮沸可以完全除去其中的
,煮沸可以完全除去其中的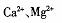
D.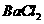 溶液能使含酚酞的
溶液能使含酚酞的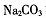 ,溶液红色褪去,原因是
,溶液红色褪去,原因是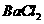 溶液呈酸性
溶液呈酸性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com