
题目列表(包括答案和解析)
18.含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是( )
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
B.x=0.6a,2Br-+Cl2=Br2+2Cl-
C.x = a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x = 1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
17.某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是( )
A.它是副族元素 B.它是第六周期元素
C.它的原子核内有63个质子 D.它的一种同位素的核内有89个中子
16.用足量的CO还原13.7 g某铅氧化物,把生成的CO2全部通到过量的澄清的石灰水中,得到的沉淀干燥后质量为8.0 g,则此铅氧化物的化学式是( )
A.PbO B.Pb2O3 C.Pb3O4 D.PbO2
15.可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是 ( )
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4OH-
B.以NaOH溶液为电解液时,负极反应为:Al+3OH--3e-=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
14.已知:2H2(g)+O2(g) = 2H2O(l);△H = -571.6 kJ•mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H = -890 kJ•mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3 695 kJ。则原混合气体中H2与CH4的物质的量之比是( )
A.1:1 B.1:3 C.1:4 D.2:3
13.水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+xOH- Fe3O4+S4O +2H2O,下列说法中,正确的是 ( )
A.每生成1mol Fe3O4,反应转移的电子总数为3mol
B.Fe2+和S2O 都是还原剂
C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol
D.可能有多组配平系数
12.为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g 样品加热,其质量变为w2 g ,则该样品的纯度(质量分数)是 ( )
 A.
A. 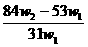 B.
B.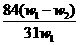 C.
C. 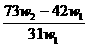 D.
D.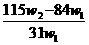
11. 已知中学化学中常见的反应形式为:A+B→C+D+H2O,对于该反应的下列叙述不正确的是 ( )
A.该反应可能是氧化还原反应 B.该反应可能是非氧化还原反应
C.C和D中有一种一定是盐 D.A和B不一定是酸或碱
10.下列有关物质检验的实验结论正确的是( )
|
选项 |
实验操作及现象 |
实验结论 |
|
A |
向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 |
该溶液中一定含有SO42 - |
|
B |
向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 |
该溶液中一定含有Fe2+ |
|
C |
将某气体通入品红溶液中,品红溶液褪色 |
该气体一定是SO2 |
|
D |
将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成 |
该物质一定属于醛类 |
9. X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y是核外电子数的一半,Y与M可形成化合物M2Y。下列说法正确的是( )
A.还原性:X的氢化物>Y的氢化物>Z的氢化物
B.简单离子的半径:M的离子>Z的离子>Y的离子>X的离子
C.YX2、M2Y都是含有极性键的极性分子
D.Z元素的最高价氧化物的水化物的化学式为HZO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com