
题目列表(包括答案和解析)
3.下列实验中,溶液颜色有明显变化的是
A.少量明矾溶液加入到过量NaOH溶液中
B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C.少量Na2O2固体加入到过量NaHSO4溶液中
D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
2.下列金属冶炼的反应原理,错误的是
A.2NaCl(熔融)通电2Na+Cl2↑ B.MgO+H2△Mg+H2O
C.Fe3O4+4CO高温3Fe+4CO2 D.2HgO△2Hg+O2↑
1.随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常加入抗氧化物质,下列不属于抗氧化物质的是
A.生石灰 B.还原铁粉 C.亚硫酸钠 D.维生素C
30.(16分)分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质在食品、
 化妆品等行业有广泛用途。
化妆品等行业有广泛用途。
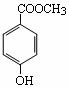
(1)C8H8O3的某一同分异构体尼泊金酯的结构简式如图。
① 下列对尼泊金酯的判断不正确的是______。
a.能发生水解反应 b.能与FeCl3溶液发生显色反应
c.分子中所有原子都在同一平面上 d.与浓溴水反应时,1 mol尼泊金酯消耗1 mol Br2
② 尼泊金酯与NaOH溶液在一定条件下反应的化学方程式是 ,
其中包含的反应类型有 、 。
(2)C8H8O3的另一种同分异构体甲满足以下条件:
① 与足量的NaOH溶液完全反应时,1 mol甲消耗3 molNaOH
② 遇FeCl3溶液显色
③ 苯环上的一氯取代物只有一种
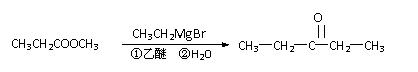 甲可能的结构简式是______
、______
_。
甲可能的结构简式是______
、______
_。
(3)已知:
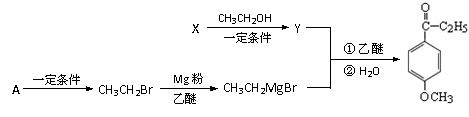 X也是C8H8O3的同分异构体。A在常温下呈气态,其产量是衡量一个国家石油化工水平的标志。
X也是C8H8O3的同分异构体。A在常温下呈气态,其产量是衡量一个国家石油化工水平的标志。
① 由A制CH3CH2Br的反应类型是_________。
② X→Y反应的化学方程式是_______ _ 。
29、(16分).某实验小组用下列装置进行乙醇催化氧化的实验。
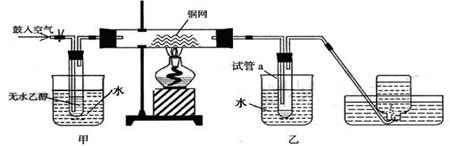
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应
是 反应。
⑵甲和乙两个水浴作用不相同。
甲的作用是 ;乙的作用是 。
⑶若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。
要除去该物质,可现在混合液中加入 (填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过 (填试验操作名称)即可除去。
28.(14分)A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:
(1)常温下,若A为气态单质,C为非金属氧化物,
A、C均能使品红溶液褪色,相对分子质量E﹥D,则:
该反应的反应方程式为 ,
检验D中阴离子的方法是 。
(2)若A为短周期的金属单质,D为气态单质,C溶液呈强酸性或强碱性时,该反应都能进行。写出反应的离子方程式 ; 。
(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的化学式(写两种) 、 。
写出生成E的一个离子方程式 。
27.
 (14分)X、Y、Z为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:Y+X 甲(g),Y+Z 乙(g)。甲、乙可化合生成离子化合物,甲的相对分子质量小于乙。
(14分)X、Y、Z为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:Y+X 甲(g),Y+Z 乙(g)。甲、乙可化合生成离子化合物,甲的相对分子质量小于乙。
(1)X的结构式是 。
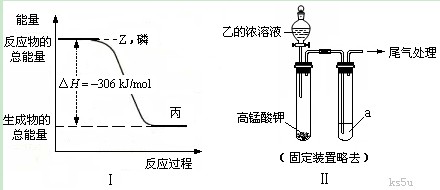
 (2)磷在Z气体中燃烧可生成液态丙分子,也可生成固态丁分子。已知丙分子中各原子最外层均是8电子结构,丙的电子式是 。磷单质和Z单质反应生成1 mol丙时,反应过程与能量变化如图Ⅰ所示,该反应的热化学方程式是 。
(2)磷在Z气体中燃烧可生成液态丙分子,也可生成固态丁分子。已知丙分子中各原子最外层均是8电子结构,丙的电子式是 。磷单质和Z单质反应生成1 mol丙时,反应过程与能量变化如图Ⅰ所示,该反应的热化学方程式是 。
(3)某同学拟用图Ⅱ所示装置证明氧化性Z>I2,已知高锰酸钾与乙的浓溶液反应生成Z,则a是 的水溶液。若仅将a换为甲的浓溶液,实验时会产生大量白烟并有气体单质生成,该反应的化学方程式是 。
(4)向一定浓度的BaCl2溶液中通入SO2气体,未见沉淀生成,若在通入SO2气体的同时加入由X. Y. Z| 中的一种或几种元素组成的某纯净物,即可生成白色沉淀,
 该纯净物可能是________、________。
该纯净物可能是________、________。
13.一定温度下,1 molX和n molY在容积为2 L的密闭容器中发生如下反应:
X(g)+Y(g) 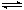 Z(g)+M(s),5 min后达到平衡,此时生成a molZ。下列说法正确的是
Z(g)+M(s),5 min后达到平衡,此时生成a molZ。下列说法正确的是
A.向平衡后的体系中加入1 molM,平衡向逆反应方向移动
B.用X表示此反应的反应速率是(0.1-0.1a) mol•(L•min)-1
C.向上述平衡体系中再充入1 molX,U (正)增大,U (逆)减小,平衡正向移动
D.当混合气体的质量不再发生变化时,说明反应达到平衡状态
II卷
12.某新型可充电电池,能长时间保持稳定的放电电压。该电池的总反应为:
|
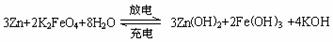
A.放电时负极反应为:Zn-2e–+2OH–=Zn(OH)2
B.放电时正极反应为: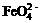 +4H2O+3e–=Fe(OH)3+5OH–
C.放电时每转移3 mol电子,正极有1 molK2FeO4被氧化
D.充电时阳极附近溶液的碱性减弱
+4H2O+3e–=Fe(OH)3+5OH–
C.放电时每转移3 mol电子,正极有1 molK2FeO4被氧化
D.充电时阳极附近溶液的碱性减弱
10.Fe3+、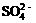 、Al3+和X四种离子以物质的量之比2:4:1:1大量共存于同一溶液中,
、Al3+和X四种离子以物质的量之比2:4:1:1大量共存于同一溶液中,
X可能是( )
A.Na+ B.OH– C.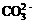 D.Cl–
D.Cl–
|
A.X、Y、Z、W均为非金属元素
B.X、Y、W的氢化物中,Y的氢化物沸点最高
C.Z的阳离子与Y的阴离子电子层结构相同
D.W元素的简单离子半径大于Z元素的简单离子半径
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com