
题目列表(包括答案和解析)
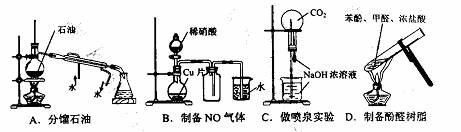
5.下列实验装置和操作中,正确的是 ( )
4.对下列事实的解释错误的是 ( )
A.用75%的乙醇溶液进行消毒,是由于乙醇能使蛋白质变性
B.医疗上用硫酸钡作“钡餐”,是由于硫酸钡难溶于水
C.用氢氟酸雕刻玻璃,是由于氢氟酸能与二氧化硅反应
D.向Na2O2与水完全反应后的溶液中加MnO2,产生O2,是由于该溶液中含H2O2
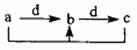
3.下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是 ( )
 物质 物质选项 |
a |
b |
c |
d |
|
A |
Al |
Al(OH)3 |
NaAlO2 |
NaOH |
|
B |
CH3CH2OH |
CH3CHO |
CH3COOH |
O2 |
|
C |
Na2CO3 |
NaHCO3 |
NaOH |
CO2 |
|
D |
Cl2 |
FeCl3 |
FeCl2 |
Fe |
2.下列化学用语正确的是 ( )
A.乙酸根离子的结构式: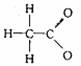
B.CO2分子的球棍模型:
C.3-甲基-1-丁烯的结构简式:(CH3)2CHCH=CH2
D.醛基的电子式: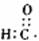
1.第十八届“世界水日”的主题是“关注水质、抓住机遇、应对挑战”。下列说法错误的是
( )
A.推广使用无磷洗衣粉主要是为了防止水体富营养化
B.日常生活中,常用加热煮沸的方法来降低硬水的硬度
C.利用ClO2对自来水消毒主要是因为ClO2具有强氧化性,能杀死水中的病菌
D.回收废旧电池主要是防止电池中的NH4Cl对水资源造成污染
20.(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两
个选修模块的内容。请选择其中一题作答。若两题都做,则按A题评分。
A.微粒A、B、C为分子,D和F为阳离子,E为阴离子,它们都含有lO个电子;B溶
于A后所得的物质可电离出D和E;C是重要的化石能源。将A、B和含F离子的物
质混合后可得D和一种白色沉淀。 离子与Ar原子的电子层结构相同。请回答:
离子与Ar原子的电子层结构相同。请回答:
(1)基态G原子的外围电子排布式是 。在A、B、C这三种分子中,属于非极
性分子的有 (写化学式)。
(2)下列有关B的说法中正确的是 。(填字母)
a.在配合物中可作为配体 b.该分子的稳定性与氢键有关
c.分子由各原子最外层均为8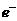 。的稳定结构
。的稳定结构
d.含1 mol B的液体中有3 mol氢键
(3)根据等电子体原理,D离子的空间构型是 ,其中心原子轨道的杂化类型
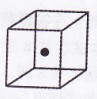 是 。
是 。
(4)构成C的中心原子可以形成多种单质,其中有一种为空间网状结
构,右图立方体中心的“●”表示该晶体中的一个原子,请在该
立方体的顶点上用“●”表示出与之紧邻的原子。
(5)光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中
不存在 。(填字母)
a.金属键 b.离子键 c.非极性键 d.极性键
f.配位键 g. 键 h.
键 h.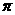 键
键
B.对氨基苯磺酸是制取某些染料和药物的重要中间体,可由苯胺磺化得到:
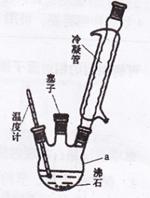

实验室可用苯胺、浓硫酸为原料,利用右图所示实验装置合成。
实验步骤如下:
①取一个250mL的仪器a,加入10mL苯胺及几粒沸石,
放人冷水中冷却,小心地加入18 mL浓硫酸。再分别
装上冷凝管、温度计等。
②将a置于油浴中缓慢加热至170`180℃,维持此温度约2.5 h。
③将反应产物冷却至约50℃后,倒入盛有100 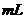 ,冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出。用该烧杯中的少量冷水将a内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到粗产品。
,冷水的烧杯中,用玻璃棒不断搅拌,促使晶体析出。用该烧杯中的少量冷水将a内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到粗产品。
④将粗产品用沸水溶解,冷却结晶(若溶液颜色过深,可用活性炭脱色),抽滤,收集
产品,晾干。(提示:100mL水在20℃时可溶解对氨基苯磺酸1.08 g,在100℃时可
溶解6.67 g)
(1)仪器a的名称是 。步骤①中加入沸石的作用是 。
(2)步骤②中采用油浴加热,下列说法正确的是 。(填字母)
A.便于控制温度 B.也可以改用水浴加热 C.温度计的水银球也可浸在油中
(3)步骤③用冷水洗涤的优点是 。
(4)步骤③和④均进行了抽滤操作,在抽滤完毕停止抽滤时,应注意先一二,然
后 。
(5)步骤④有时需重复进行多次,其目的是 。
19.(10分)硫酸在生产中有广泛的应用,某厂以硫铁矿为主要原料生产硫酸。
已知:①550℃时,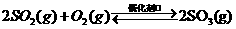
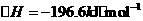
②一定温度下,硫铁矿在空气中煅烧可能发生下列反应(设空气中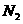 与
与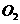 的体积
的体积
比为4:1):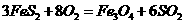 ,
,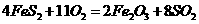
(1) 550℃时,6.4 g 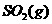 与足量
与足量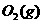 充分反应生成
充分反应生成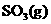 ,放出热量
,放出热量
9.83 kJ
(填“大于”、“等于”或“小于”)o
(2)欲使反应①的平衡向正反应方向移动,下列措施可行的是 。(填字母)
a.向平衡混合物中充入 b.向平衡混合物中充入
b.向平衡混合物中充入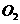
c.改变反应的催化剂 d.降低反应的温度
(3)为使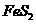 完全生成
完全生成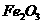 ,生产时要使用过量的
,生产时要使用过量的
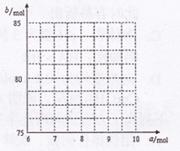 空气,则当空气过量50%时,所得炉气中
空气,则当空气过量50%时,所得炉气中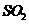 的
的
体积分数是多少?
(4)720 g纯净的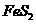 在空气中完全煅烧,所得固体
在空气中完全煅烧,所得固体
中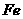 和
和 的物质的量之比n(
的物质的量之比n(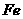 ):n(
):n( )=6:
)=6: 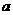 ,
,
此时消耗空气为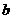 mol。
mol。
①试写出易与口的关系式: 。
②请在右图中画出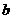 与
与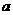 的关系曲线。
的关系曲线。
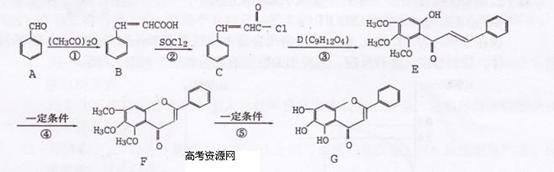
18.(12分)化合物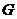 是中药黄芩中的主要活性成分之一,具有抗氧化和抗肿瘤作用。
是中药黄芩中的主要活性成分之一,具有抗氧化和抗肿瘤作用。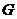 的
的
合成路线如下:
请回答下列问题:
(1)G中含有的含氧官能团的名称有 。
(2)反应③为取代反应,D的结构简式是 ,D分子中含有 种不同化
学环境的氢原子。
(3)同时符合下列a、b、c三个条件的B的同分异构体共有 种。
a.能发生银镜反应;b.属于苯的衍生物,苯环上共有3个链状取代基;c.与
FeCl3溶液发生显色反应
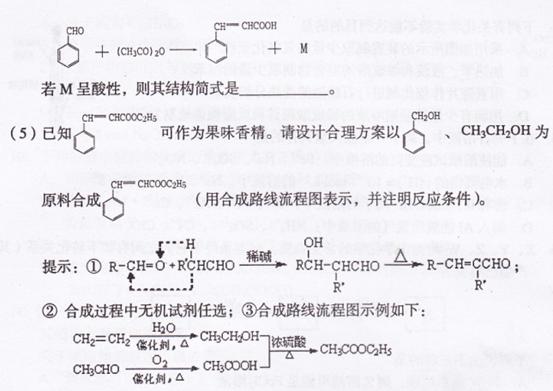
(4)反应⑤的反应类型是 。在反应①中,反应物的物质的量之比为1:l,
反应的化学方程式如下:
17.(10分)近年,我国在航天事业上取得了令世界瞩目的成就,神舟飞船多次被长征系
列火箭送入太空。
(1)长征二号捆绑式火箭推进剂以联氨(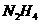 )作为燃料,
)作为燃料,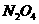 作为推进剂。
作为推进剂。
①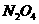 的主要作用是助燃,但其在工作时会产生红棕色气体
的主要作用是助燃,但其在工作时会产生红棕色气体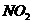 ,对环境会造
,对环境会造
成污染,为避免污染可使用下列 (填字母)代替之。
A.液态氨 B.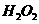 C.
C.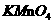 D.液态氧
D.液态氧
②在碱性条件下,用尿素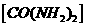 和次氯酸钠反应可以制取联氨(产物中
和次氯酸钠反应可以制取联氨(产物中
同时有两种正盐),则该反应的离子方程式是 。
(2)飞船座舱内空气的更新过程如下图所示:
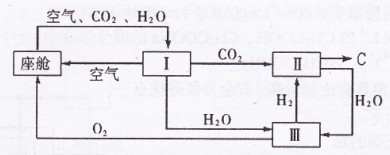
①座舱内空气更新过程可以循环利用的物质为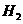 、
、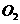 和 ;装置Ⅱ中
和 ;装置Ⅱ中
发生反应的化学方程式为 。
②从装置I、Ⅱ、Ⅲ可看出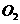 的来源,若宇航员每天消耗35mol
的来源,若宇航员每天消耗35mol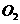 ,每天呼出
,每天呼出
的气体中含18 mol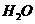 ,则呼出的气体中含
,则呼出的气体中含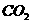 mol.
mol.
16.(10分)大气固氮属于自然固氮,合成氨是目前人工固氮的主要方法。科学家一直致
力“人工固氮”新方法的研究。
(1)有关大气固氮(以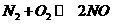 为例)、人工固氮(以
为例)、人工固氮(以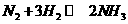 为
为
例)反应的平衡常数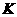 的值如下表。
的值如下表。
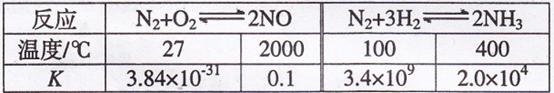
下列说法正确的是 填字母
a.大气固氮与人工固氮都是放热反应 b.人类模拟大气固氮无现实意义
c.寻找在常温下合成氨的高效催化剂是目前人工固氮的新方向
d.在常温下,人工固氮非常容易进行
(2)已知: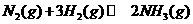
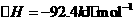
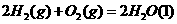
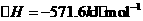
据报道,在常温、常压、光照、催化剂的条件下,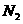 可以与水反应,则反应
可以与水反应,则反应
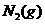 +
+ =
=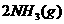 +3/2
+3/2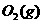 的
的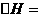

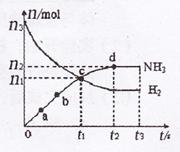 (3)某研究小组在673 K、30 MPa下,在体积为
(3)某研究小组在673 K、30 MPa下,在体积为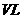 的
的
密闭容器中进行反应: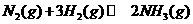 ,
,
其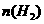 和
和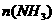 随时间变化的关系如图所示。
随时间变化的关系如图所示。
①下列叙述正确的是 填字母
A.点a的正反应速率比点b的大
B.点c处反应达到化学平衡状态
C.若如时由673 K升至773 K,则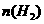 将增大
将增大
②从开始到平衡时反应的平均速率(以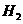 的浓度变化表示)v(
的浓度变化表示)v(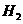 )= .
)= .
③若开始时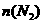 =
=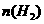 ,则反应的平衡常数K= (用代数式表示).
,则反应的平衡常数K= (用代数式表示).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com