
题目列表(包括答案和解析)
2.下列有关化学用语的表述正确的是
A.乙烯的结构式 CH2=CH2 B.苯的分子比例模型
C.NaOH的电子式 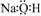 D.纤维素的分子式 C6H10O5
D.纤维素的分子式 C6H10O5
1.下列有关环境保护的说法中,不正确的是
A.劣质装修材料中的甲醛、苯等对人体有害
B.工业生产大量排放二氧化硫是全球气候变暖的主要原因
C.含氮、磷化合物的生活污水大量排放会使水体富营养化
D.废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染
12. (14分) 某化学兴趣小组欲验证:“铜和一定量的浓硝酸反应有一氧化氮产生”。设计使用了如下装置进行实验。(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)
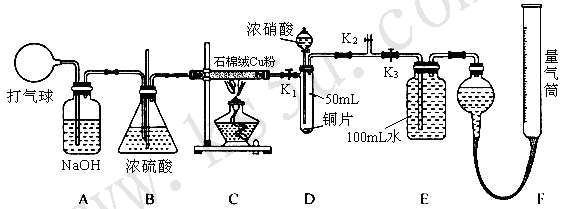
试回答下列问题:
(1) 将铜粉分散在石棉绒中的原因是___________________________________。
(2) 在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体主要成分是_________(填化学式),通入该气体的目的是__________________________;进行此步操作时应关闭_________,打开_________ (填K1、K2或K3)。
(3) 关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。则D中一定发生反应的离子方程式为:_______________________________________________________________________。
(4) 若E中出现倒吸,可采取的应急操作是_________________________________。
(5) I.从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000 mol·L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为__________________ mol·L-1。
Ⅱ.若实验测得F装置所收集到的气体体积为139.00 mL,则铜和一定量的浓硝酸反应___________(填“有”或“无”)NO生成,其依据是(请用数据和文字说明)__________________________________________________________________________________________________________________________________________________________________________________________________________________________。
11. (15分) 已知①-④均为工业生产及应用的常见反应。其中常温下B、D、J、P气体,E为分子中原子个数比为1∶l的液体。A的相对分子质量为120。(个别反应的产物已略去)
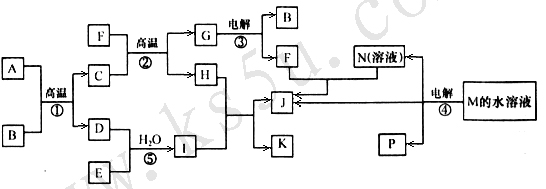
试回答下列问题:
(1) 反应F与N溶液反应的离子方程式为_____________________________________;
(2)
 反应⑤中当有1mol电子转移时,氧化剂消耗
g。
反应⑤中当有1mol电子转移时,氧化剂消耗
g。
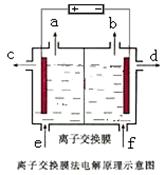
(3) 反应④的离子方程式为______________________________;
右图是该反应原理的示意图,该装置中使用的是 (填“阴”或“阳”)离子交换膜。图中从d处收集到的是 。
(4)
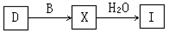 工业上由D制取I的过程可表示为:
工业上由D制取I的过程可表示为:
由D与B反应生成X的反应所用的设备是
①高炉 ②沸腾炉 ③接触室 ④分馏塔 ⑤吸收塔
已知400℃ 101Kpa时,2D(g) + B(g) 2X(g);△H = – 196.6KJ/mol,当2 mol D与1 mol B在该条件下反应达平衡时反应放热186.8
KJ。
2X(g);△H = – 196.6KJ/mol,当2 mol D与1 mol B在该条件下反应达平衡时反应放热186.8
KJ。
在实际生产中综合考虑各种因素,为提高D的转化率,工业选择了以下哪些条件______
①适当升高温度 ②增大压强 ③使用合适的催化剂 ④及时移走生成物 ⑤适当增大B的浓度 ⑥将反应物与生成物在热交换器中进行热交换
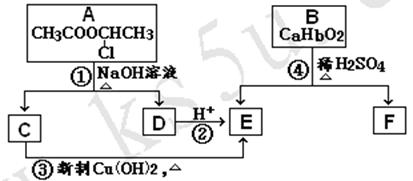
10. (共15分) 请根据下图作答:
已知:一个碳原子上连有两个羟基时,易发生下列转化:
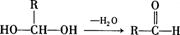
(1) 反应①所属的有机反应类型是_______________反应。
(2) 反应③的化学方程式__________________________________________________。
(3) 已知B的相对分子质量为162,其完全燃烧的产物中n(CO2)∶n (H2O) = 2∶1,则B的分子式为 。
(4) F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(5) 化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G的结构有 种。
(6)
化合物H是B的同分异构体,H分子中含有的部分结构为 ,它的水解产物经聚合反应后可得到高聚物(CaHbO2)n.。H有多种结构,写出其中一种的结构简式 。
,它的水解产物经聚合反应后可得到高聚物(CaHbO2)n.。H有多种结构,写出其中一种的结构简式 。
9. (16分) A、B、C、D、E、F属于短周期主族元素。A的原子半径在短周期中最大,B的一种原子中,质量数与质子数之差为零, C与D、E与F均同主族,C元素的原子L层电子数是K层的2倍,E原子的核外电子总数等于C、D原子核外电子总数的差。
(1) 离子B-的结构示意图为 ;化合物CE2的分子属于 分子(填“极性”或“非极性”);用电子式表示化合物A2F的形成过程 。
(2) A、E、F形成的简单离子的半径由大到小的顺序为 (用离子符号表示);
元素C、D、E形成的常见单质中,熔沸点由高到低的顺序是(用名称表示)
(3) 由B、C可以构成的最简单的化合物W,取16.0g分子式为W·8H2O的化合物,将其释放的W完全燃烧生成液态水,可放出89.03kJ的热量,则W燃烧的热化学方程式为
(4) 使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一。有人设计制造了一种燃料电池,一个电极通入富含E单质的气体和少量CE2,另一电极通入液化石油气(以C4H10表示),电池的电解质是熔融的K2CO3。该电池的负极反应式为 ,电池工作时,电解质里的CO32-向 极移动。
8.
可逆反应A(g) + 3B(g)  2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是( )
2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是( )
A.甲中A的转化率为75%
B.甲、乙中C的体积分数相同
C.平衡后再向乙中加入0.25 mol A、0.75 mol B、1.5 mol C,平衡向生成C的方向移动
D.乙中的热化学反应方程式为2C(g) A(g)+3B(g);△H=+3Q2 kJ·mol-1
A(g)+3B(g);△H=+3Q2 kJ·mol-1
第Ⅱ卷 非选择题(共174分)
7. 下列关于电解质溶液中离子关系说法中错误的是( )
A.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:
c(NaOH) < c(Na2CO3) < c(CH3COONa)
B.pH = 2的HA溶液与pH = 12的MOH溶液任意比混合:
c(H+) + c(M+) = c(OH-) + c(A-)
C.在pH=13的Na2S溶液中,Al3+、Cl-、CH3COO-不能大量共存
D.由水电离出的氢离子浓度为10-1mol/L的溶液中,SO32-、NO3-、Cl-、Na+可能大量共存
6. 下列反应的离子方程式正确的是( )
A.碳酸钙溶于醋酸中:CaCO3 + 2H+= Ca2++ H2O + CO2↑
B.硫化钠溶液中加入硫酸铜溶液:S2-+ Cu2++ 2H2O = Cu(OH)2↓+ H2S↑
C.氢氧化钠溶液中加入少量碳酸氢钡溶液:
Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O
D.亚硫酸钠的水解:SO32-+ H2O = HSO3-+ 2OH-
5. 下列关于短周期元素说法正确的是( )
①均为主族元素,除稀有气体外,最高化合价与其族序数相等
②元素所形成的单质可能是金属晶体、分子晶体、离子晶体或原子晶体
③元素的氢化物水溶液可能显酸性,也可显碱性
④元素气态氢化物的沸点随相对分子质量增大而增大
A.①②③④均不正确 B.只有①②③正确
C.只有③④正确 D.只有③正确
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com