
题目列表(包括答案和解析)
7.对0.1mol·L-1的醋酸溶液进行以下操作,下列分析判断正确的是
A.加入少量0.1mol·L-1的硫酸,水电离产生的c(H+)减小
B.升高温度,溶液的pH会增大
C.加入少量固体NaOH,溶液中c(CH3COO-)+c(OH-) > c(Na+)+c(H+)
D.与0.1mol·L-1的NaOH溶液等体积混合后,溶液中c(CH3COO-) =c(Na+)
6.下列物质中不能通过置换反应生成的是
A.F2 B.CO C.Fe 3O4 D.S
30.(18分)目前世界上已证明“达菲”是治疗甲型H1N1流感的良方。在卫生部公布的诊疗方案中 称,在发热48小时内使用达菲有效,36小时内使用最佳。达菲的生产原材料是八角中
称,在发热48小时内使用达菲有效,36小时内使用最佳。达菲的生产原材料是八角中 所含的一种重要成分莽草酸。从八角茴香中
所含的一种重要成分莽草酸。从八角茴香中 提取的莽草酸经过多次反应和其他工艺制成“达菲”颗粒。下图是莽草酸和“达菲”有效成分的键线式结构(楔形实线、虚线表示基团的立体结构)。
提取的莽草酸经过多次反应和其他工艺制成“达菲”颗粒。下图是莽草酸和“达菲”有效成分的键线式结构(楔形实线、虚线表示基团的立体结构)。
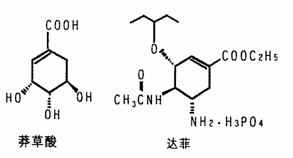 ⑴“达菲”的相对分子质量为410.4,扣除H3PO4后的部分A称为“自由基奥司他韦”。A的相对分子质量_____;写出A在一定条件下水解的化学方程式
。
⑴“达菲”的相对分子质量为410.4,扣除H3PO4后的部分A称为“自由基奥司他韦”。A的相对分子质量_____;写出A在一定条件下水解的化学方程式
。
⑵莽草酸中 含有的官能团有_______________(写名称)。
含有的官能团有_______________(写名称)。
⑶下列有关莽草酸的说法中 正确的是_______________________________。(填写序号)
正确的是_______________________________。(填写序号)
①分子式为C7H10O5 ②能使FeCl3溶液显紫色③能使溴的四氯化碳溶液褪色 ④ lmol莽草酸与足量的Na、NaOH和NaHCO3反应,消耗的Na、NaOH和NaHCO3的物质的量之比为4:l:1 ⑸莽草酸具有两性(酸性与碱性)⑥莽草酸可以发生消去反应、氧化反应、酯化反应和加成反应
⑷ 以下是以莽草酸为原料的有机合成路线。其中
以下是以莽草酸为原料的有机合成路线。其中 物质D的碳环上的一氯代物只有两种。
物质D的碳环上的一氯代物只有两种。
①C有三种可能的结构,写出其中 任意一种的结构简式______________________。
任意一种的结构简式______________________。
②写出所有符合条件的D(A.遇FeCl3溶液显紫色 B.可以发生水解反应)的同分异构体的结构简式: 。
③写出下列反应的化学方程式: D与足量的NaOH溶液反应___________________。
29.(16分)各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中 两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中
两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中 X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。
X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板。
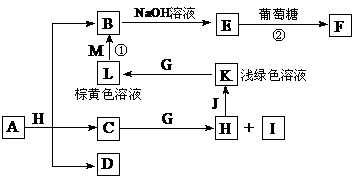
请回答下列问题:
(1)写出A的化学式______________,I的电子式______________。
(2)M的硝酸盐水溶液显酸性,用离子方程式解释原因 。
(3)写出反应②的化学方程式(有机物用结构简式表示) ___________________,
(4)写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
(5)G单质所含元素的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出Q KJ的热量。写出该反应的热化学方程式:________。
28.(15分)某工业铁红中 混有一种黑色的铁的氧化物杂质,为了解杂质的成分及测定铁红的纯度,化学兴趣小组的同学进行了实验探究。请你参与过程分析与交流。
混有一种黑色的铁的氧化物杂质,为了解杂质的成分及测定铁红的纯度,化学兴趣小组的同学进行了实验探究。请你参与过程分析与交流。
[查阅资料]
①铁的常见氧化物氧化亚铁(FeO)黑色固体,ω(Fe)=77.8%; 氧化铁(Fe2O3)红色固体,俗称铁红,ω(Fe)=70.0%;四氧化三铁(Fe3O4)黑色固体,俗称磁性氧化铁,ω(Fe)=72.4%。
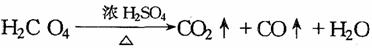 ②草酸(乙二酸H2CO4)在浓H2SO4存在下受热分解的化学方程式为:
②草酸(乙二酸H2CO4)在浓H2SO4存在下受热分解的化学方程式为:
[实验准备]
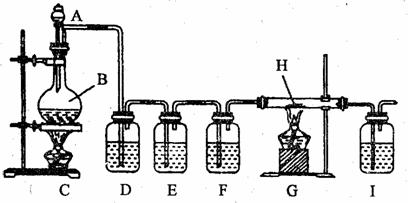
①实验的装置图如下
②药品及试剂
a、草酸 b、工业铁红 c、NaOH溶液 d、澄清石灰水 e、浓H2SO4 f、盐酸
[实验及数据]
取不同质量的样品进行实验,所得实验数据如下:
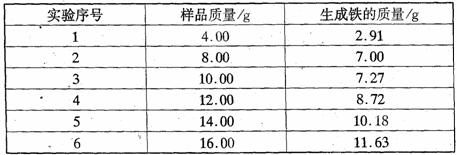
[讨论与分析]
(1)兴趣小组的同学拟以纯净的CO还原铁的氧化物,所设计的实验装置中 D、E、F应分别盛放的试剂为 、 、
、(填写序号,下同),其作用依次是
。
D、E、F应分别盛放的试剂为 、 、
、(填写序号,下同),其作用依次是
。
上述装置还有不完善之处,你建议改进措施是
(2)由实验数据不难得出,有-组实验数据不可靠,该组数据是 (填序号),该工业粗铁红所含杂质的化学式为 。
(3)该工业铁红中 ω(Fe2O3)=
。
ω(Fe2O3)=
。
13.在体积一定的密闭容器中 给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)
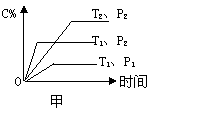
给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)  xC(g),符合下图甲所示的关系(c%表示平衡混合气体中
xC(g),符合下图甲所示的关系(c%表示平衡混合气体中 产物C的百分含量,T表示温度,p表示压强)。则图乙中
产物C的百分含量,T表示温度,p表示压强)。则图乙中 y轴是指
y轴是指
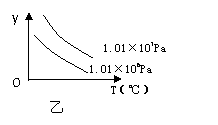
A.C的转化率
B.平衡混合气中 B的百分含量
B的百分含量
C.平衡混合气的平均相对分子质量 D.平衡混合气的密度
12. 快乐是什么?精神病学专家通过实验发现:在大脑的相应部位--“奖赏中
快乐是什么?精神病学专家通过实验发现:在大脑的相应部位--“奖赏中 心”,给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中
心”,给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中 心”部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中
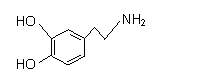
心”部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中 心”又称为多巴胺系统。多巴胺结构如右图,下列说法错误的是
心”又称为多巴胺系统。多巴胺结构如右图,下列说法错误的是
A. 多巴胺分子式为C8H11NO2
B. 多巴胺可以发生加成、取代、氧化反应
C. 和溴水反应时,1mol多巴胺可以消耗6mol溴单质
D. 多巴胺既可与强酸反应,又可以与强碱反应
11. 著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。稀土元素铈(Ce)主要存在于独居石中 ,金属铈在空气中
,金属铈在空气中 易氧化变暗,受热时燃烧,遇水很快反应。
易氧化变暗,受热时燃烧,遇水很快反应。
已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2。下列说法正确的是
A. 铈溶于氢碘酸的化学方程式可表示为:Ce
+ 4HI  CeI4 + 2H2↑
CeI4 + 2H2↑
B. 在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得铈
C. 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4+ + 2Fe2+ == Ce3+ + 2Fe3+
D. 四种稳定的核素136 58Ce、138 58Ce、140 58Ce、142 58Ce,它们互称为同系物
10.下列在限定条件溶液中 的各组离子,能够大量共存的是
的各组离子,能够大量共存的是
A.pH=3 的溶液:Na+、Cl-、Fe2+、ClO-
B.与Al能产生氢气的溶液:K+、SO 、CO
、CO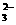 、NH4+
、NH4+
C.使酚酞试液变红的溶液:Na+、Cl-、SO 、Al3+
、Al3+
D.水电离的H+浓度为1×10-12mol·L-1的溶液:K+、Ba2+、Cl-、Br-
9.下列离子方程式正确的是
A.碳酸氢钠溶液与足量的氢氧化钡溶液混合:HCO3- + Ba2++OH- = BaCO3↓+H2O
B.Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
C.铜溶于浓硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO↑+ 4H2O
D.向氯化铝溶液中 滴加氨水:Al3+ + 3OH-=
Al(OH)3↓
滴加氨水:Al3+ + 3OH-=
Al(OH)3↓
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com