
题目列表(包括答案和解析)
5.常温下,有甲、乙两份体积均为1L,pH均为3的溶液,其中甲为醋酸,乙为盐酸。①甲用蒸馏水稀释至100倍后,溶液的pH变为a;②乙与等体积、浓度为0.01mol/L的氨水混合,在此混合液中:n(NH4+)+n(H+)-n(OH-)= bmol。则a、b正确的答案组合是 ( )
A.3~5之间;0.0005 B.3~5之间;0.001
C.5;0.0005 D.5;0.001
4.用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.32g氧气和臭氧的混合气体中含有的氧原子数为2NA
B.标准状况下,22.4LCH3CH2Br中所含分子数为NA
C.0.1molH3O+所含质子数为NA
D.0.1molFe和足量的稀硝酸充分反应,转移电子数为0.2 NA
3.下列各组离子中,加入盐酸或NaOH溶液都能大量共存的离子组是 ( )
A.Al3+、K+、HC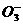 、
、 B. Na+、Cl-、SO42- 、
B. Na+、Cl-、SO42- 、
C.Na+ 、 、
、 、
、 D.Na+ 、K+、Fe2+、NO3-
D.Na+ 、K+、Fe2+、NO3-
2.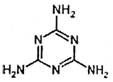 2008年9月的“结石宝宝”事件主要是婴儿饮用了添加有三聚氰胺的奶制品导致的肾结石和输尿管结石。三聚氰胺是一种用途广泛的基本有机化工中间产品,长期服用该物质后会引起肾衰竭。其结构式如右图:
2008年9月的“结石宝宝”事件主要是婴儿饮用了添加有三聚氰胺的奶制品导致的肾结石和输尿管结石。三聚氰胺是一种用途广泛的基本有机化工中间产品,长期服用该物质后会引起肾衰竭。其结构式如右图:
下列关于三聚氰胺的说法不正确的是 ( )
A.三聚氰胺是劣质蛋白质
B.三聚氰胺中氮元素的含量高于蛋白质中氮的含量
C.三聚氰胺在一定条件下可能会与氢气发生加成反应
D.三聚氰胺的化学式为C3H6N6
1.2007年10月24日我国“嫦娥一号”探月火箭发射升空,这标志中国实施绕月探测工程迈出重要一步。其任务之一是开展月面的微波辐射探测,估算月壤中3He的分布和资源量。以下关于3He的说法正确的是 ( )
A.是4He 的同素异形体 B.比4He 少一个电子
C.是4He 的同位素 D.比4He少一个质子
29.(14分)为探究浓硫酸的性质,设计如下图所示装置。检查好装置的气密性后,向烧瓶中加入过量的铁粉、碳粉,再从分液漏斗中滴加浓硫酸。

(1)A装置不加热时,B中无明显现象,这是因为:
。
(2)加热后,在C处的现象是_______________________________________________。
反应一段时间后,发现铁粉继续溶解,仍然有气体生成,在E处点燃,观察到淡蓝色火焰。写出A中可能发生的两个反应的离子方程式: 、 。
(3)反应结束后,安装好过滤装置。先用热水通过过滤器,以提高其温度,再将烧瓶中的溶液趁热过滤。将滤液转移到锥形瓶中,用胶塞塞住瓶口,静置、冷却。测得析出硫酸亚铁晶体2.69 g。将全部晶体转入硬质玻璃管,高温加热至质量不变,测得生成SO2 0.112 L (已换算为标准状况)。
已知:2(FeSO4·xH2O) Fe2O3+SO2↑+SO3↑+2x
H2O
Fe2O3+SO2↑+SO3↑+2x
H2O
①提高过滤器温度的目的是 ;
②用胶塞塞住瓶口的目的是 ;
③求该晶体中所含结晶水的数目x = 。(保留两位有效数字)
28.(18分)肉棒酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。请回答:
(1)质谱法测定肉桂酸甲酯(H)的相对分子质量不超过200。已知H中氧元素的质量分数为19.75%,则其分子式为 。
(2)已知肉桂酸甲酯(H)分子中只含有一个苯环,且苯环上只有一个取代基。实验表明,H能使溴的四氯化碳溶液褪色。氢核磁共振谱表明H分子中含有六种环境不同的氢原子。请写出H的结构简式 。
(3)用芳香烃A为原料合成肉桂酸甲酯(H)的路线如下:

①化合物F中含有的官能团为 (填名称)
②B→C的反应类型是 ,F→G的反应类型是 。
③写出下列反应的化学方程式:
F→I:
G→H:
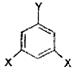
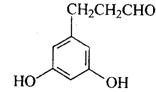
④F的同分异构体甚多,其中有一类可用通式表示(其中X、Y均不为氢),试写
出符合上述通式,能发生银镜反应且能与金属钠反应的物质共有三种,写出剩余两种物质的
结构简式:
 、
、
。
、
、
。
27.(12分)KMnO4是一种常用的强氧化剂,工业上可以用软锰矿(主要成分为MnO2)为原料,通过液相法生产,即在碱性条件下用氧气氧化MnO2得到K2MnO4,分离后得到K2MnO4;再用铂板作阳极,铁作阴极电解K2MnO4溶液得到KMnO4。简略生产过程如下图所示:
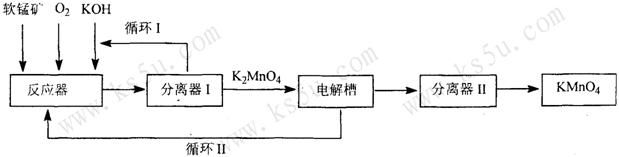
回答下列问题:
(1)写出反应器中发生反应的化学方程式 。
(2)写出电解槽中阳极的电极反应式 。
(3)循环Ⅰ、Ⅱ中利用的共同物质是 。
(4)将所得KMnO4配成0.1000 mol·L KMnO4溶液(用少量硫酸酸化),滴定20.00 mL未知浓度的H2C2O4溶液,判断达到滴定终点的依据是
。实际消耗KMnO4溶液20.00 mL,则H2C2O4溶液的浓度为
mol·L
KMnO4溶液(用少量硫酸酸化),滴定20.00 mL未知浓度的H2C2O4溶液,判断达到滴定终点的依据是
。实际消耗KMnO4溶液20.00 mL,则H2C2O4溶液的浓度为
mol·L 。
。
(已知: )
)
26.(16分)有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,其中A元素组成的单质是密度最小的物质,E元素是地壳中含量最多的金属元素。已知C、F同主族,C元素原子最外层电子数是其内层电子数的3倍,D元素原子核内质子数是B元素原子核内质子数的2倍。
请回答下列问题:
(1)单质D可在化合物甲中燃烧得单质B和化合物乙。请写出D在周期表中的位置 ;化合物甲固态时属于 晶体(填晶体类型);乙的电子式为 。
(2)A、B两元素可形成一种正四面体分子丙,右图是25℃、101kPa下,1 mol丙燃烧生成稳定化合物过程中能量变化示意图,
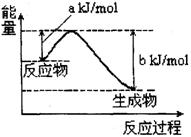 其热化学方程式为:
其热化学方程式为:
。
(3)C、F两元素可形成气态化合物丁(FC2)。
现有两个体积相同的密闭容器Ⅰ和Ⅱ,
向l中充入1 mol 丁和1 mol单质C2,
Ⅱ中充入2 mol 丁和2 mol单质C2,加
入催化剂使之发生反应,保持温度和容
器体积不变,则达到平衡时两容器中丁的转化率:Ⅰ Ⅱ(填>、<或=)。
(4)化合物X、Y、Z分别是B、E、F三种元素对应的最高价含氧酸的钠盐,X、Y溶液呈碱性,Z的溶液pH<7。
①Z的化学式为 ;
②Y、Z两溶液混合反应得到一种透明溶液W,其反应的离子方程式为
;向W溶液中加入X溶液,会产生白色沉淀和无色气体,请写出反应的离子方程式 。
13.氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生
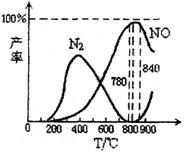 主反应①和副反应②,有关物质产率与温度的关系如右图。
主反应①和副反应②,有关物质产率与温度的关系如右图。
① ;
;

② ;
;

下列说法中不正确的是
A.加压有利于NH3生成NO,不利于NH3生成N2
B.工业上通常提高氧气的浓度,以提高NH3的转化率
C.工业上氨催化氧化生成NO时,温度应控制在780-840℃之间
D.N2(g)+O2(g) 2NO(g);△H
= +181.5kJ/mol
2NO(g);△H
= +181.5kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com