
题目列表(包括答案和解析)
7.一种从植物中提取的天然化合物a-damascone,可用于制作“香水”,其结构为:,
 有关该化合物的下列说法不正确的是
有关该化合物的下列说法不正确的是
 A.分子式为C13H20O
A.分子式为C13H20O
B. 该化合物可发生聚合反应
C.1 mol该化合物完全燃烧消耗19mol02
mol该化合物完全燃烧消耗19mol02
D.与溴的CCl4 溶液反应生成的产物经水解、稀硝酸酸化后可用AgNO3溶液检验
10.(14分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生资源,具有广泛的开发和应用前景。请按要求回答下列问题:__________________________________________
(1)工业上一般采用下列两种反应合成甲醇:
反应I:

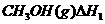
反应II: 


上述反应符合绿色化学“原子经济”的是__________________________________
下表所列数据是反应I在不同温度下的化学平衡常数(K)。
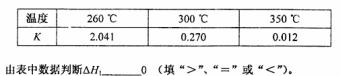
某温度下,将2molCO和6molH 充入2L的密闭容器中,充分反应,2分钟达到平衡后,测得c(CO)=0.2mol/L,则V(H
充入2L的密闭容器中,充分反应,2分钟达到平衡后,测得c(CO)=0.2mol/L,则V(H )=_____________,CO的转化率为__________,此时温度约为_______________℃。
)=_____________,CO的转化率为__________,此时温度约为_______________℃。
(2)已知在常温压下:

写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
_____________________________________________________________________
(3)某实验小组依据甲醇燃烧的反应原理,设计如下图所示的电池装置。
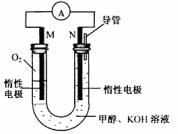
该电池正极的电极反应式为__________________________________________
工作一段时间后,U形管中溶液PH逐渐(填:“变大”、“变小”或“不变”)
该电池反应还原剂的化学式为________________________________________
当其3.2g时,将有____________mol电子转移。
河西区2009-2010学年度第二学期高三年级总复习质量调查(一)
9.(18分)某化学兴趣小组的同学利用下图所示实验装置进行实验(图中abcd表示止水夹)。请按要求回答下列问题:

I.某同学用浓盐酸和MnO 加热反应抽取氯气时,需选用以上装置(填字母,除杂质和干燥装置略)__________________、C:还需补充装置E,请在右上方方框内装置简图,并标注其所盛药品的名称。若用此套实验装置比较Cl
加热反应抽取氯气时,需选用以上装置(填字母,除杂质和干燥装置略)__________________、C:还需补充装置E,请在右上方方框内装置简图,并标注其所盛药品的名称。若用此套实验装置比较Cl 和Br
和Br 的还原性强弱,需在装置C中盛装药品的名称是____________________________________
的还原性强弱,需在装置C中盛装药品的名称是____________________________________
II.用浓硝酸和铜片反应制备NO 气体时,应选用以上装置(填字母)______________________
气体时,应选用以上装置(填字母)______________________
发生反应的化学方程式为____________________________________________________
(1)简述检验该装置气密性的方法:__________________________________________ 说明装置不漏气。
(2)欲用D装置验证试管甲中的NO 能与水(滴有石蕊试液)反应,其操作步骤为①关闭止水夹(填字母)_________,②打开止水夹(填字母)__________,③然后(填操作)__________________
,至水中有气泡冒出;随后可观察到水倒流入试管甲,其中发生反应的化学方程式为___________________________________________________________
能与水(滴有石蕊试液)反应,其操作步骤为①关闭止水夹(填字母)_________,②打开止水夹(填字母)__________,③然后(填操作)__________________
,至水中有气泡冒出;随后可观察到水倒流入试管甲,其中发生反应的化学方程式为___________________________________________________________
__________________________________________________________________________
(3)欲使试管甲中收集满的NO (标准状况下)尽可能多地被水吸收,需要进行的操作是________________________________________________________________。直至试管甲中全部充满水(假设水不外溢),所得溶液中溶质的物质的量浓度是________________mol·L
(标准状况下)尽可能多地被水吸收,需要进行的操作是________________________________________________________________。直至试管甲中全部充满水(假设水不外溢),所得溶液中溶质的物质的量浓度是________________mol·L
 。
。
8.(18分)乙偶姻是一种重要的香料。已知乙偶姻中只含有C、H、O原子个数比为2:4:1。请按要求回答下列问题:
I(1 )乙偶姻的分子式为______________________________________
(2)X是乙偶姻的同分异构体,且X属于酯类,其结构简式可能有________种,请写出X的一种结构简式_______________________________________________
II与乙偶姻有关的反应如下:
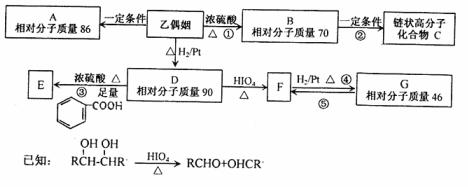
(3)乙偶姻除含有碳氧双键外,还含有的官能团名称是____________________________
写出①④的反应类型_______________________________
G的名称_______________________________________________
(4)A核磁共振氢谱仅有一种类型氢原子的吸收峰,其结构简式是___________________
(5)写出②③的化学反应方程式
_______________________________________________________________________
________________________________________________________________________
(6)设计实验检验F中的官能团:_____________________________
操作方法____________________________________________________________
现象_________________________________________________________________
结论__________________________________________________________________
7.(14分)现有部分短周期元素的性质、原子结构或物质用途如下表所述:

(1)写出由元素X与W且仅含离子键的化合物的电子式:
_______________________________________________________________
(2)Z单质的化学式为____________;含元素Z、Y的10电子阳离子的氯化物水溶液呈酸性,用离子方程式表示其原因:______________________________________
(3)下图为几种中学常见的物质间的转化关系。其中C、D为气体单质;E为金属单质;其余均为化合物;A含X与W元素,B含Z与V元素。图中部分产物已略去。请按要求回答下列问题:

F的化学式为_________________________________________
上图转化关系中不属于氧化还原反应的有(填编号)______________________________
按要求写出下列反应的方程式
反应②中阳极反应式:_______________________________________
反应⑦的离子方程式:_____________________________________
6.根据下图海水综合利用的工业流程图,判断下列说法正确是的
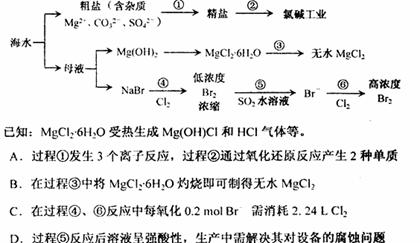
第II卷(64分)
5.氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生如下①主反应和②副反应:

有关物质产率与温度的关系如下图。下列说法正确的是
A.加压可提高NH 生成NO的转化率
生成NO的转化率
B.工业上氨催化氧化生成NO时,反应温度最好控制在780℃以下
C.达到平衡时再充入2molO 反应①的
反应①的 H
H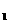 和平衡常数K均保持不变
和平衡常数K均保持不变
D.N 氧化为NO的热化学方程式为
氧化为NO的热化学方程式为

4.在常温下,①PH=2的CH COOH溶液②PH=2的HCl溶液③PH=12的氨水④PH=12的NaOH溶液。有关上述溶液的叙述正确的是
COOH溶液②PH=2的HCl溶液③PH=12的氨水④PH=12的NaOH溶液。有关上述溶液的叙述正确的是
A.四种溶液中的K 相等,由水电离出的c(H
相等,由水电离出的c(H )也相等
)也相等
B.向溶液中加入100mL水后,溶液的PH大小:④>③>①>②
C.若将②、③溶液混合后溶液PH=7,则消耗溶液的体积前者小于后者
D.足量铝粉分别与等体积的①②④溶液充分反应后生成H 的量相等
的量相等
3.下列表述不正确的是
A硫化钠的水解反应为
B在 的溶液中能含有大量
的溶液中能含有大量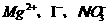
C室温下,在PH=11的溶液中 可以共存
可以共存
D向苯酚钠溶液中通入少量CO 反应为
反应为
2. 用N表示阿伏加德罗常数的值。下列说法正确的是
A.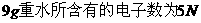
B.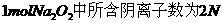
C.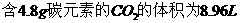
D.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com