
题目列表(包括答案和解析)
8.某溶液中可能含有Br-、NH4+、Cu2+、SO32-,向该溶液中加入少量氯水,溶液仍呈无色,则下列关于该溶液组成的判断正确的是( )。
①肯定不含Br-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有Br-
A.①③ B.①②③ C.①② D.②③④
7.设NA为阿伏加德罗常数,下列说法正确的是( )。
A.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移电子数为NA
B.7.8 g Na2O2含有阴离子数目为0.2NA
C.1L0.5mol/L的(NH4)2SO4溶液中含有NA个NH4+
D.58.5g氯化钠中约含有6.02×1023个氯化钠分子
6.下列变化不能说明发生了化学变化的是( )。
A.变化时有电子的得失或共用电子对的形成
B.变化过程中有旧化学键的断裂和新化学键形成
C.变化时释放出能量
D.变化前后原子的种类和数目没有改变,分子种类增加了
5.有机物的种类繁多,下列有机物命名正确的是( )。
A.CH3CH(OH)CH3 丙醇 B.CH2=CHCH2CH3 1-丁烯
C.CH3CCl2CH3 2-二氯丙烷 D.CH3CH(CH2CH3)CH3 2-乙基丙烷
4.光导纤维被认为是20世纪最伟大的发明之一, 2009年诺贝尔物理学奖授予被誉为“光纤之父”的华人科学家高锟。组成光导纤维主要成分SiO2是( )。
A.分子晶体 B.原子晶体 C.离子晶体 D.金属晶体
3.在通常条件下,下列各组物质的性质排列正确的是( )。
A.熔点: KCl>SiO2> SO2
B.结合质子能力:CH3COO->OH->Cl-
C.沸点:正戊烷>异戊烷>新戊烷
D.稳定性:H2S>H2O>PH3
2.以下表示锂离子结构的轨道表示式是( )。
 A.Li+
B.
C.1s2 D.
A.Li+
B.
C.1s2 D. 
1.2010上海世博会园区建设采用了许多先进的技术,下列做法不能体现节能减排理念的是( )。
A.采用绿颜色涂料 B.使用电动汽车
C.利用太阳能作为能源 D.采用自然采光通风的技术
31、钾元素可以与氧元素在不同条件下生成K2O2、KO2和KO3,如:
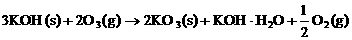
(1)KOH与O3反应,反应前后气体体积减小67.2L(S.T.P.),则生成KO3 g。
(2)将上述生成的混和物用液氨冷却结晶,可得到KO3晶体。它会缓慢分解为KO2和O2:

已知分解后残留固体中含氧的质量分数为0.5063,则KO3的分解百分率为 。(保留两位小数)
(3)已知某样品中含有K2O2、KO2和KO3中的两种,把71.1g该样品加入过量的Al2(SO4)3溶液中,产生白色沉淀23.4g。
①该样品中钾原子与氧原子个数的最简整数比为 。(写出计算过程)
②写出可能存在的组合中两种化合物的物质的量之比。
2009学年第二学期普陀区高三质量调研化学试卷
30、稀有气体在一定条件下也能与某些物质反应,如:Xe与F2在一定条件下可以形成XeF4、XeF6。现有标准状况下的XeF4、XeF6的混合气体1L,密度为10.26g/L。
(1)混合气体的平均摩尔质量为 。(保留两位小数,下同)
(2)混合气体中XeF4的质量为 g。
(3)氟化氙都是强氧化剂,如在水中都能将Cl-氧化成Cl2,并生成Xe(g)和HF。将上述标准状况下的混合气体1L通入含过量Cl-的溶液中,能生成Cl2 mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com