
题目列表(包括答案和解析)
(一)从以上材料获得的信息有:
(1)该消毒液的酸碱性:________,原因是(用离子方程式表示)________。
(2)该消毒液可能具有的化学性质是_________性和________性(任意写出两种)。
(3)写出其中一种因素引起该消毒液失效涉及的化学反应方程式__ __。
7.我国08年遭遇了特大雪灾,我国科学家用氯化钙、尿素、葡萄糖酸钠等为原料成功研制出一种新型复合融雪剂。下列说法正确的是
A.传统的氯化钠融雪剂通过升高水的凝固点实现雪融化
B.传统的氯化钠融雪剂由于价格偏高而减少使用
C.葡萄糖酸钠是强电解质
D.尿素通过CO2与NH3发生化合反应制得
8.用硫酸铁电化浸出黄铜矿精矿工艺中,精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S。下列说法正确的是
A.反应中硫元素被氧化,所有铁元素均被还原 B.还原剂是Fe3+,氧化剂是S2-
C.氧化产物是S,还原产物是Cu2+和Fe2+
D.当转移1mol电子时,46 g CuFeS2参加反应
9.设NA为阿伏加德罗常数。下列叙述中正确的是
A.标准状况下,22.4 L CO2和O2混合气体中含有的氧原子数约为NA
B.2 mol SO2和1 molO2 混合在V2O5存在条件下的密闭容器中反应,反应后分子总数大于2 NA
C.常温常压下,0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.3 NA
D.1 L 1 mol/L的K2CO3溶液中离子总数小于3NA
10.能在溶液中大量共存,加入(NH4)2Fe(SO4)2·6H2O晶体后仍能大量存在的离子组是
A.Na+、H+、Cl-、NO3- B.K+、Ba2+、OH-、I-
C.Na+、Mg2+、Cl-、SO42- D.Cu2+、S2-、Br-、ClO-
11.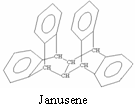 右图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是
右图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是
A.Janusene的分子式为C30H20
B.Janusene属于苯的同系物
C.Janusene苯环上的一氯代物有8种
D.Janusene既可发生氧化反应,又可发生还原反应
12. 根据下列实验现象,所得结论正确的是
根据下列实验现象,所得结论正确的是
A B C D
|
实验 |
实验现象 |
结论 |
|
A |
左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Fe>Cu |
|
B |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
|
C |
白色固体先变为淡黄色,后变为黑色 |
溶解性:Ag2S>AgBr>AgCl |
|
D |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:Cl>C>Si |
13.常温下,一定量的醋酸与氢氧化钠溶液发生中和反应。下列说法正确的是
A.当溶液中c(CH3COO-) = c(Na+)时,醋酸与氢氧化钠恰好完全反应
B.当溶液中c(CH3COO-) = c(Na+)时.一定是氢氧化钠过量
C.当溶液中c(CH3COO-) = c(Na+)>c(H+) = c(OH-)时,一定是醋酸过量
D.当溶液中c(Na+)>c(CH3COO-) >c(OH-)>c(H+)时,一定是氢氧化钠过量
第Ⅱ卷
25.(13分)A、B、C、D为4种常见的短周期元素,常温下A、B可形成两种液态化合物,其最简式分别为BA和B2A;B与D可形成分子X,也可形成阳离子Y,X、Y在水溶液中酸、碱性正好相反;C+的焰色反应呈黄色。
(1)液态X类似B2A,也能微弱自电离产生电子数相同的两种离子,则液态X的电离方程式为:_________________ _____。
(2)M、N是由A、B、C、D四种元素中任意三种组成的不同类型的强电解质,M的水溶液呈碱性,N的水溶液呈酸性,且物质的量浓度相等的M、N溶液中水的电离程度前者小于后者。则M、N分别为(填化学式) ___________、___________;用化学用语分别说明M的水溶液呈碱性、N的水溶液呈酸性的原因: 、 ;若将0.1mol·L-1 M和0.2mol·L-1 N两种溶液等体积混合后所得溶液中离子浓度的大小顺序为:_______________________________________。
(3)氮可以形成多种离子,如N3-、N3-、NH2-、NH4+、N2H5+、N2H62+。N2H6+是由中性分子结合质子形成的,有类似于NH4+的性质。写出Na3N与水反应的化学方程式:_______________________________。② 离子化合物NH5的电子式为:___________ ,写出该物质在低温下与水反应的化学方程式 ,
③
写出N2H 离子与过量强碱溶液反应的离子方程式:_______ __________
。
离子与过量强碱溶液反应的离子方程式:_______ __________
。
26.(15分)下图中的A~H是中学化学中常见的八种物质,所有物质均由短周期元素组成,其中B、F、H都含有同一种元素;B、D、E为单质、其他为化合物,常温常压下C为无色液体,D、E为气体;H的晶体熔点高、硬度大、闪烁着晶莹的光泽。A~H之间的转化关系如图所示。

⑴H的化学式为 、A的电子式为 ;
⑵A、B的混合物加C后,可能发生的反应的化学方程式为 、
。
⑶向F溶液中逐渐滴入盐酸直至过量,若看到的现象是先出现白色沉淀后沉淀消失,写出符合现象的离子方程式 ,与之对应的D、E恰好完全反应生成C时A与B的物质的量之比为: ;
27.(16分)某品牌消毒液包装说明中的部分内容摘录如下:
主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。
21.
(1)AsH3
(2)Br2
(3)a c
(4)
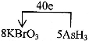
20.(1)铁屑 Fe +2H+=Fe2++H2↑
(2)打开 H2
(3)关闭活塞D,使FeSO4溶液压入B瓶中进行反应
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
19.(1) (2)弱于
(2)弱于
(3)S+2H2SO4(浓) 3SO2↑+2H2O
3SO2↑+2H2O
(4)2H2O2
 2H2O+O2↑(或其他合理答案:)
2H2O+O2↑(或其他合理答案:)
18.
|
各物质(杂质) |
除杂质所需试剂 |
离子方程式 |
|
Fe2O3(Al2O3) |
NaOH溶液 |
Al2O3+2OH-=
2AlO2-+H2O |
|
FeCl2溶液(FeCl3) |
铁粉 |
2Fe3++Fe=3Fe2+ |
|
Na2CO3溶液(NaHCO3) |
适量NaOH溶液 |
HCO3-+OH-= CO32-+H2O
|
|
NaHCO3溶液(Na2CO3) |
过量CO2 |
CO3 2-+CO2+H2O=2HCO3- |
17.(1)a-m=b+n (2)18,7
16.A :HCl B:Cl C:FeCl2 D:FeCl3 E:AgCl
(1)MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
(2) Fe +2H+= Fe 2++H2 ↑
(3) 2Fe 2++Cl2= 2Fe 3++2 Cl-
 (4)2Fe +3Cl2= 2Fe Cl3
(4)2Fe +3Cl2= 2Fe Cl3
(5)Ag+ + Cl -=AgCl↓
21.(9分)某反应中反应物与生成物有: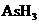 、
、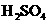 、
、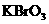 、
、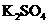 、
、 、
、 和一种未知物质X。
和一种未知物质X。
(1)已知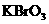 在反应中得到电子,则该反应的还原剂是
。
在反应中得到电子,则该反应的还原剂是
。
(2)已知0.2mol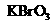 在反应中得到1mol电子生成X,则X的化学式为
。
在反应中得到1mol电子生成X,则X的化学式为
。
(3)根据上述反应可推知 。
a.氧化性: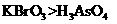 b.氧化性:
b.氧化性: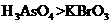
c.还原性: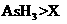 d.还原性:
d.还原性:
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方
向和数目:

第四次月考答案:
20.(10分)图示装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化。实验时必须使用铁屑和6mol·L-1的硫酸,其他试剂任选。填写下列空白:

(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是 。
 A中反应的离子方程式是
。
A中反应的离子方程式是
。
(2)实验开始时先应将活塞D (填“打开”“关闭”或“无关系”),
C中收集到气体的主要成分是 。
(3)简述生成Fe(OH)2的操作过程 。
(4)拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com