
题目列表(包括答案和解析)
26.(14分) 自2009年3月起,从墨西哥、美国等国逐渐扩散到全世界的甲型H1N1型流感爆发疫情,引起全球关注和积极应对。防控专家表示,含氯消毒剂和过氧化物等强氧化性消毒剂可预防甲型H1N1型流感。
(1) 过碳酸钠 (化学式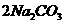 ·
·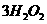 ) 俗称固体双氧水,白色结晶颗粒。过碳酸钠溶于水或受热时,分解生成碳酸钠和过氧化氢,是很好的固体氧释放剂。
) 俗称固体双氧水,白色结晶颗粒。过碳酸钠溶于水或受热时,分解生成碳酸钠和过氧化氢,是很好的固体氧释放剂。
①请你写出过氧化氢的电子式 ,其中氧元素的化合价是 。
②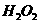 有时可作为矿业废物消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:
有时可作为矿业废物消毒剂,有“绿色氧化剂”的美称,如消除采矿业胶液中的氰化物(如KCN),经以下反应实现: +
+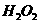 +
+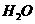 =
= +
+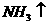 ,则生成物A的化学式为 ,
,则生成物A的化学式为 ,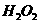 被称为“绿色氧化剂”的理由是
。
被称为“绿色氧化剂”的理由是
。
③某强酸性反应体系中,反应物和生成物共六种物质; 、
、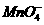 、
、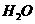 、
、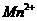 、
、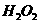 、
、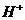 。已知该反应中
。已知该反应中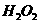 只发生了如下过程:
只发生了如下过程: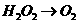 。写出该反应的离子方程式
。
。写出该反应的离子方程式
。
④实验室制 主要有4种方法,用化学方程式写出任意一种 。
主要有4种方法,用化学方程式写出任意一种 。
(2) 碳酸钠水溶液显碱性。用离子方程式解释其原因 ;pH值相同的①碳酸钠溶液、②醋酸钠溶液、③氢氧化钠溶液,其浓度由大到小的顺序是: (填写序号)。
(3) 漂白剂亚氯酸钠 ( ) 在常温黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为:
) 在常温黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为: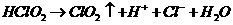 (未配平)。在该反应中,当有1mol
(未配平)。在该反应中,当有1mol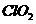 生成时,转移的电子数是 个。
生成时,转移的电子数是 个。
(4) 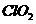 不稳定,可与NaOH溶液、
不稳定,可与NaOH溶液、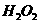 反应,转化为较稳定的亚氯酸钠 (
反应,转化为较稳定的亚氯酸钠 ( )。
)。
该反应的化学方程式为 。
25.(16分) 多巴胺是一种重要的中枢神经传导物质,用来帮助细胞传送脉冲的化学物质,
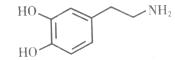 能影响人对事物的欢愉感受,其分子结构如右图所示。
能影响人对事物的欢愉感受,其分子结构如右图所示。
试回答下列问题:
(1) 多巴胺的分子式是 ,在多巴胺的核磁共振氢谱中可以发现有 个特征吸收峰。
(2) 多巴胺分子中的官能团名称是 、 。
(3) 多巴胺属于 有机物 (填写序号)。
①酸性 ②碱性 ③两性
多巴胺可由香兰素与硝基甲烷反应后再经锌汞齐还原水解制得。合成过程可如下图所示:
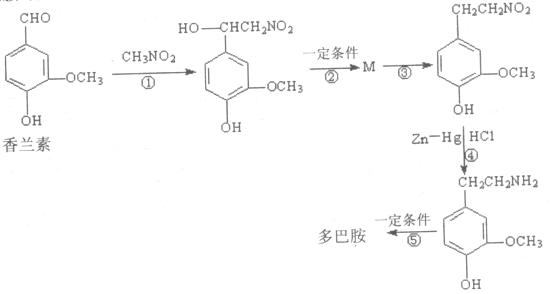
(4) 反应①的反应类型是 。
(5) 反应②的化学方程式是 。
(6) 香兰素的一类同分异构体具有以下特点:
①与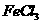 溶液显紫色 ②属于酯类 ③在苯环的一氯取代物只有两种
溶液显紫色 ②属于酯类 ③在苯环的一氯取代物只有两种
写出符合以上条件的所有同分异构体的结构简式 。
12.下列说法正确的是
A.向氯化钡溶液中通入 后没有沉淀,再通入
后没有沉淀,再通入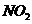 后也不产生沉淀
后也不产生沉淀
B.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
C.常温下,Al、Cu和浓硝酸溶液构成的原电池中Al作负极
D.向浑浊的苯酚溶液中加入少量碳酸钠晶体,振荡后溶液变澄清
11.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍,是Y原子最外层电子数的3倍。下列说法正确的是
A.X的氢化物溶于水显酸性 B.Y的氧化物是离子化合物
C.Z的氢化物比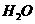 稳定 D.Y离子的半径比Z离子的半径大
稳定 D.Y离子的半径比Z离子的半径大
10.设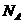 为阿伏加德罗常数,下列说法不正确的是
为阿伏加德罗常数,下列说法不正确的是
A.28g乙烯和28g丙烯中均含有6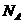 对共用电子对
对共用电子对
B.1L
0.2mol/L的氯化铁溶液中含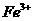 和
和 共0.8
共0.8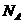
C.标准状况下,11.2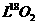 中所含中子数为10
中所含中子数为10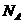
D.2.4g镁作还原剂时失去电子数为0.2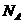
9.下列叙述正确的是
A.90℃纯水的pH<7,说明加热可导致水呈酸性
B.将稀氨水逐滴加入稀盐酸中,当溶液的pH=7时,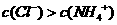
C.在KI溶液中加入 固体,溶液中
固体,溶液中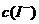 下降
下降
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
8.下列说法中正确的是
A.钢、青铜、硬铝和金刚石都是合金材料
B.所有的分解反应都属于氧化还原反应
C.氨基酸不能通过缩聚反应结合成蛋白质
D.一定条件下,稻草可制得葡萄糖或酒精
7.分类是学习和研究化学的一种常用的科学方法,下列分类合理的是
A.根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸等
B.根据氧化物中是否含有金属元素,将氧化物分为碱性氧化物、酸性氧化物
C.根据化学反应的热效应,将化学反应分为放热反应、吸热反应
D.根据分散系的稳定性大小,将分散系分为胶体、浊液和溶液
6.化学知识在生产和生活中有着广泛的应用,下列说法中不正确的是
A.用天然气代替煤,可防止全球变暖
B.与铜质水龙头连接处的钢质水管易发生锈蚀
C.青霉素的不良反应是过敏反应,因此用药前要进行皮肤敏感试验
D.食盐加碘是防止人体缺碘而加的营养强化剂,能预防地方性甲状腺肿瘤
31. (8 分)[化学--化学与技术] (未命题) 32. (8 分)[化学--物质结构与性质] T、X、Y、Z 是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:

请根据信息回答有关问题(答题时如需表示具体元素,请用相应的元素符号):
(1)T、X、Y 三种元素的电负性由大到小的顺序是 ; (2)写出与X 单质分子互为等电子体的物质的化学式(分子、离子各一种) 、 ; (3)X 的氢化物分子间能形成氢键,Z 的氢化物分子间不易形成氢键,原因是 ;
(4)元素Q 的原子序数是Y 与Z 的原子序数之和
① 元素Q 基态原子的价电子排布式为
;
② 元素Q 与元素T 、X 能形成平面型的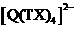 离子,其中Q 与
离子,其中Q 与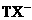 之间的化学键类型为
。
33. (8分)[化学--有机化学基础]
X、Y 都是芳香族化合物,1 mol X 水解得到1 mol Y 和1 mol CH3CH2OH
; X 的相对分子质量不超过200 ,完全燃烧只生成CO2 和H2O ,且分子中碳和氮元素总的质量分数约为81.8%
之间的化学键类型为
。
33. (8分)[化学--有机化学基础]
X、Y 都是芳香族化合物,1 mol X 水解得到1 mol Y 和1 mol CH3CH2OH
; X 的相对分子质量不超过200 ,完全燃烧只生成CO2 和H2O ,且分子中碳和氮元素总的质量分数约为81.8%
(l) X 的分子式是 ; (2) G 和X 互为同分异构体,且具有相同的官能团。用芳香烃A 合成G 路线如下:
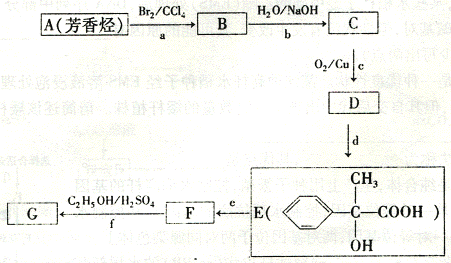
① 上图反应过程中,可以看作是取代反应的是 ; ② 反应E→F 的化学方程式为: ; ③ 写出符合下列条件的F 的同分异构体的结构简式(任写一种): ;
i. 分子内除了苯环外无其他环状结构,且苯环上有2 个对位取代基;
ii. 一定条件下,该物质既能与银氨溶液发生银镜反应,又能和FeCl3 溶液发生显色反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com