
题目列表(包括答案和解析)
25. 现有A─E五种元素,其中C、D、E三种是短周期元素。A、B的单质均为生活中常见的金属,A的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160,B的相对原子质量比A大8。C是金属元素,其原子的M层有一个未成对的p电子;D元素的主族序数是其所在周期序数的3倍;E的某种原子的原子核内没有中子。
(1)请写出A在元素周期表中的位置__________________;写出C的核外电子排布式___________________;D和E按1:1的原子个数比形成的化合物中含有的化学键为______(填“极性键”、“非极性键”或“极性键和非极性键”)。
(2)①写出C单质与强碱溶液反应的离子方程式是_______________________。
②在高温条件下,将D、E组成的气态化合物与A 的粉末充分反应,生成8g E的单质和相应的固态化合物时,放出a kJ 热量,此反应的热化学方程式是
____________________________________________________________。
③A的某种氯化物溶液呈黄色,它与B的单质的反应工业上常用于腐蚀电路板,请写出反应的离子方程式___________________________________ ____。
13.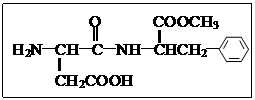 代糖是一种人工合成的甜味剂(sweetener),由于它不会被消化而变为能量供给身体所需,所以适合一些减肥人士食用。目前为止,天冬酰苯丙氨酸甲酯(aspartame)尚未有证据证实它是致癌物质,是糖的最佳代用品,比一般的蔗糖甜160倍。请根据右图结构式判断下列关于aspartame的说法不正确的是
代糖是一种人工合成的甜味剂(sweetener),由于它不会被消化而变为能量供给身体所需,所以适合一些减肥人士食用。目前为止,天冬酰苯丙氨酸甲酯(aspartame)尚未有证据证实它是致癌物质,是糖的最佳代用品,比一般的蔗糖甜160倍。请根据右图结构式判断下列关于aspartame的说法不正确的是
A.是芳香族化合物
B.分子式中含有醛基
C.既能与NaOH溶液反应,也能与HCl反应
D.1mol aspartame最多能与3mol NaOH反应
12.关于下列图示的说法中正确的是
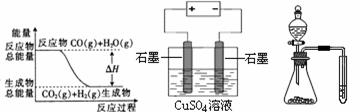
① ② ③ ④
A.图①表示可逆反应“CO(g) + H2O(g) CO2(g)+H2(g)”中的ΔH大于0
CO2(g)+H2(g)”中的ΔH大于0
B.图②为电解硫酸铜溶液的装置,一定时间内,两电极产生单质的物质的量之比一定为1︰1
C.图③实验装置可完成比较乙酸、碳酸、苯酚酸性强弱的实验
D.图④量取0.10 mol•L-1KMnO420.00mL
11.某无色溶液中可能含有I-、NH4+ 、Cu2+、SO32 -(还原性SO32 -大于I-),
向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-;②肯定不含Cu2+;③肯定含有SO32 -;④可能含有I-。
A.①③ B.①②③ C.①② D.②③④

10.已知H2C2O4是二元弱酸,酸式盐NaHC2O4的溶液呈酸性。30℃时,浓度均为0.1mol•L-1 NaHC2O4溶液和Na2C2O4溶液中均存在的关系是
A.c(H+)•c(OH-) =1×10-14
B.c(H+) + c(H2C2O4) =c(C2O42-)+ c(OH-)
C.c(Na+)+ c(H+)= c(OH-)+ c(HC2O4--)+ 2c(C2O42-)
D.c(OH-) = c(H+) +c(HC2O4-)+ 2c(H2C2O4)
9. 不能实现下列物质间直接转化的元素是

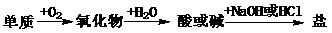
 A. 硅
B. 硫
C. 碳
D. 钠
A. 硅
B. 硫
C. 碳
D. 钠
8.H3AsO3与SnCl2在浓盐酸中可发生以下反应:
3SnCl2+12Cl-+2H3AsO3+6H+=2As+3M+6H2O 关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3 ;② 还原性:Cl->As;③ 每生成1 mol As,反应中转移电子的物质的量为2 mol;④ M为SnCl62-;⑤ M是氧化产物。
A.①④⑤ B.①②⑤ C.①③④ D.①③⑤
7. 据国外媒体报道,“火星快车”号和“金星快车”号探测器日前分别在火星和金星大气层中发现了一种非常特殊的气态化合物。这种化合物的存在不但会导致金星上的温室效应被成倍的放大,而且可能会在火星上也诱发温室效应的产生。它的结构式为:16O=C=18O)。下列说法正确的是
A.16O2与18O2为同素异形体
B.16O=C=18O与16O=C=16O互为同位素
C.16O=C=18O的物理性质与16O=C=16O相同
D.46g16O=C=18O中含有3NA个原子
28.(14分) A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族。己知D元素的一种单质是日常生活中饮水机常用的消毒剂,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质。
(1) C元素在周期表中的位置 。
(2) A元素与水反应的离子方程式是 。
(3) 写出C元素的单质从A、B两元素组成的化合物的水溶液中置换出B元素的单质的
化学方程式 。
(4) 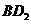 和
和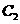 均具有漂白性,二者的漂白原理 。(填“相同”或“不同”)
均具有漂白性,二者的漂白原理 。(填“相同”或“不同”)
(5) B元素的单质在不同的条件下可以与 发生一系列反应:
发生一系列反应:
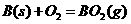 ;
;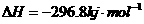
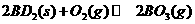 ;
;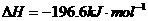
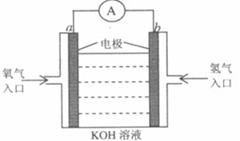 则1 mol
则1 mol 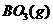 若完全分解成B(s),反应过程中的热效应为
。
若完全分解成B(s),反应过程中的热效应为
。
(6) 氢氧燃料电池能量转化率高,具有广阔的发展前景。
如右图所示,电池中正极的电极反应式为 。
(7) 氢气是合成氨的重要原料,合成氨反应
的热化学方程式如下:
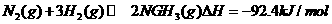
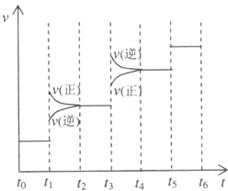
①当合成氨反应达到平衡后,改变某一外界条件
 (不改变
(不改变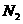 、
、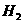 和
和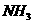 的量),反应速率与时
的量),反应速率与时
间的关系如右图所示。图中 时引起平衡移动
时引起平衡移动
的条件可能是 。其中表示平衡混合物
中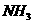 的含量最高的一段时间是
。
的含量最高的一段时间是
。
②温度为T℃时,将2a mol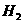 和a mol
和a mol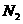 放入0.5 L
放入0.5 L
密闭容器中,充分反应后测得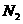 的转化率为50%。则该反应的平衡常数为 。
的转化率为50%。则该反应的平衡常数为 。
27.(14分) 类比是化学学习中常用的方法之一,已知硝酸能把铁氧化成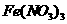 ,但当铁过量时,产物是
,但当铁过量时,产物是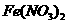 。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当
。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当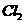 足量时生成
足量时生成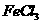 ,当铁粉过量时产物是
,当铁粉过量时产物是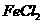 。为验证此观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的
。为验证此观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的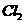 中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分。探究过程如下:
中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分。探究过程如下:
(1) 提出假设:A是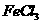 ,B是
,B是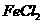 。
。
(2) 设计实验方案:分别取A、B的溶液均进行以下实验,但实验现象相同。请填写下表中的相应空格
|
实验方法 |
实验现象 |
结论 |
|
分别向A、B溶液中加KSCN溶液 |
|
固体物质中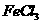 |
分别向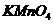 溶液中加入适量A、B溶液 溶液中加入适量A、B溶液 |
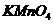 溶液颜色无明显变化 溶液颜色无明显变化 |
固体物质中不含 |
(3) 根据上述实验结论,写出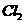 与铁粉加热时发生反应的化学方程式
。
与铁粉加热时发生反应的化学方程式
。
(4) 为进一步探究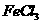 溶液的性质,他又利用A溶液做了如下一些实验,其中明显错
溶液的性质,他又利用A溶液做了如下一些实验,其中明显错
误的是 (填写序号)。
A.将A溶液滴入淀粉碘化钾溶液中,可得到蓝色液体,该液体能产生丁达尔现象
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将A溶液加热蒸干并灼烧,得到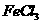 固体
固体
(5) 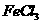 溶液常作印刷电路铜板腐蚀剂,写出反应的离子方程式
。腐蚀后的废液中含有
溶液常作印刷电路铜板腐蚀剂,写出反应的离子方程式
。腐蚀后的废液中含有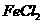 、
、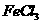 、
、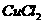 ,某研究性学习小组的同学们设计了两种从废液中回收
,某研究性学习小组的同学们设计了两种从废液中回收 的方案:
的方案:
方案1:向废液中加入过量的铁粉,充分反应后,过滤。在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得到铜,该方案中涉及的四种阳离子的氧化性由强到弱的顺序为: 。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的 已全部析出。该方案中铜作
极,该电极上所发生的电极反应为 (若有多个电极反应,请全部写出) 。方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为: 。
已全部析出。该方案中铜作
极,该电极上所发生的电极反应为 (若有多个电极反应,请全部写出) 。方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com