
题目列表(包括答案和解析)
26.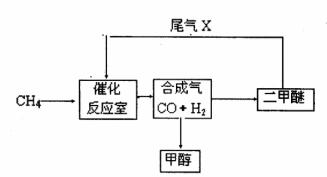 (12分)合成气(CO+H2)是一种重要的化工原料,在化工生产中具有十分广泛的用途。 可以生产被称为21世纪的新型燃料--甲醇、二甲醚(CH3OCH3)等物质。其工艺流程如下:
(12分)合成气(CO+H2)是一种重要的化工原料,在化工生产中具有十分广泛的用途。 可以生产被称为21世纪的新型燃料--甲醇、二甲醚(CH3OCH3)等物质。其工艺流程如下:
(1)写出用合成气生产二甲醚的化学方程式 。
 (2)尾气循环中涉及到以下反应:CH4(g)+H2O(g) CO(g)+3H2(g),请写出某温度下该反应的平衡常数表达式
。
(2)尾气循环中涉及到以下反应:CH4(g)+H2O(g) CO(g)+3H2(g),请写出某温度下该反应的平衡常数表达式
。
(3)工业上一般采用下列两种反应合成甲醇:
 反应Ⅰ: CO(g)+2H2(g)
CH3OH(g)
反应Ⅰ: CO(g)+2H2(g)
CH3OH(g) 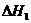
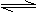 反应Ⅱ:CO2(g)+3H2(g)
CH3(g)+H2O(g)
反应Ⅱ:CO2(g)+3H2(g)
CH3(g)+H2O(g)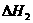
①下表所列数据是反应在不同温度下的化学平衡常数(K)。
|
温度 |
250 |
300 |
350 |
|
K |
2.041 |
0.270 |
0.012 |
由表中数据判断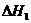 0(填“>”、“=”、“<”)。
0(填“>”、“=”、“<”)。
②已和:
CH3OH(g)+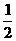 O2(g)
O2(g) CO2(g)+2H2(g) 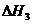 =-192.9kJ·mol-1
=-192.9kJ·mol-1
H2(g)+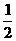 O2(g)
O2(g) H2O(g) 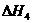 =-241.8kJ·mol-1
=-241.8kJ·mol-1
则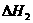 =
。
=
。
(4)以二甲醚、空气、氢氧化钾溶液为原料,铂为电极构成燃料电池。写出该电池负极的电极反应式 。
25.(15分)以下是一些元素的信息,其中有一种元素不在短周期。根据信息完成问题:
|
元素A |
元素B |
元素C |
元素X |
元素Y |
元素Z |
|
单质是一种常见金属,与元素X形成黑色和砖红色两种化合物 |
单质是一种黄绿色气体 |
短周期中金属性最强,与X反应能生成两种化合物 |
最外层电子数是内层电子数的3倍,能形成双原子阴离子 |
单质为双原子分子,结构中 键与 键与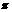 键数目比为1:2 键数目比为1:2 |
阳离子就是一个质子 |
(1)写出A元素基态原子的核外电子排布式 。
(2)B、C、X的简单离子半径由大到小的顺序为 (用元素离子符号表示)。
(3)化合物YZ4B化学键的类型是 ,检验该固体化合 物中阳离子的实验的方法和现象是 。
(4)A元素的单质在潮湿空气中锈蚀生成绿色物质,用一个化学方程式表示锈蚀过程 。
(5)常温下,工业上用惰性电极在电解槽中电解100 L 1.5mol·L-1CB的水溶液时,两极共收集到气体22.4L(标准状况下),计算电解后阴极区溶液的pH= (假设电解前后溶液体积不变)。
13.用铜片、银片设计成如图所示的原电池。以下有关该原电池的叙述正确的是 ( )

A.电子通过盐桥从乙池流向甲池
B.铜导线替换盐桥,原电池仍继续工作
C.开始时,银片上发生的反应是:Ag-e Ag+
D.将铜片浸入AgNO3溶液中发生的化学反应与该原电池总反应相同
第Ⅱ卷(本卷共1 l小题,共180分)
12. 在一密闭容器中充人4 mol SO2和一定量O2,发生反应:
在一密闭容器中充人4 mol SO2和一定量O2,发生反应:
 2SO2(g)+O2(g)
2SO3(g)△H=一196.6 kJ·mol-1。
2SO2(g)+O2(g)
2SO3(g)△H=一196.6 kJ·mol-1。
则下列说法正确的是 ( )
A.为提高反应速率和SO2的转化率选择更高效的催化剂
B.增大压强有利于SO2转化,平衡常数也会增大
C.当放出353.6 kJ热量时,SO2的转化率接近90%
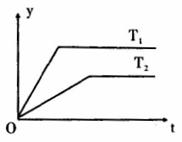
D.右图中纵坐标y为SO3的含量
11.下列离子方程式书写正确的是 ( )
A.氧化铁溶于氢碘酸:Fe2O3+6H+ 2Fe3+3H2O
B.等物质的量的KHCO3和Ba(OH)2的溶液混合:
HCO3-+Ba2++OH一 BaCO3↓+H2O
C.过氧化钠固体与水反应:2O22一+2H2O 4OH一+O2↑
 D.硫化钠水溶液呈碱性的原因:S2-+2H2O H2S↑T+2OH-
D.硫化钠水溶液呈碱性的原因:S2-+2H2O H2S↑T+2OH-
10.某溶液中含有NH4+、H+、SO42-和OH-,对该溶液的描述一定正确的是 ( )
A.该溶液可能呈酸性,也可能呈碱性或中性
B.只能是硫酸铵和硫酸的混合溶液
C.离子浓度由大到小的顺序是:c(NH4+)>c(SO42-)>c(H+)>e(OH一)
D.离子浓度存在下列关系:c(NH4+)+c(H+)=c(OH一)+c(SO42-)
9.如图所示,利用培养皿进行实验。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。
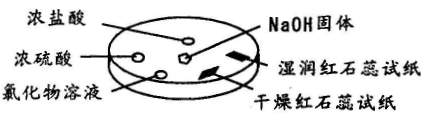
下表中对实验现象所做的解释不正确的是 ( )
|
选项 |
实验现象 |
解释 |
|
A |
浓盐酸附近产生白烟 |
NH3与HCI反应产生了NH4CI固体 |
|
B |
浓硫酸附近无白烟 |
NH3与浓硫酸不发生反应 |
|
C |
干燥红色石蕊试纸不变色,湿润红色石蕊试纸变蓝 |
NH3与水反应生成了NH3.H2O,电离出OH一使红色石蕊试纸变蓝 |
|
D |
氯化物溶液变浑浊 |
可能是AICI3与NH3反应生成AI(OH)3 |
8.用M表示阿伏加德罗常数的数值,下列说法中一定正确的是 ( )
A.1 L l mol·L-1的FeCl3溶液中含有NA个Fe3+
B.4.8g镁与足量盐酸反应时,转移0.2 NA个电子
C.钠与水反应生成1.12 L H2,反应中转移的电子数为0.1NA
D.常温常压下,22g氧气和26g臭氧混合气体所含氧原子总数为3NA
7.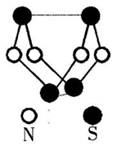 现代无机化学对硫一氮化合物的研究是最为活跃的
现代无机化学对硫一氮化合物的研究是最为活跃的
领域之一。其中右图是已经合成的最著名的硫一
氮化合物的分子结构。下列说法错误的是( )
A.该物质的分子式为S4N4
B.该物质与化合物s2N2互为同素异形体
C.该物质的分子结构中含有极性键
D.该物质中所含化学键S-N键能小于N2中N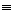 N键能
N键能
30.(15分)根据以下有机物之间的高*考#资^源*网转化关系框图,回答问题:
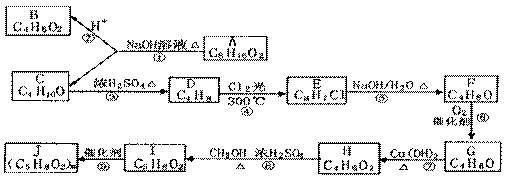
(已知:B的高*考#资^源*网分子结构中带有支链,可由C通过两步氧化反应得到)
(1)D的高*考#资^源*网名称为(用系统命名法命名)____________________。
(2)F中含有的高*考#资^源*网官能团的高*考#资^源*网名称为____________________。
(3)③和⑧的高*考#资^源*网反应类型分别是_______________________、____________________。
(4)写出与H具有相同官能团的高*考#资^源*网H的高*考#资^源*网所有同分异构体的高*考#资^源*网结构简式:__________________________.
(5)B与C可通过酯化反应生成A,反应方程式为_________________________。
(6)分别写出反应⑦和⑨的高*考#资^源*网化学方程式:
⑦_____________________________________________________;
⑨_____________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com