
题目列表(包括答案和解析)
17.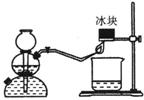 (6分)众所周知,氢气燃烧生成水。然而,资料表明,氢气燃烧时除生成水外,还生成另一产物。某同学用如图所示的实验装置,验证该
(6分)众所周知,氢气燃烧生成水。然而,资料表明,氢气燃烧时除生成水外,还生成另一产物。某同学用如图所示的实验装置,验证该
产物的存在。 实验步骤及现象如下:制H2、验纯,
将火焰对着冰块。
①在小烧杯内加入用硫酸酸化的稀KI淀粉溶液,将小
烧杯放在冰块下方,观察到烧杯中溶液由无色变成了蓝色。
②在另一个小烧杯内加入用硫酸酸化的稀KMn04溶液,将小烧杯放在冰块下方,观察
到烧杯中溶液变成了无色。
(1)另一产物的电子式为 ;
(2)由上述实验中可以归纳出该产物的化学性质有 。
(3)配平实验②中的反应方程式:
□ +□H++□MnO4-=□Mn2++□H2O+□O2↑
16.下列物质能通过化合反应直接制得的是
①FeCl2 ②Fe(OH) 3 ③NH4NO3 ④HCl
A.只有①②③ B.只有②③
C.只有①③④ D.全部
Ⅱ卷(非选择题共86分)
15.下列现象或应用不能用胶体知识解释的是
A.氯化铝溶液中加入小苏打溶液会产生白色沉淀和气体
B.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
C.水泥、冶金厂常用高压电除去工厂烟尘,以减少对空气污染
D.牛油与烧碱溶液共煮,向反应后所得的溶液中加入食盐,则有固体析出
14.几种短周期元素的原子半径及主要化合价如下表:
|
元素代号 |
W |
R |
X |
Y |
Z |
|
原子半径/nm |
0.099 |
0.102 |
0.074 |
0.075 |
0.077 |
|
主要化合价 |
-1、+7 |
-2、+6 |
-2 |
-3,+5 |
+2、+4 |

 下列叙述正确的是
下列叙述正确的是
A.Z与X可形成ZX 、Z2X 等阴离子
B.R的氢化物的沸点高于X的氢化物的沸点
C.R的气态氢化物的稳定性强于W的气态氢化物
D.Z分别与X、R、W均可形成非极性分子的化合物
13.下列各选项中两种粒子所含电子数不相等的是
A.羟甲基(-CH2OH)和甲氧基(CH3O-)
B.硝基(-NO2)和二氧化氮(NO2)
C.亚硝酸(HNO2)和亚硝酸根(NO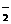 )
)
D.羟基(-OH)和氢氧根(OH-)
10.反应⑴是自海藻灰中提取碘的主要反应,反应⑵是自智利硝石中提取碘的主要反应:
2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2 …………⑴
2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2 …………⑵
下列有关说法正确的是
A.NaI 和NaIO3在一定条件下能反应生成I2
B.I2在反应⑴中是还原产物,在反应⑵中是氧化产物
C.两个反应中生成等量的I2时转移的电子数相等
D.氧化性:MnO2>IO3->I2>SO42->Mn2+
11,aXn-和bYm+是由短周期元素形成的简单离子,已知Xn-比Ym+多两个电子层,下列说法正确的是( )
A,X只能是第三周期元素
B,Y不可能是第二周期元素
C,b≤4
D,a-b+m+n等于10或20
12,某金属的最高价氧化物的相对分子质量为M,最高价氯化物的相对分子质量为N。若其最高正价为X,则用M、N来表示X的关系为 ( )
A、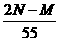 B、
B、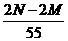 C、
C、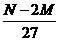 D、
D、
9.下列各组离子,在指定的环境中一定能大量共存的是
A.在pH为7的溶液中:Ag+、K+、SO42-、Cl-
B.在能使pH试纸变深蓝色的溶液中:Na+、S2-、NO3-、CO32-
C.在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3-、
D.在由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、I-
8.能说明碳元素的非金属性比硅元素强的是
A.甲烷比硅化氢稳定 B.碳与SiO2反应生成硅
C.碳酸与硅酸钠溶液反应生成原硅酸 D.高温下SiO2和Na2CO3反应
7、下列离子方程式书写正确的是
A.向碳酸氢钠溶液中滴入少量氢氧化钠 HCO3-+OH-====CO32-+H2O
B.向碳酸氢钾溶液中滴入过量澄清石灰水
2HCO3-+Ca2++2OH-====CO32-+2H2O+CaCO3↓
C.次氯酸钠溶液中通入过量的二氧化硫 ClO-+SO2+H2O====HSO3-+HClO
D.硫酸铜和氢氧化钡溶液混合 Cu2++SO42-+Ba2++2OH-====Cu(OH)2↓+BaSO4↓
6.下列关于盐的反应规律的说法中不正确的是
①盐和酸反应一定生成另一种盐和另一种酸②盐和碱反应一定生成另一种盐和另一种碱③两种盐反应一定生成另外两种盐 ④阳离子相同的两种盐一定不能发生反应
A.只有② B.只有③ C.只有①④ D.①②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com